Физиология реобаза – Методика определения порога силы раздражения (реобаза) и хронаксии — физиология шпоры #
3. Реобаза. Хронаксия.
Существует определенное соотношение между временем действия раздражителя и его амплитудой. Эта зависимость получил название кривой «сила-длительность» или по имени автора Гоорвега-Вейса-Лапика.
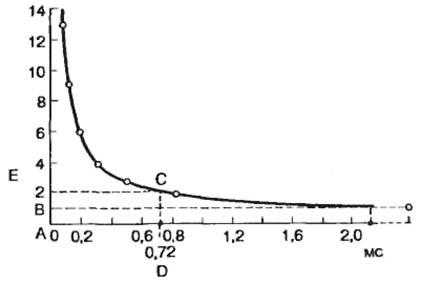
На этой кривой видно, что уменьшение значения тока ниже определенной критической величины не приводит к возбуждению ткани независимо от продолжительности времени, в течение которого действует этот раздражитель, а минимальная величина тока, вызывающая возбуждение , получила название порога раздражения, или реобазы. Величина реобазы определяется разностью между критическим потенциалом и мембранным потенциалом покоя.
С другой стороны, раздражитель должен действовать не меньше определенного времени. Уменьшение времени действия раздражителя ниже критического значения приводит к тому, что раздражитель любой интенсивности не оказывает эффекта. Для характеристики возбудимости ткани по времени ввели понятие порога времени – минимальное (полезное) время, в течение которого должен действовать раздражитель пороговой силы с тем, чтобы вызвать возбуждение (отрезок AC)
Порог времени определяется емкостью и резистивной характеристикой клеточной мембраны. Те.. постоянной времени T = R*C
В связи с тем, что величина реобазы может изменяться, особенно в естественных условиях, и это может привести к значительной погрешности в определении порога времени, Лапик ввел понятие хронаксии для характеристики временных свойств клеточных мембран. Хронаксия – время, в течение которого должен действовать раздражитель удвоенной реобазы. Чтобы вызвать возбуждение. Использование этого критерия позволяет точно измерить временные характеристики возбудимых структур, поскольку измерение происходит на крутом изгибе гиперболы (AD на рис)
4. Дыхание в покое при нагрузке и гипервентиляции.
Необходимо для работы — Секундомер.
Испытуемый делает максимальный вдох и задерживает дыхание. По секундомеру отмечают время наступления непроизвольного вдоха. Затем делается максимальный выдох и задерживается дыхание. Определяют время наступления непроизвольного вдоха. Опыт повторяют после выполнения физической нагрузки (10-15 приседаний).
Без нагрузки | С нагрузкой | |||
На вдохе | На выдохе | На вдохе | ||
Билет № 9.
1. Строение и функции мембраны, ионные каналы и их функции, ионные градиенты.
Согласно современным представлениям, биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Наиболее характерным структурным признаком является то, что мембраны всегда образуют замкнутые пространства, и такая микроструктурная организация мембран позволяет им выполнять важнейшие функции.
Строение и функции клеточных мембран.
Барьерная функция выражается в том, что мембрана при помощи соответствующих механизмов участвует в создании концентрационных градиентов, препятствуя свободной диффузии. При этом мембрана принимает участие в механизмах электрогенеза. К ним относятся механизмы создания потенциала покоя, генерация потенциала действия, механизмы распространения биоэлектрических импульсов по однородной и неоднородной возбудимым структурам.
Регуляторная функция клеточной мембраны заключается в тонкой регуляции внутриклеточного содержимого и внутриклеточных реакций за счет рецепции внеклеточных биологически активных веществ, что приводит к изменению активности ферментных систем мембраны и запуску механизмов вторичных «месенджеров» («посредников»).
Преобразование внешних стимулов неэлектрической природы в электрические сигналы (в рецепторах).
Высвобождение нейромедиаторов в синаптических окончаниях.
Современными методами электронной микроскопии была определена толщина клеточных мембран (6—12 нм). Химический анализ показал, что мембраны в основном состоят из липидов и белков, количество которых неодинаково у разных типов клеток. Сложность изучения молекулярных механизмов функционирования клеточных мембран обусловлена тем, что при выделении и очистке клеточных мембран нарушается их нормальное функционирование. В настоящее время можно говорить о нескольких видах моделей клеточной мембраны, среди которых наибольшее распространение получила жидкостно-мозаичная модель.
Согласно этой модели, мембрана представлена бислоем фосфолипидных молекул, ориентированных таким образом, что гидрофобные концы молекул находятся внутри бислоя, а гидрофильные направлены в водную фазу. Такая структура идеально подходит для образования раздела двух фаз: вне- и внутриклеточной.
В фосфолипидном бислое интегрированы глобулярные белки, полярные участки которых образуют гидрофильную поверхность в водной фазе. Эти интегрированные белки выполняют различные функции, в том числе рецепторную, ферментативную, образуют ионные каналы, являются мембранными насосами и переносчиками ионов и молекул.
Некоторые белковые молекулы свободно диффундируют в плоскости липидного слоя; в обычном состоянии части белковых молекул, выходящие по разные стороны клеточной мембраны, не изменяют своего положения.
Электрические характеристики мембран:
Емкостные свойства в основном определяются фосфолипидным бислоем, который непроницаем для гидратированных ионов и в то же время достаточно тонок (около 5 нм), чтобы обеспечивать эффективное разделение и накопление зарядов и электростатическое взаимодействие катионов и анионов. Кроме того, емкостные свойства клеточных мембран являются одной из причин, определяющих временные характеристики электрических процессов, протекающихщих на клеточных мембранах.
Проводимость (g) — величина, обратная электрическому сопротивлению и равная отношению величины общего трансмембранного тока для данного иона к величине, обусловившей его трансмембранной разности потенциалов.
Через фосфолипидный бислой могут диффундировать различные вещества, причем степень проницаемости (Р), т. е. способность клеточной мембраны пропускать эти вещества, зависит от разности концентраций диффундирующего вещества по обе стороны мембраны, его растворимости в липидах и свойств клеточной мембраны.
Проводимость мембраны является мерой ее ионной проницаемости. Увеличение проводимости свидетельствует об увеличении количества ионов, проходящих через мембрану.
Строение и функции ионных каналов. Ионы Na+, K+, Са2+, Сl- проникают внутрь клетки и выходят наружу через специальные, заполненные жидкостью каналы. Размер каналов довольно мал.
Все ионные каналы подразделяются на следующие группы:
По избирательности:
Селективные, т.е. специфические. Эти каналы проницаемы для строго определенных ионов.
Малоселективные, неспецифические, не имеющие определенной ионной избирательности. Их в мембране небольшое количество.
По характеру пропускаемых ионов:
калиевые
натриевые
кальцевые
хлорные
По скорости инактивации, т.е. закрывания:
быстроинактивирующиеся, т.е. быстро переходящие в закрытое состояние. Они обеспечивают быстро нарастающее снижение МП и такое же быстрое восстановление.
медленноинактирующиеся. Их открывание вызывает медленное снижение МП и медленное его восстановление.
4. По механизмам открывания:
потенциалзависимые, т.е. те которые открываются при определенном уровне потенциала мембраны.
хемозависимые, открывающиеся при воздействии на хеморецепторы мембраны клетки физиологически активных веществ (нейромедиаторов, гормонов и т. д).
В настоящее время установлено, что ионные каналы имеют следующее строение:
1.Селективный фильтр, расположенный в устье канала. Он обеспечивает прохождение через канал строго определенных ионов.
2.Активационные ворота, которые открываются при определенном уровне мембранного потенциала или действии соответствующего ФАВ. Активационные ворота потенциалзависимых каналов имеется сенсор, который открывает их на определенном уровне МП.
3.Инактивационные ворота, обеспечивающие закрывание канала и прекращение проведения ионов по каналу на определенном уровне МП.(Рис).
Неспецифические ионные каналы не имеют ворот.
Селективные ионные каналы могут находиться в трех состояниях, которые определяются положением активационных (м) и инактивационных (h) ворот:
1.Закрытом, когда активационные закрыты, а инактивационные открыты.
2.Активированном, и те и другие ворота открыты.
3.Инактивированном, активационные ворота открыты, а инактивационные закрыты
Функции ионных каналов:
Калиевый (в покое) – генерация потенциала покоя
Натриевый – генерация потенциала действия
Кальциевый — генерация медленных действий
Калиевый (задержанное выпрямление) – обеспечение реполяризации
Калиевый кальций-активируемый – ограничение деполяризации, обусловленной током Са+2
Функцию ионных каналов изучают различными способами. Наиболее распространенным является метод фиксации напряжения, или «voltage-clamp». Сущность метода заключается в том, что с помощью специальных электронных систем в процессе опыта изменяют и фиксируют на определенном уровне мембранный потенциал. При этом измеряют величину ионного тока, протекающего через мембрану. Если разность потенциалов постоянна, то в соответствии с законом Ома величина тока пропорциональна проводимости ионных каналов. В ответ на ступенчатую деполяризацию открываются те или иные каналы, соответствующие ионы входят в клетку по электрохимическому градиенту, т. е. возникает ионный ток, который деполяризует клетку. Это изменение регистрируется с помощью управляющего усилителя и через мембрану пропускается электрический ток, равный по величине, но противоположный по направлению мембранному ионному току. При этом трансмембранная разность потенциалов не изменяется.
Изучение функции отдельных каналов возможно методом локальной фиксации потенциала «path-clamp». Стеклянный микроэлектрод (микропипетка) заполняют солевым раствором, прижимают к поверхности мембраны и создают небольшое разрежение. При этом часть мембраны подсасывается к микроэлектроду. Если в зоне присасывания оказывается ионный канал, то регистрируют активность одиночного канала. Система раздражения и регистрации активности канала мало отличается от системы фиксации напряжения.
Ток через одиночный ионный канал имеет прямоугольную форму и одинаков по амплитуде для каналов различных типов. Длительность пребывания канала в открытом состоянии имеет вероятностный характер, но зависит от величины мембранного потенциала. Суммарный ионный ток определяется вероятностью нахождения в открытом состоянии в каждый конкретный период времени определенного числа каналов.
Наружная часть канала сравнительно доступна для изучения, исследование внутренней части представляет значительные трудности. П. Г. Костюком был разработан метод внутриклеточного диализа, который позволяет изучать функцию входных и выходных структур ионных каналов без применения микроэлектродов. Оказалось, что часть ионного канала, открытая во внеклеточное пространство, по своим функциональным свойствам отличается от части канала, обращенной во внутриклеточную среду.
Именно ионные каналы обеспечивают два важных свойства мембраны: селективность и проводимость.
Селективность, или избирательность, канала обеспечивается его особой белковой структурой. Большинство каналов являются электроуправляемыми, т. е. их способность проводить ионы зависит от величины мембранного потенциала. Канал неоднороден по своим функциональным характеристикам, особенно это касается белковых структур, находящихся у входа в канал и у его выхода (так называемые воротные механизмы).
Рассмотрим принцип работы ионных каналов на примере натриевого канала. Полагают, что в состоянии покоя натриевый канал закрыт. При деполяризации клеточной мембраны до определенного уровня происходит открытие m-активационных ворот (активация) и усиление поступления ионов Na+ внутрь клетки. Через несколько миллисекунд после открытия m-ворот происходит закрытие h-ворот, расположенных у выхода натриевых каналов (инактивация). Инактивация развивается в клеточной мембране очень быстро и степень инактивации зависит от величины и времени действия деполяризующего стимула.
При генерации одиночного потенциала действия в толстом нервном волокне изменение концентрации ионов Na+ во внутренней среде составляет всего 1/100000 от внутреннего содержания ионов Na гигантского аксона кальмара.
Кроме натриевых, в клеточных мембранах установлены другие виды каналов, избирательно проницаемых для отдельных ионов: К+, Са2+, причем существуют разновидности каналов для этих ионов.
Ходжкин и Хаксли сформулировали принцип «независимости» каналов, согласно которому потоки натрия и калия через мембрану независимы друг от друга.
Свойство проводимости различных каналов неодинаково. В частности, для калиевых каналов процесс инактивации, как для натриевых каналов, не существует. Имеются особые калиевые каналы, активирующиеся при повышении внутриклеточной концентрации кальция и деполяризации клеточной мембраны. Активация калий-кальцийзависимых каналов ускоряет реполяризацию, тем самым восстанавливая исходное значение потенциала покоя.
Особый интерес представляют кальциевые каналы. Входящий кальциевый ток, как правило, недостаточно велик, чтобы нормально деполяризовать клеточную мембрану. Чаще всего поступающий в клетку кальций выступает в роли «мессенджера», или вторичного посредника. Активация кальциевых каналов обеспечивается деполяризацией клеточной мембраны, например входящим натриевым током.
Процесс инактивации кальциевых каналов достаточно сложен. С одной стороны, повышение внутриклеточной концентрации свободного кальция приводит к инактивации кальциевых каналов. С другой стороны, белки цитоплазмы клеток связывают кальций, что позволяет поддерживать длительное время стабильную величину кальциевого тока, хотя и на низком уровне; при этом натриевый ток полностью подавляется. Кальциевые каналы играют существенную роль в клетках сердца. Электрогенез кардиомиоцитов рассматривается в главе 7. Электрофизиологические характеристики клеточных мембран исследуют с помощью специальных методов.
studfiles.net
Реобаза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 6 июля 2018; проверки требуют 2 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 6 июля 2018; проверки требуют 2 правки.В электрофизиологии, реобазой называют минимальную силу тока, вызывающую ответ: сокращение мышцы либо биоэлектрический потенциал в одиночной нервной клетке, при неограниченном времени воздействия (на практике обычно не более нескольких сот миллисекунд).
Реобаза составляет половину силы тока, которая вызывает реакцию мышечной или нервной ткани за время хронаксии.
Хронаксия и реобаза – это параметры, описывающие кривую «сила-длительность». Эта кривая иллюстрирует отношение интенсивности (силы тока) порогового стимула к его длительности. С увеличением длительности пробного стимула минимальная сила тока, необходимая для запуска потенциала действия одиночной нервной клетки понижается:[1]
It=QtD{\displaystyle I_{t}={\frac {Q_{t}}{D}}}
It{\displaystyle I_{t}} – сила тока порогового трансмембранного стимула; Qt{\displaystyle Q_{t}}– величина заряда, необходимая для возбуждения одиночной нервной клетки; D
ru.wikipedia.org
Физиология возбудимых тканей. Законы раздражения.
Лекция №2 Для медико-профилактическогофакультета
Кафедра нормальной физиологии им. Н.Ю.Беленкова доцент Продиус Петр Анатольевич
2013 г.
План лекции
•1. Условия возникновения возбуждения.
•2. Понятие о пороговых характеристиках раздражителя.
•3. Кривая «сила-длительность».Понятие о реобазе, полезном времени, хронаксии.
•4. Законы раздражения, действующие в пределах клетки и ткани.
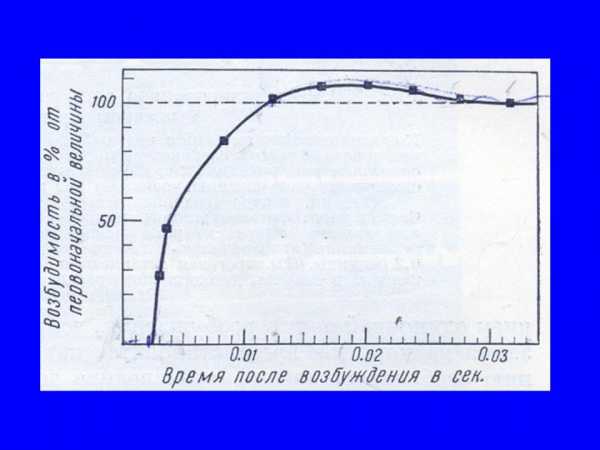
•5. Изменение возбудимости в процессе возбуждения.
•6. Понятие о лабильности. Оптимальные и пессимальные реакции возбудимых тканей.
УСЛОВИЯ ВОЗНИКНОВЕНИЯ ВОЗБУЖДЕНИЯ
А. Структурно-функциональноесостояние мембраны:
достаточный уровень МПП,
определенный уровень Екр.,
уровень порогового потенциала (ΔЕ),
уровень К+,Na+-проницаемости
Б. Значение параметров раздражителя :
достаточная сила,
достаточное время,
достаточный градиент нарастания силы во времени,
для возникновения возбуждения.
С. Воздействие раздражителя на возбудимую ткань.
ПОНЯТИЕ О ПОРОГОВЫХ ХАРАКТЕРИСТИКАХ РАЗДРАЖИТЕЛЯ
Порог раздражителя — минимальная сила раздражителя, способная вызвать возбуждение.
Параметры раздражителя могут быть подпороговыми, пороговыми и сверхпороговыми.
Абсолютный порог силы — минимальная величина силы раздражителя, вызывающая возбуждение.
Абсолютный порог времени — минимальная величина силы раздражителя, вызывающая возбуждение.
Между пороговыми показателями силы и времени раздражителя существует обратная связь. Графически эта связь представлена гиперболой называемой «силадлительность» (иликривой Гоорвейга-Вейса-Лапика).

ЗАВИСИМОСТЬ ПОРОГОВОЙ СИЛЫ РАЗДРАЖИТЕЛЯ ОТ ВРЕМЕНИ ЕГО ДЕЙСТВИЯ
Р – Реобаза
ПВ – Полезное время
Х – Хронаксия
ПОНЯТИЕ О РЕОБАЗЕ, ПОЛЕЗНОМ ВРЕМЕНИ И ХРОНАКСИИ
•Реобаза (Абсолютный порог силы)- минимальная величина силы раздражителя, вызывающая возбуждение.
•Полезное время — это минимальное время, в течение которого должен действовать раздражитель пороговой силы(реобаза) с тем, чтобы вызвать возбуждение.
•Хронаксия – минимальное время, в течение которого должен действовать раздражитель удвоенной реобазы, чтобы вызвать возбуждение.
ЗАКОНЫ РАЗДРАЖЕНИЯ ДЛЯ ВОЗБУДИМОЙ КЛЕТКИ
Для возникновения возбуждения должны быть достаточными
•сила,
•время действия раздражителя,
•крутизна нарастания силы раздражителя во времени.
•
Для клетки закон силы и времени действует
по принципу «все или ничего».
•
Закон градиента нарастания силы во времени проявляется в линейнойзависимости с максимально возможным значением сверхпороговых величин при прямоугольном импульсе.

ЗАКОНЫ РАЗДРАЖЕНИЯ ДЛЯ ВОЗБУДИМОЙ КЛЕТКИ
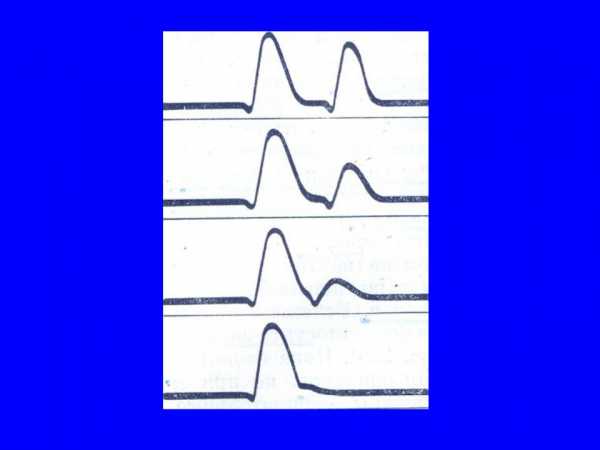
Подписи к предыдущему рисунку.
А. Изменение мембранного потенциала при раздражении нерва.
1А – Сила раздражения < 50% пороговой величины (Пассивная деполяризация мембраны) -электротон. 2А — Сила раздражения50%- 99,9% пороговой
величины (Пассивная деполяризация мембраны +
повышения натриевой проводимости) – локальный ответ.
3А — Сила раздражения — 100% пороговой величины — потенциал действия 4А — Сила раздражения ->100% пороговой величины —
потенциал действия.
Б. Изменение длины мышечного волокна при раздражении.
ЗАКОНЫ РАЗДРАЖЕНИЯ ДЛЯ ВОЗБУДИМОЙ ТКАНИ
•• Для ткани законы силы и времени
•действуют по принципу «силовых
•отношений».
•• Различают:
•• 1). Подпороговые раздражители
•• 2). Пороговые раздражители
•• 3). Сверхпороговые раздражители –
•субмаксимальные, максимальный,
•супермаксимальные раздражители
studfiles.net
3. Реобаза. Хронаксия.
Существует определенное соотношение между временем действия раздражителя и его амплитудой. Эта зависимость получил название кривой «сила-длительность» или по имени автора Гоорвега-Вейса-Лапика.
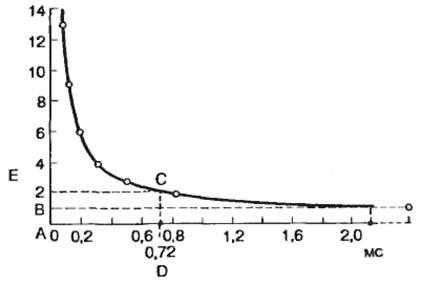
На этой кривой видно, что уменьшение значения тока ниже определенной критической величины не приводит к возбуждению ткани независимо от продолжительности времени, в течение которого действует этот раздражитель, а минимальная величина тока, вызывающая возбуждение , получила название порога раздражения, или реобазы. Величина реобазы определяется разностью между критическим потенциалом и мембранным потенциалом покоя.
С другой стороны, раздражитель должен действовать не меньше определенного времени. Уменьшение времени действия раздражителя ниже критического значения приводит к тому, что раздражитель любой интенсивности не оказывает эффекта. Для характеристики возбудимости ткани по времени ввели понятие порога времени – минимальное (полезное) время, в течение которого должен действовать раздражитель пороговой силы с тем, чтобы вызвать возбуждение (отрезок AC)
Порог времени определяется емкостью и резистивной характеристикой клеточной мембраны. Те.. постоянной времени T = R*C
В связи с тем, что величина реобазы может изменяться, особенно в естественных условиях, и это может привести к значительной погрешности в определении порога времени, Лапик ввел понятие хронаксии для характеристики временных свойств клеточных мембран. Хронаксия – время, в течение которого должен действовать раздражитель удвоенной реобазы. Чтобы вызвать возбуждение. Использование этого критерия позволяет точно измерить временные характеристики возбудимых структур, поскольку измерение происходит на крутом изгибе гиперболы (AD на рис)
4. Дыхание в покое при нагрузке и гипервентиляции.
Необходимо для работы — Секундомер.
Испытуемый делает максимальный вдох и задерживает дыхание. По секундомеру отмечают время наступления непроизвольного вдоха. Затем делается максимальный выдох и задерживается дыхание. Определяют время наступления непроизвольного вдоха. Опыт повторяют после выполнения физической нагрузки (10-15 приседаний).
Испытуемый делает гипервентиляцию легких, делает глубокий вдох и задерживает дыхание. По секундомеру отмечается время наступления непроизвольного выдоха. Сравнивают полученные результаты.
Без нагрузки | С нагрузкой | |||
На вдохе | На выдохе | На вдохе | На выдохе | |
Билет № 9.
1. Строение и функции мембраны, ионные каналы и их функции, ионные градиенты.
Согласно современным представлениям, биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Наиболее характерным структурным признаком является то, что мембраны всегда образуют замкнутые пространства, и такая микроструктурная организация мембран позволяет им выполнять важнейшие функции.
Строение и функции клеточных мембран.
Барьерная функция выражается в том, что мембрана при помощи соответствующих механизмов участвует в создании концентрационных градиентов, препятствуя свободной диффузии. При этом мембрана принимает участие в механизмах электрогенеза. К ним относятся механизмы создания потенциала покоя, генерация потенциала действия, механизмы распространения биоэлектрических импульсов по однородной и неоднородной возбудимым структурам.
Регуляторная функция клеточной мембраны заключается в тонкой регуляции внутриклеточного содержимого и внутриклеточных реакций за счет рецепции внеклеточных биологически активных веществ, что приводит к изменению активности ферментных систем мембраны и запуску механизмов вторичных «месенджеров» («посредников»).
Преобразование внешних стимулов неэлектрической природы в электрические сигналы (в рецепторах).
Высвобождение нейромедиаторов в синаптических окончаниях.
Современными методами электронной микроскопии была определена толщина клеточных мембран (6—12 нм). Химический анализ показал, что мембраны в основном состоят из липидов и белков, количество которых неодинаково у разных типов клеток. Сложность изучения молекулярных механизмов функционирования клеточных мембран обусловлена тем, что при выделении и очистке клеточных мембран нарушается их нормальное функционирование. В настоящее время можно говорить о нескольких видах моделей клеточной мембраны, среди которых наибольшее распространение получила жидкостно-мозаичная модель.
Согласно этой модели, мембрана представлена бислоем фосфолипидных молекул, ориентированных таким образом, что гидрофобные концы молекул находятся внутри бислоя, а гидрофильные направлены в водную фазу. Такая структура идеально подходит для образования раздела двух фаз: вне- и внутриклеточной.
В фосфолипидном бислое интегрированы глобулярные белки, полярные участки которых образуют гидрофильную поверхность в водной фазе. Эти интегрированные белки выполняют различные функции, в том числе рецепторную, ферментативную, образуют ионные каналы, являются мембранными насосами и переносчиками ионов и молекул.
Некоторые белковые молекулы свободно диффундируют в плоскости липидного слоя; в обычном состоянии части белковых молекул, выходящие по разные стороны клеточной мембраны, не изменяют своего положения.
Электрические характеристики мембран:
Емкостные свойства в основном определяются фосфолипидным бислоем, который непроницаем для гидратированных ионов и в то же время достаточно тонок (около 5 нм), чтобы обеспечивать эффективное разделение и накопление зарядов и электростатическое взаимодействие катионов и анионов. Кроме того, емкостные свойства клеточных мембран являются одной из причин, определяющих временные характеристики электрических процессов, протекающихщих на клеточных мембранах.
Проводимость (g) — величина, обратная электрическому сопротивлению и равная отношению величины общего трансмембранного тока для данного иона к величине, обусловившей его трансмембранной разности потенциалов.
Через фосфолипидный бислой могут диффундировать различные вещества, причем степень проницаемости (Р), т. е. способность клеточной мембраны пропускать эти вещества, зависит от разности концентраций диффундирующего вещества по обе стороны мембраны, его растворимости в липидах и свойств клеточной мембраны.
Проводимость мембраны является мерой ее ионной проницаемости. Увеличение проводимости свидетельствует об увеличении количества ионов, проходящих через мембрану.
Строение и функции ионных каналов. Ионы Na+, K+, Са2+, Сl- проникают внутрь клетки и выходят наружу через специальные, заполненные жидкостью каналы. Размер каналов довольно мал.
Все ионные каналы подразделяются на следующие группы:
По избирательности:
Селективные, т.е. специфические. Эти каналы проницаемы для строго определенных ионов.
Малоселективные, неспецифические, не имеющие определенной ионной избирательности. Их в мембране небольшое количество.
По характеру пропускаемых ионов:
калиевые
натриевые
кальцевые
хлорные
По скорости инактивации, т.е. закрывания:
быстроинактивирующиеся, т.е. быстро переходящие в закрытое состояние. Они обеспечивают быстро нарастающее снижение МП и такое же быстрое восстановление.
медленноинактирующиеся. Их открывание вызывает медленное снижение МП и медленное его восстановление.
4. По механизмам открывания:
потенциалзависимые, т.е. те которые открываются при определенном уровне потенциала мембраны.
хемозависимые, открывающиеся при воздействии на хеморецепторы мембраны клетки физиологически активных веществ (нейромедиаторов, гормонов и т. д).
В настоящее время установлено, что ионные каналы имеют следующее строение:
1.Селективный фильтр, расположенный в устье канала. Он обеспечивает прохождение через канал строго определенных ионов.
2.Активационные ворота, которые открываются при определенном уровне мембранного потенциала или действии соответствующего ФАВ. Активационные ворота потенциалзависимых каналов имеется сенсор, который открывает их на определенном уровне МП.
3.Инактивационные ворота, обеспечивающие закрывание канала и прекращение проведения ионов по каналу на определенном уровне МП.(Рис).
Неспецифические ионные каналы не имеют ворот.
Селективные ионные каналы могут находиться в трех состояниях, которые определяются положением активационных (м) и инактивационных (h) ворот:
1.Закрытом, когда активационные закрыты, а инактивационные открыты.
2.Активированном, и те и другие ворота открыты.
3.Инактивированном, активационные ворота открыты, а инактивационные закрыты
Функции ионных каналов:
Калиевый (в покое) – генерация потенциала покоя
Натриевый – генерация потенциала действия
Кальциевый — генерация медленных действий
Калиевый (задержанное выпрямление) – обеспечение реполяризации
Калиевый кальций-активируемый – ограничение деполяризации, обусловленной током Са+2
Функцию ионных каналов изучают различными способами. Наиболее распространенным является метод фиксации напряжения, или «voltage-clamp». Сущность метода заключается в том, что с помощью специальных электронных систем в процессе опыта изменяют и фиксируют на определенном уровне мембранный потенциал. При этом измеряют величину ионного тока, протекающего через мембрану. Если разность потенциалов постоянна, то в соответствии с законом Ома величина тока пропорциональна проводимости ионных каналов. В ответ на ступенчатую деполяризацию открываются те или иные каналы, соответствующие ионы входят в клетку по электрохимическому градиенту, т. е. возникает ионный ток, который деполяризует клетку. Это изменение регистрируется с помощью управляющего усилителя и через мембрану пропускается электрический ток, равный по величине, но противоположный по направлению мембранному ионному току. При этом трансмембранная разность потенциалов не изменяется.
Изучение функции отдельных каналов возможно методом локальной фиксации потенциала «path-clamp». Стеклянный микроэлектрод (микропипетка) заполняют солевым раствором, прижимают к поверхности мембраны и создают небольшое разрежение. При этом часть мембраны подсасывается к микроэлектроду. Если в зоне присасывания оказывается ионный канал, то регистрируют активность одиночного канала. Система раздражения и регистрации активности канала мало отличается от системы фиксации напряжения.
Ток через одиночный ионный канал имеет прямоугольную форму и одинаков по амплитуде для каналов различных типов. Длительность пребывания канала в открытом состоянии имеет вероятностный характер, но зависит от величины мембранного потенциала. Суммарный ионный ток определяется вероятностью нахождения в открытом состоянии в каждый конкретный период времени определенного числа каналов.
Наружная часть канала сравнительно доступна для изучения, исследование внутренней части представляет значительные трудности. П. Г. Костюком был разработан метод внутриклеточного диализа, который позволяет изучать функцию входных и выходных структур ионных каналов без применения микроэлектродов. Оказалось, что часть ионного канала, открытая во внеклеточное пространство, по своим функциональным свойствам отличается от части канала, обращенной во внутриклеточную среду.
Именно ионные каналы обеспечивают два важных свойства мембраны: селективность и проводимость.
Селективность, или избирательность, канала обеспечивается его особой белковой структурой. Большинство каналов являются электроуправляемыми, т. е. их способность проводить ионы зависит от величины мембранного потенциала. Канал неоднороден по своим функциональным характеристикам, особенно это касается белковых структур, находящихся у входа в канал и у его выхода (так называемые воротные механизмы).
Рассмотрим принцип работы ионных каналов на примере натриевого канала. Полагают, что в состоянии покоя натриевый канал закрыт. При деполяризации клеточной мембраны до определенного уровня происходит открытие m-активационных ворот (активация) и усиление поступления ионов Na+ внутрь клетки. Через несколько миллисекунд после открытия m-ворот происходит закрытие h-ворот, расположенных у выхода натриевых каналов (инактивация). Инактивация развивается в клеточной мембране очень быстро и степень инактивации зависит от величины и времени действия деполяризующего стимула.
При генерации одиночного потенциала действия в толстом нервном волокне изменение концентрации ионов Na+ во внутренней среде составляет всего 1/100000 от внутреннего содержания ионов Na гигантского аксона кальмара.
Кроме натриевых, в клеточных мембранах установлены другие виды каналов, избирательно проницаемых для отдельных ионов: К+, Са2+, причем существуют разновидности каналов для этих ионов.
Ходжкин и Хаксли сформулировали принцип «независимости» каналов, согласно которому потоки натрия и калия через мембрану независимы друг от друга.
Свойство проводимости различных каналов неодинаково. В частности, для калиевых каналов процесс инактивации, как для натриевых каналов, не существует. Имеются особые калиевые каналы, активирующиеся при повышении внутриклеточной концентрации кальция и деполяризации клеточной мембраны. Активация калий-кальцийзависимых каналов ускоряет реполяризацию, тем самым восстанавливая исходное значение потенциала покоя.
Особый интерес представляют кальциевые каналы. Входящий кальциевый ток, как правило, недостаточно велик, чтобы нормально деполяризовать клеточную мембрану. Чаще всего поступающий в клетку кальций выступает в роли «мессенджера», или вторичного посредника. Активация кальциевых каналов обеспечивается деполяризацией клеточной мембраны, например входящим натриевым током.
Процесс инактивации кальциевых каналов достаточно сложен. С одной стороны, повышение внутриклеточной концентрации свободного кальция приводит к инактивации кальциевых каналов. С другой стороны, белки цитоплазмы клеток связывают кальций, что позволяет поддерживать длительное время стабильную величину кальциевого тока, хотя и на низком уровне; при этом натриевый ток полностью подавляется. Кальциевые каналы играют существенную роль в клетках сердца. Электрогенез кардиомиоцитов рассматривается в главе 7. Электрофизиологические характеристики клеточных мембран исследуют с помощью специальных методов.
studfiles.net
81. Методика определения порога силы раздражения (реобаза) и хронаксии.
Хронаксиметрия— методика измерения хронаксии для исследования возбудимости живых тканей с учетом не только силы раздражителя, но и фактора времени — длительности действия раздражителя. Хронаксия — наименьшее время, в течение которого постоянный электрический ток силой в 2 раза большей порогового может вызвать реакцию.
Вопрос о значении времени как фактора, определяющего деятельность различных систем, был разработан Н. Е. Введенским при исследовании лабильности. Опытами ряда физиологов была установлена зависимость порогового эффекта как от силы раздражителя, так и от времени его действия. Эта зависимость выражается кривой силы — длительности порогового раздражителя (ABCна рис. 1). Данная кривая наиболее полно характеризует возбудимость ткани, но для ее построения необходимо для каждой силы тока определить пороговую длительность. Лапик (L.Lapicque) предложил определять кривую силы — длительности только по двум точкам — реобазе и хронаксии. Реобаза — пороговая сила тока при достаточной его длительности, при которой фактор времени уже не играет определяющей роли (HL=OM). Реобаза выражается в вольтах или миллиамперах. Для измерения хронаксии надо удвоитьpeo6aзy(FH=ЕК) и найти наименьшее время действия удвоенного тока (DE=OKна рис. 1). Хронаксию выражают в миллисекундах. Удалось показать, что возбудимость всех живых образований характеризуется однотипной гиперболической кривой силы — длительности. Различие заключается лишь в абсолютных величинах реобазы и хронаксии. Были установлены общебиологические закономерности — эволюция хронаксии в филогенезе и онтогенезе. Так, при переходе от медленно сокращающихся гладких мышц к быстро сокращающимся поперечнополосатым хронаксия укорачивается в тысячу раз. Большая величина хронаксии мышц эмбриона укорачивается в раннем постнатальном периоде и достигает самых коротких величин у взрослых.
Французский невропатолог Бургиньон (G.Bourguignon) в 1915 г. создал клиническую хронаксиметрию. Для определения хронаксии были применены разряды конденсаторов различной емкости. На рис. 2 дана принципиальная схема конденсаторного хронаксиметра, а на рис. 3 и 4 — общий вид приборов разной конструкции. Исследование хронаксии различных мышц и нервов у здоровых и больных выявило ряд закономерностей. В норме хронаксия мышц колеблется в пределах 0,04—1,0 м/сек. Имеется определенное соотношение хронаксии мышц-антагонистов; хронаксия сгибателей на руках в 2—3 раза короче, чем у разгибателей, хронаксия дистальных мышц конечностей длиннее, чем проксимальных.
Учение о хронаксии выдвинуло понятие изохронизма. Распространение возбуждения с одной ткани на другую (например, с нерва на мышцу) обусловлено изохронизмом, т. е. способностью этих тканей развивать возбуждение с одинаковой скоростью. Об этом свидетельствуют одинаковые или близкие хронаксии нерва и мышцы. Изохронизмом отдельных звеньев рефлекторной дуги объясняется и возможность прохождения возбуждения по сложным рефлекторным путям. Если по какой-либо причине хронаксия одного звена будет заметно отличаться от хронаксии другого, то возникнет гетерохронизм, препятствующий передаче возбуждения. Ряд советских исследователей выдвинул идею о динамическом изохронизме, который не предсуществует, а создается в процессе физиологической деятельности.
Уровень хронаксии мышц обусловлен в значительной степени состоянием нервных центров. Хронаксия мышц, сохраняющих обычную связь с ЦНС, называется субординационной. Хронаксия мышц, лишенных этой связи, именуется конституциональной и зависит от свойств самих мышц.
Повреждения иннервационного аппарата мышцы, поражения периферического неврона (например, при полиомиелите) влекут за собой резкое удлинение моторной хронаксии. Хронаксиметрию применяют в неврологической, хирургической, частично терапевтической клиниках. Дерматологическая, офтальмологическая, отиатрическая клиники заинтересованы в определении сенсорной хронаксии. Кожную чувствительную, зрительную, вестибулярную хронаксии исследуют по ощущению или рефлекторной реакции.
Хронаксиметрия помогает поставить ранний диагноз или уточнить его, обосновать прогноз, выявить эффективность лечебных мероприятий.
Хронаксиметрия имеет большое практическое значение, расширяя возможности электродиагностики
studfiles.net
Реобаза — Большая советская энциклопедия
Возбуждение (биологическое), реакция живой клетки на раздражение, выработанная в процессе эволюции. При В. живая система переходит из состояния относительного физиологического покоя к деятельности (…
Лапик (Lapicque) Луи (1.8.1866, Эпиналь, — 7.12.1952, Париж), французский физиолог, член Парижской АН (1930) и Французской медицинской академии (1925). Профессор Парижского университета (1919-36)…
Хронаксия (от греч. chronos — время и axia — цена, мера), наименьшее время действия на ткань постоянного электрического тока удвоенной пороговой силы, вызывающего возбуждение ткани. Понятие «Х.»…
Возбудимость, раздражимость, способность живых клеток (от простейших одноклеточных организмов до нервных клеток человека) воспринимать изменения внешней среды и отвечать на эти изменения (раздражения)…
Порог раздражения (в физиологии нервных и мышечных клеток), наименьшая сила раздражителя (обычно электрического тока), способная вызвать распространяющийся потенциал действия; мера возбудимости клетки…
Реобаза (от греч. rhéos — течение, поток и básis — ход, движение; основание), наименьшая сила постоянного электрического тока, вызывающая при достаточной длительности его действия возбуждение в живых тканях. Понятие Р. ввёл в физиологию Л. Лапик в 1909, определяя зависимость между силой тока и длительностью его действия при изучении наименьшего (порогового) эффекта возбудимых тканей. Р., как и хронаксия, даёт представление о возбудимости тканей и органов по порогу силы и длительности действия раздражения. Р. соответствует порогу раздражения и выражается в вольтах или миллиамперах. Значение Р. можно вычислить по формуле: i = a/t + b, где i — сила тока, t — длительность его действия, а и b — константы, определяемые свойствами ткани. Константа b является Р., так как при длительном действии раздражающего тока отношение a/t будет очень мало и i практически равняется b. Р. нередко называются пороговые значения не только электрических, но и других раздражителей.
allencyclopedia.ru
Физиология возбудимых тканей — Информация
Физиология возбудимых тканей
Введение
Раздражимость — это общее свойство тканей реагировать на различные раздражители.
Возбудимость — более узкое понятие, которое характеризует свойство тканей возбуждаться в ответ на действие раздражителя. Ткани, обладающие этим свойством, называются возбудимыми. Проявляется возбуждение возникновением потенциала действия. В основе возбуждения лежат сложные физико-химические процессы. Начальный пусковой момент возбуждения — изменения ионной проницаемости и электрических потенциалов мембраны. Возбудимые ткани имеют ряд свойств: раздражимость — способность тканей воспринимать раздражение, возбудимость — способность тканей реагировать возбуждением на раздражение, проводимость — способность распространять возбуждение, лабильность — скорость протекания элементарных циклов возбуждения. Лабильность отражает время, в течение которого ткань восстанавливает работоспособность после очередного цикла возбуждения. Порог раздражения (в физиологии нервных и мышечных клеток), наименьшая сила раздражителя (обычно электрического тока), способная вызвать распространяющийся потенциал действия
Методы изучения описанных явлений разнообразны. Так, о возбудимости можно судить по наименьшей силе раздражителя, необходимой для возникновения той или иной рефлекторной реакции или по пороговой силе тока или пороговому сдвигу потенциала, достаточным для возникновения ПД. Здесь необходимо ввести такие понятия, как реобаза и хронаксия. Реобаза (от греч. rheos — течение, поток и basis — ход, движение; основание), наименьшая сила постоянного электрического тока, вызывающая при достаточной длительности его действия возбуждение в живых тканях. Понятие реобазы и хронаксии ввёл в физиологию Л. Лапик в 1909, определяя зависимость между силой тока и длительностью его действия при изучении наименьшего (порогового) эффекта возбудимых тканей. Реобаза, как и хронаксия, даёт представление о возбудимости тканей и органов по порогу силы и длительности действия раздражения. Реобаза соответствует порогу раздражения и выражается в вольтах или миллиамперах. Значение реобазы можно вычислить по формуле: i = a/t + b, где i — сила тока, t — длительность его действия, а и b — константы, определяемые свойствами ткани. Константа b является Р., так как при длительном действии раздражающего тока отношение a/t будет очень мало и i практически равняется b. Р. нередко называются пороговые значения не только электрических, но и других раздражителей. Хронаксия (от греч. chronos — время и axia — цена, мера), наименьшее время действия на ткань постоянного электрического тока удвоенной пороговой силы (удвоенной реобазы), вызывающего возбуждение ткани. Было также экспериментально установлено (голландский физик Л. Горвег, 1892, французский физиолог Ж. Вейс, 1901), что величина стимула, вызывающего возбуждающий эффект в тканях, находится в обратной зависимости от длительности его действия и графически выражается гиперболой — кривая <сила — время. Минимальная сила тока, которая при неограниченно долгом действии вызывает эффект возбуждения (реобаза), соответствует на рисунке отрезку OA (BC). Наименьшее т. н. полезное время действия порогового раздража
ющего стимула соответствует отрезку OC (полезное потому, что дальнейшее увеличение времени действия тока не имеет значения для возникновения потенциала действия). При кратковременных раздражениях кривая силы — времени становится параллельной оси ординат, т. е. возбуждение не возникает при любой силе раздражителя. Приближение кривой асимптотически к линии, параллельной абсциссе, не позволяет достаточно точно определять полезное время, т.к. незначительные отклонения реобазы, отражающие изменения функционального состояния биологических мембран в покое, сопровождаются значительными колебаниями времени раздражения. В связи с этим Лапик предложил измерять другую условную величину — хронаксию, т. е. время действия раздражителя, равное двойной реобазе [на рисунке соответствует отрезку OD (EF)]. При данной величине раздражителя наименьшее время его действия, при котором возможен пороговый эффект, равно OF. Установлено, что форма кривой, характеризующей возбудимость ткани в зависимости от интенсивности и длительности действия раздражителя, однотипна для самых разнообразных тканей. Различия между ними касаются только абсолютного значения соответствующих величин и, прежде всего, времени, т. е. возбудимые ткани отличаются друг от друга временной константой раздражения. Лабильность можно измерить, раздражая ткань электрическим током различной частоты. Момент, когда ткань произойдёт преобразование ритма (ткань перестанет воспроизводить заданный ритм без изменений) и будет лабильностью данной ткани. Единицы её измерения — количество воспроизводимых импульсов за единицу времени [имп./сек.(мин.), и т. д. ]. Проводимость можно охарактеризовать расстоянием, преодолённым импульсом за единицу времени, то есть скоростью распространения импульса.
История вопроса.
Изучался этот вопрос давно. Многих учёных интересовал тот факт, что некоторые животные способны генерировать <электрический ток. Это явление было названо <животное электричество. К этому времени относится начало исследований итальянского физиолога и врача Л. Гальвани, заложивших основу учения о Б. п. Многолетний научный спор (1791-97) между Л. Гальвани и физиком А. Вольта о природе <животного электричества завершился двумя крупными открытиями: были получены факты о существован
www.studsell.com
