Стимуляторы гемопоэза: Стимуляторы гемопоэза: описание фармакологической группы
| Веро-Эпоэтин | Лиофилизат д/пригот. р-ра д/в/в и п/к введения 10 000 МЕ: фл. 1, 5 или 10 шт. рег. №: ЛС-000258 от 18.05.10 | |||
| Веро-Эпоэтин | Лиофилизат д/пригот. | |||
| Веро-Эпоэтин | Лиофилизат д/пригот. р-ра д/в/в и п/к введения 2000 МЕ: фл. 1, 5 или 10 шт. рег. №: ЛС-000258 от 18.05.10 | |||
| Веро-Эпоэтин | Лиофилизат д/пригот. | |||
| Вирутер® | Р-р д/ректальн. введения 10 мг/мл: фл. 25 мл или 50 мл рег. №: ЛП-001823 от 06.09.12 Дата перерегистрации: 24.06.16 | |||
| Нуклеоспермат натрия | Р-р д/инъекц. | |||
| Нуклеоспермат натрия | Р-р д/инъекц. 75 мг/5 мл: амп. 1 шт. рег. №: ЛС-002093 от 07.02.12 | |||
| Эпостим | Р-р д/в/в и п/к введения 10 000 МЕ/1 мл: шприцы 1или 3 шт; амп. | |||
| Эпостим | Р-р д/в/в и п/к введения 1000 МЕ/1 мл: шприцы 1или 3 шт., ампулы 5 или 10 шт., флаконы 1 или 5 шт. рег. №: ЛСР-002490/07 от 28.08.07 | |||
| Эпостим | Р-р д/в/в и п/к введения 10000 МЕ/1 мл: шприцы 1 или 3 шт; амп. | |||
| Эпостим | Р-р д/в/в и п/к введения 2000 МЕ/1 мл: шприцы 1 или 3 шт; амп. 5 или 10 шт. рег. №: ЛСР-002490/07 от 22.03.12 | |||
| Эпостим | Р-р д/в/в и п/к введения 2000 МЕ/1 мл: шприцы 1 или 3 шт; амп. | |||
| Эпостим | Р-р д/в/в и п/к введения 4000 МЕ/1 мл: шприцы 1или 3 шт., ампулы 5 ил 10 шт., флаконы 1 или 5 шт. рег. №: ЛСР-002490/07 от 28.08.07 | |||
| Эпостим | Р-р д/в/в и п/к введения 5000 МЕ/1 мл: шприцы 1 или 3 шт; амп. | |||
| Эпоэтин бета | Р-р д/в/в и п/к введения 500 МЕ: 1 мл амп. 5 или 10 шт. рег. №: Р N000525/01 от 20.01.12 Дата перерегистрации: 15.08.13Р-р д/в/в и п/к введения 2000 МЕ: 1 мл амп. Р-р д/в/в и п/к введения 3000 МЕ: 1 мл амп. 5 или 10 шт. рег. №: Р N000525/01 от 20.01.12 Дата перерегистрации: 15.08.13Р-р д/в/в и п/к введения 4000 МЕ: 1 мл амп. 5 или 10 шт. рег. №: Р N000525/01 от 20.01.12 Дата перерегистрации: 15.08.13 | |||
| Полидан™ (Натрия нуклеоспермат) | Р-р д/инъекц. Р-р д/инъекц. 75 мг/5 мл: фл. 1 или 5 шт. рег. №: П N000552/01-2001 от 24.07.01 | |||
| Эритростим® | Р-р д/в/в и п/к введения 500 МЕ/1 мл: амп. 5, 10 или 100 шт. Р-р д/в/в и п/к введения 2000 МЕ/1 мл: амп. 5, 10, 50 или 100 шт., флаконы 50 или 100 шт. рег. №: Р N000525/01 от 17.11.06Р-р д/в/в и п/к введения 3000 МЕ/1 мл: амп. 5, 10, 50 или 100 шт., флаконы 50 или 100 шт. рег. №: Р N000525/01 от 17.11.06Р-р д/в/в и п/к введения 4000 МЕ/1 мл: амп. или флаконы 5, 10, 50 или 100 шт. рег. №: Р N000525/01 от 17.11.06 | |||
| Эритростим® | Р-р д/инъекц. |
Стимуляторы гемопоэза – препараты, описание фармакологической группы
Процесс образования форменных элементов крови (лейкоцитов, эритроцитов и тромбоцитов) называется кроветворением. Стимуляторы гемопоэза – это лекарственные препараты, действие которых направлено на стимуляцию процесса пролиферации стволовых клеток костного мозга, их дифференциации и созревания специализированных клеток крови. Например, стимуляция эритропоэза (формирование эритроцитов) приводит к повышению уровня насыщения крови гемоглобином (основному переносчику кислорода к органам и тканям), что предотвращает развитие анемии, как осложнения при тяжелых заболеваниях различной этиологии Важное значение имеют и препараты, стимулирующие созревание тромбоцитов в мегакариоцитах костного мозга, при лечении и профилактики тромбоцитопении, возникающей как осложнение при интенсивной химио- и лучевой терапии опухолей.
Фармакологическое действие
Для стимуляции процесса гемопоэза назначают комплексное лечение, включающее в себя прием препаратов:
- двух- и трехвалентного железа, что позволяет предотвратить развитие анемии и повысить уровень гемоглобина;
- витаминов B12, Е, В2, В6, фолиевой и аскорбиновой кислоты, которые принимают активное участие в процессе кроветворения;
- анаболических стероидов – для улучшения кровенаполенности сосудов и оксигенации тканей;
- андрогенов, что способствуют усвоению кальция, повышению активности ферментов и активизации процессов тканевого дыхания;
- эритропоэтинов – как средства повышения уровня гемоглобина крови и улучшения подачи кислорода к клеткам организма больного.
Описание фармакологической группы
Препараты, которые относятся к гематотропным средствам, объединены в разные подгруппы, выделенные за принципом их воздействия на организм. Данная группа включает в себя стимуляторы гемопоэза, антикоагулянты, гемостатические препараты, плазмозаменители крови, средства, подавляющие процесс растворения тромбов, фибринолитики, антиагреганты, коагулянты и другие гематотропные препараты. Лекарственные средства этой фармакологической группы обеспечивают сохранение основных свойств крови, способствуют увеличению ее объема, укреплению сосудов, активному формированию количества и качества специализированных кровяных клеток (эритроцитов, тромбоцитов и лейкоцитов).
Лекарственные средства этой фармакологической группы обеспечивают сохранение основных свойств крови, способствуют увеличению ее объема, укреплению сосудов, активному формированию количества и качества специализированных кровяных клеток (эритроцитов, тромбоцитов и лейкоцитов).
Лечение Нарушения гемопоэза в Израиле
Содержание статьи:
1. Что такое гемопоэз
2. Причины нарушения гемопоэза
3. Стимуляторы гемопоэза
Клетки крови принимают участие во всех физиологических процессах, происходящих в организме. Чтобы они могли выполнять свои функции, система крови регулярно подвергается обновлению. Генетически заложено, что у каждого типа форменных элементов своя продолжительность существования. Так, у эритроцитов она составляет от 80 до 120 дней, а лейкоциты живут всего 6-10 дней. Затем старые элементы подвергаются разрушению, а на их место приходят новые, полноценные, которые образуются в результате гемопоэза.
Что такое гемопоэз
Гемопоэз (кроветворение) – физиологический процесс, в результате которого из клеток-предшественников образуются, размножаются и дифференцируются клетки крови. Он проходит в специфических условиях под строгим контролем регуляторных механизмов. Это гарантирует постоянство состава крови, и обеспечивает равновесие между отжившими клетками и новыми. Регуляцию гемопоэза осуществляют гормоны, витамины, прочие активные соединения.
Клетки крови образуются в костном мозге. Для гемопоэза организм использует плоские кости: грудина, ребра, тазовые и другие.
В норме в процессе гемопоэза клетки успешно проходят все стадии созревания и поступают в кровяное русло в строго определенном количественном и качественном эквиваленте. Благодаря этому кровь может в полной мере осуществлять многообразные, важные для жизни функции. Угнетение деятельности кроветворных органов, вызванное негативными факторами, их заболевания, повреждения неизбежно вызывают смещение равновесия в системе крови, что приводит к развитию патологических состояний.
Причины нарушения гемопоэза
Гемопоэз могут нарушить следующие факторы.
· Инфекции. Токсины, выделяемые инфекционными агентами, оказывают отрицательное действие на кроветворные органы. В результате гемопоэз нарушается, образование кровяных клеток замедляется.
· Дефицит витаминов, минеральных и других веществ. Погрешности в рационе или нарушение всасывания питательных веществ приводят к угнетению или патологическому изменению процесса созревания форменных элементов.
· Системные заболевания крови. Некоторые из них, например, лейкоз, способствуют выходу в кровяное русло неполноценных лейкоцитов.
· Яды. Такие ядовитые соединения, как, например, бензол, угнетают активность кроветворных органов.
· Радиация, рентгеновские лучи. Оказывают сильное повреждающее действие на органы кроветворения.
· Воспалительные процессы в организме. Провоцируют поступление в кровь незрелых клеток.
Провоцируют поступление в кровь незрелых клеток.
Угнетающее воздействие на систему кроветворения оказывают спиртные напитки, некоторые лекарственные препараты и многие другие факторы. Во всех случаях равновесие между новыми полноценными и разрушенными клетками смещается в сторону последних. Для восстановления гемопоэза в таких условиях используют стимуляторы кроветворения.
Стимуляторы гемопоэза
Стимуляторы кроветворения – фармакологические препараты, активные компоненты которых оказывают стимулирующее воздействие на костный мозг. Среди них различают стимуляторы эритропоэза и лейкопоэза. Первые способствуют увеличению в крови эритроцитов, насыщению их гемоглобином. Средства, стимулирующие лейкопоэз, используют при дефиците лейкоцитов, вызванном инфекциями, иммунодефицитом, онкологическими заболеваниями и прочими нарушениями. Все стимуляторы должны применяться по показаниям врача, использовать их для самолечения не рекомендуетсяВред от применения стимуляторов эритропоэза по незарегистрированным показаниям у людей в критических состояниях
Суть
Стимуляторы эритропоэза (СЭ) – это лекарства, которые стимулируют образование красных кровяных клеток. Их можно вводить внутривенно или подкожно. Они используются у людей в критических состояниях, несмотря на отсутствие соответствующих зарегистрированных показаний (т.е. «off-label»). Мы не смогли найти информацию о вреде, связанном с этими лекарствами; однако, согласно доказательствам низкого и умеренного качества, у них есть благоприятные эффекты в отношении вероятности смертельного исхода.
Их можно вводить внутривенно или подкожно. Они используются у людей в критических состояниях, несмотря на отсутствие соответствующих зарегистрированных показаний (т.е. «off-label»). Мы не смогли найти информацию о вреде, связанном с этими лекарствами; однако, согласно доказательствам низкого и умеренного качества, у них есть благоприятные эффекты в отношении вероятности смертельного исхода.
Актуальность
У людей в критических состояниях число красных кровяных клеток или уровень гемоглобина в крови часто снижены. В случае неэффективности профилактических мер переливание донорской крови является эффективным лечением, однако с ним сопряжены известные риски, такие как аллергические/иммунологические реакции, перегрузка объемом и передозировка электролитами, а также развитие инфекций. В качестве альтернативы для стимуляции образования собственных красных кровяных клеток могут применяться СЭ. Однако, при этом необходимо учитывать риск, связанный со СЭ, так как их применение у большинства людей в критических состояниях не одобрено регуляторными органами.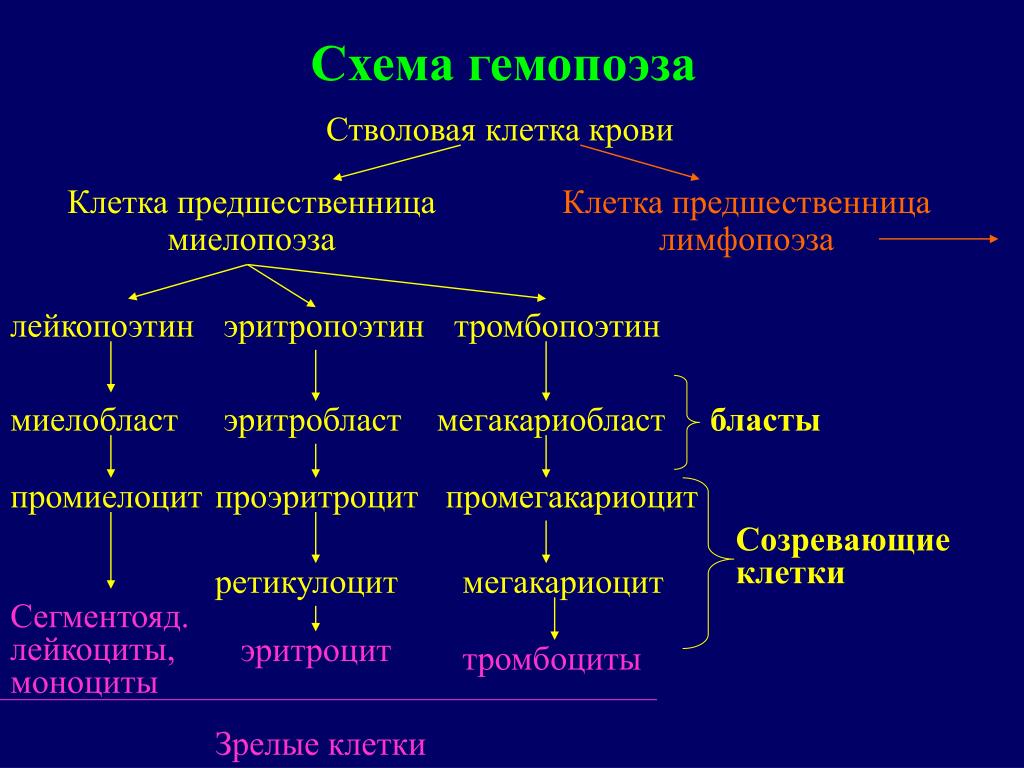
Характеристика исследований
Мы провели поиск исследований, в которых СЭ применяли для лечения людей в критических состояниях, в 10 базах данных. Доказательства актуальны на февраль 2017 года. Мы нашли 53 исследования с 945 240 участниками, получавшими эпоэтин-альфа, эпоэтин-бета, дарбэпоэтин-альфа или плацебо. Пять исследований ожидают классификации.
Основные результаты
Основываясь на доказательствах преимущественно низкого качества, мы не смогли исключить, что СЭ оказывают вред, связанный с их неблагоприятными эффектами. «Неблагоприятные эффекты» включали любые неблагоприятные события и проблемы, связанные с образованием тромбов в венах. Однако, мы обнаружили доказательства низкого качества в пользу защитного эффекта этих лекарств в отношении общего риска смерти у людей в критических состояниях.
препаратов, влияющие на гематопоэйс — Университет Джона Хопкинса
TY — CHAP
TY — CHAP
T1 — Препараты, влияющие на HematoPoiesis
AU — Aschenbrenner, Диана С.
PY — 2012/11/7
Y1 — 2012/11/7
N2 — • Иммунная система представляет собой сложную систему клеток и химических посредников, которая предотвращает проникновение в организм чужеродных патогенов или клеток. • Зрелые клетки крови различаются по структуре и функциям, но все они развиваются из общей клетки-предшественника, или стволовой клетки, внутри костного мозга.• Компоненты клеток крови могут быть изменены из-за патофизиологии или лекарственной терапии для лечения болезненного процесса. • Лекарства, которые стимулируют иммунную систему к производству клеток крови, являются гемопоэтическими факторами роста. Препараты, стимулирующие выработку эритроцитов, относятся к эритропоэтикам, препараты, вырабатывающие лейкоциты, — к колониестимулирующим факторам, а препараты, повышающие тромбоциты, включают особый интерлейкин. Эти препараты выполняют ту же функцию, что и их эндогенные аналоги. • Рекомбинантный человеческий эритропоэтин, также известный как эпоэтин альфа, используется для лечения анемий, возникающих в результате снижения образования эритроцитов (эритропоэз). Оксигенация тканей не может происходить оптимально при анемии. Анемия часто встречается при хронической болезни почек, при ХСН и после некоторых видов медикаментозной терапии. • Железо также необходимо для формирования эритроцитов. Терапия эпоэтином альфа, которая не эффективна или имеет ослабленный эффект, вероятно, связана с дефицитом железа, который может быть абсолютным или функциональным. Большинству пациентов, получающих терапию эпоэтином альфа, в какой-то момент требуется прием препаратов железа для образования эритроцитов. • К колониестимулирующим факторам относятся гранулоцитарные колониестимулирующие факторы (Г-КСФ) и гранулоцитарно-макрофагальные колониестимулирующие факторы (ГМ-КСФ).Они стимулируют выработку лейкоцитов. Нейтропения и другие виды подавления количества лейкоцитов часто возникают после химиотерапии и применения некоторых других типов лекарств. Низкое количество лейкоцитов, особенно низкое количество нейтрофилов, подвергает пациента повышенному риску заражения инфекцией.
Оксигенация тканей не может происходить оптимально при анемии. Анемия часто встречается при хронической болезни почек, при ХСН и после некоторых видов медикаментозной терапии. • Железо также необходимо для формирования эритроцитов. Терапия эпоэтином альфа, которая не эффективна или имеет ослабленный эффект, вероятно, связана с дефицитом железа, который может быть абсолютным или функциональным. Большинству пациентов, получающих терапию эпоэтином альфа, в какой-то момент требуется прием препаратов железа для образования эритроцитов. • К колониестимулирующим факторам относятся гранулоцитарные колониестимулирующие факторы (Г-КСФ) и гранулоцитарно-макрофагальные колониестимулирующие факторы (ГМ-КСФ).Они стимулируют выработку лейкоцитов. Нейтропения и другие виды подавления количества лейкоцитов часто возникают после химиотерапии и применения некоторых других типов лекарств. Низкое количество лейкоцитов, особенно низкое количество нейтрофилов, подвергает пациента повышенному риску заражения инфекцией. • В отличие от других интерлейкинов, интерлейкин-11 (опрелвекин) обладает гемопоэтическими свойствами и стимулирует выработку тромбоцитов. Без достаточного количества тромбоцитов не может иметь место надлежащее свертывание крови. Пациент подвержен риску чрезмерного кровотечения (внутреннего или внешнего).• Лекарства, стимулирующие выработку клеток крови, не следует назначать одновременно с химиотерапией, потому что быстро продуцирующиеся клетки, скорее всего, будут уничтожены медикаментозной терапией.
• В отличие от других интерлейкинов, интерлейкин-11 (опрелвекин) обладает гемопоэтическими свойствами и стимулирует выработку тромбоцитов. Без достаточного количества тромбоцитов не может иметь место надлежащее свертывание крови. Пациент подвержен риску чрезмерного кровотечения (внутреннего или внешнего).• Лекарства, стимулирующие выработку клеток крови, не следует назначать одновременно с химиотерапией, потому что быстро продуцирующиеся клетки, скорее всего, будут уничтожены медикаментозной терапией.
AB — • Иммунная система представляет собой сложную систему клеток и химических медиаторов, которая предотвращает проникновение в организм чужеродных патогенов или клеток. • Зрелые клетки крови различаются по структуре и функциям, но все они развиваются из общей клетки-предшественника, или стволовой клетки, внутри костного мозга. • Компоненты клеток крови могут быть изменены из-за патофизиологии или лекарственной терапии для лечения болезненного процесса.• Лекарства, которые стимулируют иммунную систему к производству клеток крови, являются гемопоэтическими факторами роста. Препараты, стимулирующие выработку эритроцитов, относятся к эритропоэтикам, препараты, вырабатывающие лейкоциты, — к колониестимулирующим факторам, а препараты, повышающие тромбоциты, включают особый интерлейкин. Эти препараты выполняют ту же функцию, что и их эндогенные аналоги. • Рекомбинантный человеческий эритропоэтин, также известный как эпоэтин альфа, используется для лечения анемий, возникающих в результате снижения образования эритроцитов (эритропоэз).Оксигенация тканей не может происходить оптимально при анемии. Анемия часто встречается при хронической болезни почек, при ХСН и после некоторых видов медикаментозной терапии. • Железо также необходимо для формирования эритроцитов. Терапия эпоэтином альфа, которая не эффективна или имеет ослабленный эффект, вероятно, связана с дефицитом железа, который может быть абсолютным или функциональным. Большинству пациентов, получающих терапию эпоэтином альфа, в какой-то момент требуется прием препаратов железа для образования эритроцитов.
Препараты, стимулирующие выработку эритроцитов, относятся к эритропоэтикам, препараты, вырабатывающие лейкоциты, — к колониестимулирующим факторам, а препараты, повышающие тромбоциты, включают особый интерлейкин. Эти препараты выполняют ту же функцию, что и их эндогенные аналоги. • Рекомбинантный человеческий эритропоэтин, также известный как эпоэтин альфа, используется для лечения анемий, возникающих в результате снижения образования эритроцитов (эритропоэз).Оксигенация тканей не может происходить оптимально при анемии. Анемия часто встречается при хронической болезни почек, при ХСН и после некоторых видов медикаментозной терапии. • Железо также необходимо для формирования эритроцитов. Терапия эпоэтином альфа, которая не эффективна или имеет ослабленный эффект, вероятно, связана с дефицитом железа, который может быть абсолютным или функциональным. Большинству пациентов, получающих терапию эпоэтином альфа, в какой-то момент требуется прием препаратов железа для образования эритроцитов. • К колониестимулирующим факторам относятся гранулоцитарные колониестимулирующие факторы (Г-КСФ) и гранулоцитарно-макрофагальные колониестимулирующие факторы (ГМ-КСФ).Они стимулируют выработку лейкоцитов. Нейтропения и другие виды подавления количества лейкоцитов часто возникают после химиотерапии и применения некоторых других типов лекарств. Низкое количество лейкоцитов, особенно низкое количество нейтрофилов, подвергает пациента повышенному риску заражения инфекцией. • В отличие от других интерлейкинов, интерлейкин-11 (опрелвекин) обладает гемопоэтическими свойствами и стимулирует выработку тромбоцитов. Без достаточного количества тромбоцитов не может иметь место надлежащее свертывание крови. Пациент подвержен риску чрезмерного кровотечения (внутреннего или внешнего).• Лекарства, стимулирующие выработку клеток крови, не следует назначать одновременно с химиотерапией, потому что быстро продуцирующиеся клетки, скорее всего, будут уничтожены медикаментозной терапией.
• К колониестимулирующим факторам относятся гранулоцитарные колониестимулирующие факторы (Г-КСФ) и гранулоцитарно-макрофагальные колониестимулирующие факторы (ГМ-КСФ).Они стимулируют выработку лейкоцитов. Нейтропения и другие виды подавления количества лейкоцитов часто возникают после химиотерапии и применения некоторых других типов лекарств. Низкое количество лейкоцитов, особенно низкое количество нейтрофилов, подвергает пациента повышенному риску заражения инфекцией. • В отличие от других интерлейкинов, интерлейкин-11 (опрелвекин) обладает гемопоэтическими свойствами и стимулирует выработку тромбоцитов. Без достаточного количества тромбоцитов не может иметь место надлежащее свертывание крови. Пациент подвержен риску чрезмерного кровотечения (внутреннего или внешнего).• Лекарства, стимулирующие выработку клеток крови, не следует назначать одновременно с химиотерапией, потому что быстро продуцирующиеся клетки, скорее всего, будут уничтожены медикаментозной терапией.
UR – http://www. scopus.com/inward/record.url?scp=84971299782&partnerID=8YFLogxK
scopus.com/inward/record.url?scp=84971299782&partnerID=8YFLogxK
UR – http://www.scopus.com/inward/citedby.url?scp=84971299782&partnerID=8YFLogxK
м3 — Глава
AN — Scopus: 84971299782
99782
SN — 9781451187663
SP — 672
EP — 692
BT — 690
BT — лекарственная терапия в кормяте
PB — Wolders Kluwer Health Adis (ESP)
ER
Гемопоэтические факторы роста | Препараты, безрецептурные препараты и травы
О компании Medscape Drugs & Diseases
Клинический справочникMedscape — это наиболее авторитетный и доступный медицинский справочник для врачей и медицинских работников, доступный в Интернете и на всех основных мобильных устройствах.Весь контент бесплатный.
Клиническая информация представляет собой опыт и практические знания ведущих врачей и фармацевтов из ведущих академических медицинских центров США и всего мира.
Предоставленные темы являются всеобъемлющими и охватывают более 30 медицинских специальностей, включая:
Болезни и состояния Более 6000 научно обоснованных и проверенных врачами статей о заболеваниях и состояниях организованы таким образом, чтобы быстро и всесторонне отвечать на клинические вопросы и предоставлять подробную информацию в поддержку диагностики, лечения и принятия других клинических решений. Темы богато иллюстрированы более чем 40 000 клинических фотографий, видео, диаграмм и рентгенографических изображений.
Темы богато иллюстрированы более чем 40 000 клинических фотографий, видео, диаграмм и рентгенографических изображений.
Более 1000 статей о клинических процедурах содержат четкие пошаговые инструкции и содержат обучающие видеоролики и изображения, которые позволяют врачам освоить новейшие методы или улучшить свои навыки в процедурах, которые они выполняли ранее.
АнатомияБолее 100 статей по анатомии содержат клинические изображения и диаграммы основных систем и органов человеческого тела.Статьи помогают понять анатомию, связанную с лечением конкретных состояний и выполнением процедур. Они также могут способствовать обсуждению между врачом и пациентом.
Монографии по лекарствамБолее 7100 монографий предоставлено для рецептурных и безрецептурных препаратов, а также для соответствующих фирменных препаратов, трав и пищевых добавок. Изображения наркотиков также включены.
Средство проверки лекарственного взаимодействия Наша программа проверки взаимодействий с лекарственными средствами обеспечивает быстрый доступ к десяткам тысяч взаимодействий между брендовыми и непатентованными препаратами, отпускаемыми без рецепта препаратами и добавками. Проверьте от легких взаимодействий до серьезных противопоказаний до 30 лекарств, трав и добавок одновременно.
Проверьте от легких взаимодействий до серьезных противопоказаний до 30 лекарств, трав и добавок одновременно.
Получите доступ к информации о лекарственном формуляре плана медицинского страхования при поиске конкретного лекарства и сэкономьте время и усилия для себя и своего пациента. Выберите из нашего полного списка из более чем 1800 планов страхования во всех 50 штатах США. Настройте свою учетную запись Medscape с помощью планов медицинского обслуживания, которые вы принимаете, чтобы необходимая информация сохранялась и была готова каждый раз, когда вы ищете лекарство на нашем сайте или в приложении Medscape.Легко сравнивайте статус препаратов одного класса при выборе альтернативного препарата для вашего пациента.
Медицинские калькуляторы Medscape Reference содержит 129 медицинских калькуляторов, охватывающих формулы, шкалы и классификации. Кроме того, более 600 монографий по лекарствам в нашем справочнике включают встроенные калькуляторы дозирования.
Сотни презентаций в виде слайд-шоу с богатыми изображениями визуально привлекают и бросают вызов читателям, расширяя их знания как о распространенных, так и о необычных болезнях, презентациях клинических случаев и текущих противоречиях в медицине.
МЕДЛАЙННажмите на цитаты по темам, связанным с лекарствами и болезнями, в нашем клиническом справочнике, чтобы ознакомиться с клиническими данными в MEDLINE. Кроме того, поищите журнальные статьи в базе данных MEDLINE.
Medscape — ведущее онлайн-направление для медицинских работников, которым нужна клиническая информация. В дополнение к клиническим эталонным инструментам Medscape предлагает:
Медицинские новости Узнать большеНепрерывное медицинское образование Узнать больше
Потребностно-адаптированная регуляция раннего кроветворения при инфекции и воспалении | Кровь
В последние десятилетия стало ясно, что ранняя система кроветворения при БМ в основном задействована для создания соответствующего гемато-иммунного ответа на системную инфекцию и воспаление.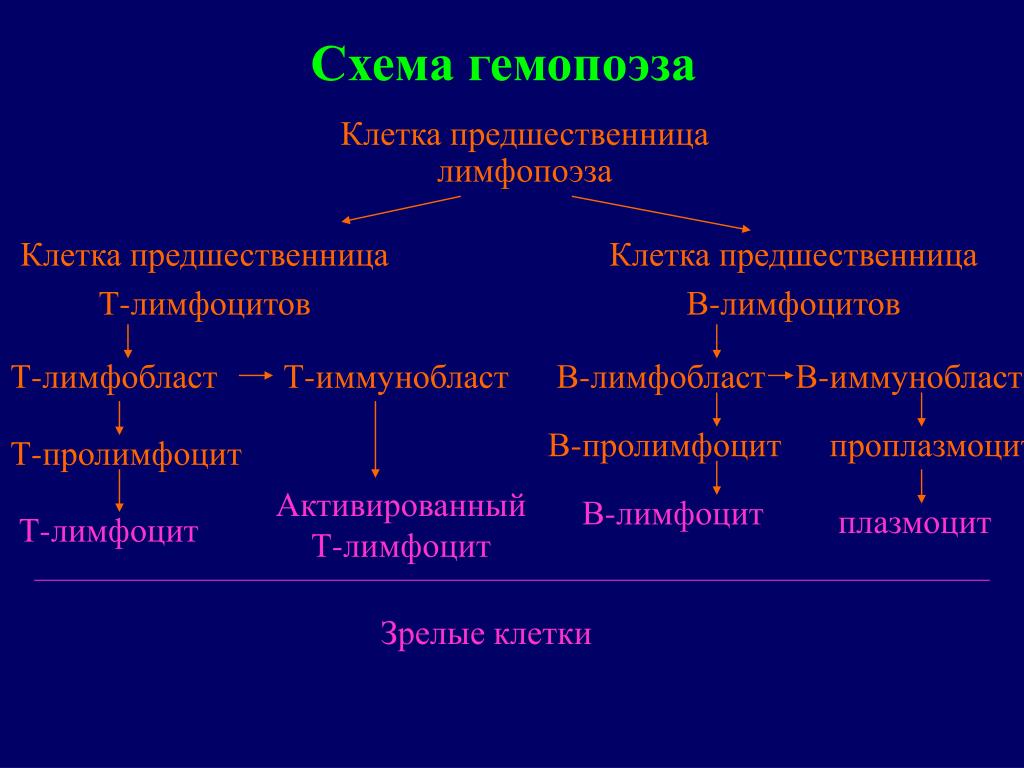 Этот процесс включает в себя прямое и косвенное обучение гемопоэтических клеток цитокинами, хемокинами и консервативными паттернами инфекции, что приводит к адаптированному образованию гемопоэтических клеток и направленной миграции нуждающихся клеток. Относительный вес специфических воздействий на рецепторы-мишени в различных инфекционных и воспалительных ситуациях все еще должен быть проанализирован экспериментальными системами с усилением и утратой функции специфического гена и клиническими наблюдениями.
Этот процесс включает в себя прямое и косвенное обучение гемопоэтических клеток цитокинами, хемокинами и консервативными паттернами инфекции, что приводит к адаптированному образованию гемопоэтических клеток и направленной миграции нуждающихся клеток. Относительный вес специфических воздействий на рецепторы-мишени в различных инфекционных и воспалительных ситуациях все еще должен быть проанализирован экспериментальными системами с усилением и утратой функции специфического гена и клиническими наблюдениями.
Изучение природы, однако, уже привело к рутинному клиническому использованию цитокинов, таких как G-CSF и GM-CSF, для усиления регенерации миелоидных клеток, 56 агонистов тромбопоэтина для образования тромбоцитов, 118 и антагонистов CXCR4 для мобилизации HSPC. 119 Ожидается, что за этим последуют другие, и можно предположить, что селективная доставка агонистов PRR также может быть терапевтической возможностью для усиления или защиты регенерации гемопоэтических клеток в определенных ситуациях. Хотя механистические детали не разобраны, недавно была предложена полезная роль агониста TLR5 в регенерации кишечника и гемопоэза после облучения. 120 Кроме того, естественно развившиеся ранние механизмы активации системы кроветворения могут быть «захвачены» терапевтически для воздействия на злокачественные новообразования кроветворной системы.Покойные клетки, инициирующие хронический миелоидный лейкоз, а также здоровые HSC могут быть привлечены к циклированию при лечении IFN-α. 30 После этого путем селективного нацеливания могут быть элиминированы только клетки хронического миелоидного лейкоза, несущие слитые клетки BCR-ABL1 и зависимые от тирозинкиназы, но не здоровые HSC. Хотя это и не доказано напрямую, недавнее клиническое исследование предполагает, что это действительно может иметь место. 121 Более того, можно предположить, что мобилизация лейкозных клеток и здоровых гемопоэтических клеток из костного мозга и расширенный доступ к этим клеткам затем помогут относительно специфически нацеливаться на больные клетки, которые в противном случае могли бы быть защищены их нишами в костном мозге.
Хотя механистические детали не разобраны, недавно была предложена полезная роль агониста TLR5 в регенерации кишечника и гемопоэза после облучения. 120 Кроме того, естественно развившиеся ранние механизмы активации системы кроветворения могут быть «захвачены» терапевтически для воздействия на злокачественные новообразования кроветворной системы.Покойные клетки, инициирующие хронический миелоидный лейкоз, а также здоровые HSC могут быть привлечены к циклированию при лечении IFN-α. 30 После этого путем селективного нацеливания могут быть элиминированы только клетки хронического миелоидного лейкоза, несущие слитые клетки BCR-ABL1 и зависимые от тирозинкиназы, но не здоровые HSC. Хотя это и не доказано напрямую, недавнее клиническое исследование предполагает, что это действительно может иметь место. 121 Более того, можно предположить, что мобилизация лейкозных клеток и здоровых гемопоэтических клеток из костного мозга и расширенный доступ к этим клеткам затем помогут относительно специфически нацеливаться на больные клетки, которые в противном случае могли бы быть защищены их нишами в костном мозге. Проводятся первые соответствующие исследования с использованием антагонистов CXCR4. Наконец, необходимо определить, экспрессируются ли некоторые PRR или даже избыточно экспрессируются при некоторых ранних гематопоэтических злокачественных новообразованиях, и если да, то могут ли они стать мишенями для будущей терапии. 116,117,122,123 Кроме того, хотя терапевтическая активация раннего гемопоэза уже используется в клинических условиях, до сих пор не установлено, будет ли терапевтическое прерывание активирующих сигналов иметь клиническую пользу.Это можно предположить в условиях хронической ранней стимуляции кроветворения, вызванной инфекцией и воспалением. Хотя в этом обзоре мы фокусируемся на последствиях взаимодействия патоген-хозяин для раннего кроветворения, аналогичные механизмы и каскады запускаются при различных патологических состояниях, не требующих вторжения патогена. В этом отношении так называемые опасные молекулярные паттерны хозяина и аларминины, высвобождаемые при травматических, сосудистых, метаболических или токсических повреждениях или даже во время естественного старения или восстановления тканей, распознаются как эндогенные лиганды PRR или другими рецепторами и вызывают ранние гемопоэтические процессы.
Проводятся первые соответствующие исследования с использованием антагонистов CXCR4. Наконец, необходимо определить, экспрессируются ли некоторые PRR или даже избыточно экспрессируются при некоторых ранних гематопоэтических злокачественных новообразованиях, и если да, то могут ли они стать мишенями для будущей терапии. 116,117,122,123 Кроме того, хотя терапевтическая активация раннего гемопоэза уже используется в клинических условиях, до сих пор не установлено, будет ли терапевтическое прерывание активирующих сигналов иметь клиническую пользу.Это можно предположить в условиях хронической ранней стимуляции кроветворения, вызванной инфекцией и воспалением. Хотя в этом обзоре мы фокусируемся на последствиях взаимодействия патоген-хозяин для раннего кроветворения, аналогичные механизмы и каскады запускаются при различных патологических состояниях, не требующих вторжения патогена. В этом отношении так называемые опасные молекулярные паттерны хозяина и аларминины, высвобождаемые при травматических, сосудистых, метаболических или токсических повреждениях или даже во время естественного старения или восстановления тканей, распознаются как эндогенные лиганды PRR или другими рецепторами и вызывают ранние гемопоэтические процессы. реакции, вероятно, с такими же краткосрочными и долгосрочными последствиями, как микробные инфекции. 5,124-126
реакции, вероятно, с такими же краткосрочными и долгосрочными последствиями, как микробные инфекции. 5,124-126
Мы убеждены, что дальнейшие исследования разносторонней реакции гемопоэтической системы, адаптированной к потребностям, не только предоставят новые базовые идеи и терапевтические возможности для гематологов, онкологов, иммунологов и специалистов по инфекционным заболеваниям, но, вероятно, также проинструктируют о принципиальных механизмах гомеостаза и регенерация при инфекции и воспалении в других системах органов, поддерживаемых стволовыми клетками, таких как кожа, кишечник и мозг.
Электронная версия этой статьи содержит дополнение данных.
Воздействие кокаина нарушает многолинейный гемопоэз человеческих гемопоэтических клеток-предшественников, опосредованный рецептором сигма-1
Ганапати, В. Наркотики и плацента человека. Life Sci 88, 926–930 (2011).
Life Sci 88, 926–930 (2011).
КАС Статья пабмед Google Scholar
Беллоне, К., Mameli, M. & Luscher, C. Воздействие кокаина в утробе матери задерживает постнатальное синаптическое созревание глутаматергической передачи в VTA. Nat Neurosci 14, 1439–1446 (2011).
КАС Статья пабмед Google Scholar
Benveniste, H. et al. Кокаин фармакологически активен в мозге плода приматов. Proc Natl Acad Sci U S A 107, 1582–1587 (2010).
КАС Статья ОБЪЯВЛЕНИЯ пабмед ПабМед Центральный Google Scholar
Мейер, К.Д. и Чжан Л. Краткосрочные и долгосрочные побочные эффекты злоупотребления кокаином во время беременности на развитие сердца. Ther Adv Cardiovasc Dis 3, 7–16 (2009).
Артикул пабмед ПабМед Центральный Google Scholar
Бенке, М. и Смит, В. К. Пренатальное злоупотребление психоактивными веществами: краткосрочные и долгосрочные последствия для подвергшегося воздействию плода. Педиатрия 131, e1009-1024 (2013).
и Смит, В. К. Пренатальное злоупотребление психоактивными веществами: краткосрочные и долгосрочные последствия для подвергшегося воздействию плода. Педиатрия 131, e1009-1024 (2013).
Артикул пабмед Google Scholar
Чен В.A. & Maier, S.E. Комбинированное употребление наркотиков и риск повреждения плода. Алкоголь Res Health 34, 27-28 (2011).
ПабМед ПабМед Центральный Google Scholar
Mayes, L.C., Granger, R.H., Frank, M.A., Schottenfeld, R. & Bornstein, MH. Нейроповеденческие профили новорожденных, подвергавшихся пренатальному воздействию кокаина. Педиатрия 91, 778-783 (1993).
КАС пабмед Google Scholar
Руссотт, Ф., Содерберг, Л. и Соуэлл, Э. Структурные, метаболические и функциональные нарушения мозга в результате пренатального воздействия наркотиков: данные нейровизуализации. Neuropsychol Rev 20, 376–397 (2010).
Neuropsychol Rev 20, 376–397 (2010).
Артикул пабмед ПабМед Центральный Google Scholar
Мессия, С. Э., Миллер, Т. Л., Липшульц, С. Э. и Бандстра, Э. С. Потенциальные скрытые эффекты пренатального воздействия кокаина на рост и риск сердечно-сосудистых и метаболических заболеваний в детстве.Prog Pediatr Cardiol 31, 59–65 (2011).
Артикул пабмед ПабМед Центральный Google Scholar
Eyler, FD, Behnke, M., Conlon, M., Woods, NS & Wobie, K. Исход родов по результатам проспективного, согласованного исследования пренатального употребления крэка/кокаина: I. Интерактивное и дозовое воздействие на здоровье и рост. Педиатрия 101, 229-237 (1998).
КАС Статья пабмед Google Scholar
Бауэр, К.Р. и др. Острые неонатальные последствия воздействия кокаина во время беременности. Arch Pediatr Adolesc Med 159, 824–834 (2005).
Артикул пабмед Google Scholar
Ричардсон, Г. А. Пренатальное воздействие кокаина. Лонгитюдное исследование развития. Ann NY Acad Sci 846, 144–152 (1998).
КАС Статья ОБЪЯВЛЕНИЯ пабмед Google Scholar
Мантри, К.К., Пандхэр Дэш, Дж., Мантри, Дж.В. и Дэш, К.С. Кокаин усиливает репликацию ВИЧ-1 в CD4 + Т-клетках, подавляя миР-125b. PLoS One 7, e51387 (2012 г.).
КАС Статья ОБЪЯВЛЕНИЯ пабмед ПабМед Центральный Google Scholar
Pandhare, J. et al. Кокаин усиливает индуцированный ВИЧ-1 апоптоз CD4(+) Т-клеток: влияние на прогрессирование заболевания у пациентов с ВИЧ-1, злоупотребляющих кокаином. Ам Дж. Патол 184, 927–936 (2014).
КАС Статья пабмед ПабМед Центральный Google Scholar
Пеллегрино, Т. и Байер, Б.М. Влияние кокаина in vivo на функцию иммунных клеток. J Нейроиммунол 83, 139-147 (1998).
и Байер, Б.М. Влияние кокаина in vivo на функцию иммунных клеток. J Нейроиммунол 83, 139-147 (1998).
КАС Статья пабмед Google Scholar
Перейра, Дж. и др. Активация тромбоцитов у хронических потребителей кокаина: эффект кратковременного воздержания. Тромбоциты 22, 596-601 (2011).
КАС Статья пабмед Google Scholar
Риос-Оливарес, Э.и другие. Нарушение продукции цитокинов и подавление активности пролиферации лимфоцитов у инфицированных ВГС потребителей кокаина и героина («спидбол»). Наркотики и алкоголь зависят 85, 236-243 (2006).
КАС Статья пабмед Google Scholar
Weber, J. E. et al. Влияние употребления кокаина на эритропоэз, опосредованный костным мозгом. Acad Emerg Med 10, 705–708 (2003).
Артикул пабмед Google Scholar
Кумп Д. Ф., Станулис, Э.Д., Холсаппл, М.П., Конрад, Д.Х. и Роузкранс, Дж.А. Высвобождение кортикостерона, индуцированное кокаином, опосредует различные эффекты на ответы клеток Т-хелпер1 и Т-хелпер2. Adv Exp Med Biol 437, 189-198 (1998).
Ф., Станулис, Э.Д., Холсаппл, М.П., Конрад, Д.Х. и Роузкранс, Дж.А. Высвобождение кортикостерона, индуцированное кокаином, опосредует различные эффекты на ответы клеток Т-хелпер1 и Т-хелпер2. Adv Exp Med Biol 437, 189-198 (1998).
КАС Статья пабмед Google Scholar
Bayer, B.M., Hernandez, M.C. & Ding, XZ. Толерантность и перекрестная толерантность к подавляющему действию кокаина и морфина на пролиферацию лимфоцитов.Pharmacol Biochem Behav 53, 227-234 (1996).
КАС Статья пабмед Google Scholar
Куррич, С. и др. Динамическое взаимодействие между рецептором сигма-1 и Kv1.2 формирует нейрональные и поведенческие реакции на кокаин. Ячейка 152, 236–247 (2013).
КАС Статья пабмед ПабМед Центральный Google Scholar
Kim, S.G. et al. Воздействие кокаина повышает восприимчивость покоящихся Т-клеток к ВИЧ-инфекции. J Leukoc Biol 94, 835-843 (2013).
J Leukoc Biol 94, 835-843 (2013).
КАС Статья пабмед ПабМед Центральный Google Scholar
Морис, Т. и Су, Т. П. Фармакология рецепторов сигма-1. Pharmacol Ther 124, 195-206 (2009).
КАС Статья пабмед ПабМед Центральный Google Scholar
Нараянан С., Месанжо С., Пуперт Дж. Х. и Маккарди С. Р. Сигма-рецепторы и злоупотребление кокаином.Curr Top Med Chem 11, 1128–1150 (2011).
КАС Статья пабмед Google Scholar
Наварро, Г. и др. Прямое участие рецепторов сигма-1 в опосредованных дофаминовыми рецепторами D1 эффектах кокаина. Proc Natl Acad Sci U S A 107, 18676–18681 (2010).
КАС Статья ОБЪЯВЛЕНИЯ пабмед ПабМед Центральный Google Scholar
Рот, доктор медицины, Whittaker, K.M., Choi, R. , Tashkin, D.P. & Baldwin, G.C. Кокаиновые и сигма-1 рецепторы модулируют ВИЧ-инфекцию, хемокиновые рецепторы и ось HPA в модели huPBL-SCID. J Leukoc Biol 78, 1198-1203 (2005).
, Tashkin, D.P. & Baldwin, G.C. Кокаиновые и сигма-1 рецепторы модулируют ВИЧ-инфекцию, хемокиновые рецепторы и ось HPA в модели huPBL-SCID. J Leukoc Biol 78, 1198-1203 (2005).
КАС Статья пабмед Google Scholar
Тиан, М. и др. Изменение гемопоэза, поведения и сексуальной функции у мышей с дефицитом мю-опиоидных рецепторов. J Exp Med 185, 1517–1522 (1997).
КАС Статья пабмед ПабМед Центральный Google Scholar
Лекарственные гематологические синдромы
Цель .Лекарства могут вызывать почти весь спектр гематологических нарушений, поражая лейкоциты, эритроциты, тромбоциты и систему свертывания крови. Эта статья направлена на то, чтобы подчеркнуть широкий спектр гематологических синдромов, вызванных лекарствами, и выделить некоторые из новых лекарств и синдромов. Методы . Был проведен обзор литературы Medline по гематологическим синдромам, индуцированным лекарствами. Большинство отчетов и обзоров посвящены отдельным препаратам или цитопениям. Результаты . Медикаментозные синдромы включают гемолитическую анемию, метгемоглобинемию, эритроцитарную аплазию, сидеробластную анемию, мегалобластную анемию, полицитемию, апластическую анемию, лейкоцитоз, нейтропению, эозинофилию, иммунную тромбоцитопению, микроангиопатические синдромы, гиперкоагуляцию, гипопротромбинемию, циркулирующие антикоагулянты, миелодисплазию и острый лейкоз.Некоторые из классических препаратов, которые, как известно, вызывают гематологические нарушения, были заменены более новыми препаратами, в том числе биопрепаратами, сопровождающимися их собственными синдромами и непреднамеренными побочными эффектами. Выводы . Лекарства могут вызывать токсичность, охватывающую многие гематологические синдромы, опосредованные различными механизмами. Врачи должны быть готовы к возможности ятрогенных гематологических осложнений, вызванных лекарственными препаратами.
Большинство отчетов и обзоров посвящены отдельным препаратам или цитопениям. Результаты . Медикаментозные синдромы включают гемолитическую анемию, метгемоглобинемию, эритроцитарную аплазию, сидеробластную анемию, мегалобластную анемию, полицитемию, апластическую анемию, лейкоцитоз, нейтропению, эозинофилию, иммунную тромбоцитопению, микроангиопатические синдромы, гиперкоагуляцию, гипопротромбинемию, циркулирующие антикоагулянты, миелодисплазию и острый лейкоз.Некоторые из классических препаратов, которые, как известно, вызывают гематологические нарушения, были заменены более новыми препаратами, в том числе биопрепаратами, сопровождающимися их собственными синдромами и непреднамеренными побочными эффектами. Выводы . Лекарства могут вызывать токсичность, охватывающую многие гематологические синдромы, опосредованные различными механизмами. Врачи должны быть готовы к возможности ятрогенных гематологических осложнений, вызванных лекарственными препаратами.
1. Введение
Гематологические расстройства возникают по различным механизмам и этиологии.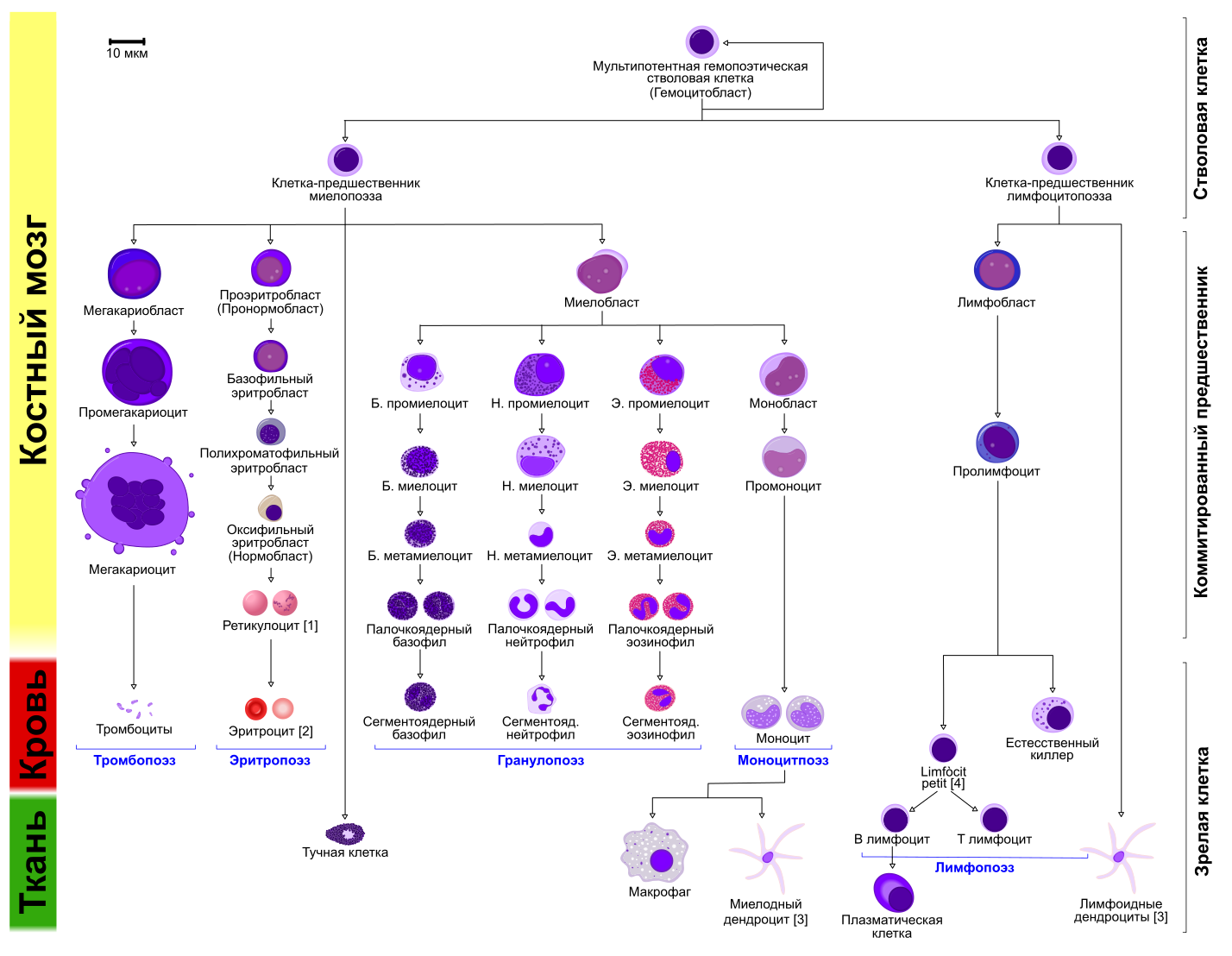 Лекарственные гематологические расстройства могут охватывать почти весь спектр гематологии, поражая эритроциты, лейкоциты, тромбоциты и систему свертывания крови. Самые последние обзоры гематологических нарушений, вызванных лекарственными препаратами, были сосредоточены на конкретных лекарствах или цитопениях. Цель этого обзора состоит в том, чтобы подчеркнуть широкий спектр гематологических синдромов, вызванных лекарствами, и выделить некоторые из новых описанных лекарств и синдромов. Однако из-за ограничений по объему этот обзор не претендует на полноту всех гематологических дискразий, вызванных лекарственными препаратами.
Лекарственные гематологические расстройства могут охватывать почти весь спектр гематологии, поражая эритроциты, лейкоциты, тромбоциты и систему свертывания крови. Самые последние обзоры гематологических нарушений, вызванных лекарственными препаратами, были сосредоточены на конкретных лекарствах или цитопениях. Цель этого обзора состоит в том, чтобы подчеркнуть широкий спектр гематологических синдромов, вызванных лекарствами, и выделить некоторые из новых описанных лекарств и синдромов. Однако из-за ограничений по объему этот обзор не претендует на полноту всех гематологических дискразий, вызванных лекарственными препаратами.
2. Иммунная гемолитическая анемия
Иммунная гемолитическая анемия (ИГА) характеризуется разрушением эритроцитов антителами, действующими против антигенов на мембране эритроцитов. Опосредованная антителами IgG или IgM, IHA может быть идиопатической или вторичной по отношению к инфекциям, аутоиммунным заболеваниям, лимфопролиферативным заболеваниям или лекарственным препаратам. У больных отмечаются анемия, ретикулоцитоз, непрямая гипербилирубинемия, повышенный уровень ЛДГ при положительной пробе Кумбса.
У больных отмечаются анемия, ретикулоцитоз, непрямая гипербилирубинемия, повышенный уровень ЛДГ при положительной пробе Кумбса.
Лекарственно-индуцированная ИГА может быть связана как с лекарственно-зависимыми, так и с лекарственно-независимыми антителами [1].Другие препараты могут вызывать неиммунологическую адсорбцию белка на эритроцитах, обработанных лекарствами. С независимыми от лекарств аутоантителами, типичным примером которых является альфа-метил ДОФА, IHA может сохраняться в течение длительного времени даже после отмены препарата. IHA описана при применении цефалоспоринов, нестероидных противовоспалительных средств, левахина, оксалиплатина и тейкопланина, среди прочих [1, 2].
Внутривенный Rh (D) иммуноглобулин, используемый для лечения иммунной тромбоцитопенической пурпуры у неспленэктомированных Rh (D)-положительных пациентов, преднамеренно вызывает легкий гемолиз, что, вероятно, объясняет его механизм действия.Однако в небольшом числе случаев сообщалось о тяжелом гемолизе с почечной недостаточностью, синдромом диссеминированного внутрисосудистого свертывания крови и летальным исходом [3].
Сообщалось, что флударабин, химиотерапевтический агент на основе пуриновых нуклеозидов, вызывает или усугубляет аутоиммунную гемолитическую анемию, связанную с хроническим лимфоцитарным лейкозом. Однако сочетание флударабина с ритуксимабом и циклофосфамидом может снизить этот риск [4].
3. Неиммунные гемолитические анемии
Дефицит G6PD является наиболее частой энзимопатией эритроцитов, связанной с гемолизом.Гемолиз может быть спровоцирован инфекцией, фасолью и лекарствами. Чувствительность к различным препаратам зависит от наследственной мутации и связанной с ней степени дефицита. В большинстве случаев медикаментозный гемолиз проходит самостоятельно. Дефицит сцеплен с Х-хромосомой, поэтому чаще и тяжелее проявляется у мужчин. Примахин, феназопиридин, нитрофурантоин и некоторые сульфаты связаны с гемолизом [5].
Рибавирин, используемый с пегинтерфероном для лечения гепатита С, вызывает анемию.Рибавирин концентрируется в эритроцитах, истощает запасы АТФ и способствует гемолизу за счет окислительного повреждения мембран. Хотя анемия улучшится при прекращении приема рибавирина или снижении его дозы, такие стратегии могут поставить под угрозу эффективность противовирусной терапии. Сообщалось, что эритропоэтин помогает уменьшить анемию [6].
Хотя анемия улучшится при прекращении приема рибавирина или снижении его дозы, такие стратегии могут поставить под угрозу эффективность противовирусной терапии. Сообщалось, что эритропоэтин помогает уменьшить анемию [6].
4. Метгемоглобинемия
Приблизительно 3% гемоглобина организма двухвалентное железо в геме окисляется при дезоксигенации с образованием метгемоглобина.Большая часть этого встречающегося в природе метгемоглобина восстанавливается до гемоглобина с помощью ферментной системы метгемоглобинредуктазы. Метгемоглобинемия, характеризующаяся избыточной продукцией метгемоглобина, вызывает нарушение транспорта кислорода. Метгемоглобинемия может быть врожденной (вследствие дефектов ферментативного восстановления гемоглобина) или приобретенной. У пациентов появляются симптомы аноксии, цианоза, снижения насыщения кислородом и шоколадно-коричневого цвета артериальной крови. Подтверждение диагноза производится измерением метгемоглобина в пробе газов артериальной крови.
Препараты, вызывающие метгемоглобинемию, либо непосредственно окисляют гемоглобин, либо метаболически активируются до окисляющих соединений [7]. Феназопиридин, применяемый для купирования цистита, может вызывать окислительный гемолиз [8]. Дапсон, используемый при проказе, герпетиформном дерматите и для профилактики пневмоцистной карины, метаболизируется до производного гидроксиламина [9]. Это была наиболее частая причина метгемоглобинемии в одном недавнем исследовании [10]. Примахин и местные анестетики, такие как местный или аэрозольный бензокаин (используемый перед эндоскопическими процедурами верхних отделов) и прилокаин, могут вызывать метгемоглобинемию [11–13].Также были замешаны амилнитрит и изобутилнитрит [7]. Лечение включает прекращение введения индуцирующего агента, кислорода и метиленового синего.
5. Мегалобластная анемия
Мегалобластные анемии характеризуются наличием гиперклеточного костного мозга с крупными аномальными гемопоэтическими клетками-предшественниками (мегалобластами). Также наблюдаются лейкопения и тромбоцитопения. Мегалобластные анемии могут быть врожденными или приобретенными и чаще всего связаны с дефицитом витаминов (кобаламина) и фолиевой кислоты.Хотя они обычно являются результатом недоедания или неправильного всасывания, они также могут быть вызваны лекарственными препаратами.
Также наблюдаются лейкопения и тромбоцитопения. Мегалобластные анемии могут быть врожденными или приобретенными и чаще всего связаны с дефицитом витаминов (кобаламина) и фолиевой кислоты.Хотя они обычно являются результатом недоедания или неправильного всасывания, они также могут быть вызваны лекарственными препаратами.
Лекарственные препараты, препятствующие синтезу ДНК, такие как антиметаболиты и алкилирующие агенты, некоторые антинуклеозиды, применяемые против ВИЧ и других вирусов [14], могут вызывать мегалобластную анемию. Триметоприм (в высоких, увеличенных дозах) и пириметамин, которые связываются с бактериями с большим сродством, чем человеческая дигидрофолатредуктаза, были связаны с мегалобластной анемией, в первую очередь у пациентов, уже подверженных риску дефицита фолиевой кислоты.Антибиотики, такие как сульфасалазин, и противосудорожные средства, такие как фенитоин, связаны с изменениями, связанными с фолиевой кислотой, которые вызывают мегалобластную анемию, возможно, связанную с нарушением всасывания.
Сообщалось о снижении уровня кобаламина при длительном применении антагонистов гистаминовых рецепторов 2 и ингибиторов протонной помпы (например, омепразола) [15, 16]. В то время как абсорбция B 12 , связанная с белком, может быть нарушена этими агентами, клинически значимый дефицит кажется редким, несмотря на широкое использование.
6. Сидеробластная анемия
Сидеробластные анемии (СА) характеризуются кольцевидными сидеробластами (эритробластами, содержащими железоположительные гранулы, расположенные вокруг ядра) в костном мозге. Сидеробластные анемии, которые могут быть наследственными или приобретенными, проявляются нарушением биосинтеза гема в эритроидных предшественниках. Большинство сидеробластных анемий приобретаются как клональные нарушения эритропоэза. Кроме того, кольцевидные сидеробласты могут быть обнаружены у истощенных пациентов, злоупотребляющих алкоголем [17].
Лекарственно-индуцированная сидеробластная анемия была связана с изониазидом [18]. Анемия устраняется пироксидином или отменой изониазида. Хлорамфеникол, редко используемый в настоящее время, вызывает обратимое подавление эритропоэза и образование кольцевидных сидеробластов [17]. Линезолид, пеницилламин и дигидрохлорид триэтилентетрамина (хелатирующий агент, используемый для лечения болезни Вильсона) вызывают обратимую СА [19–21]. Миелодисплазии и вторичные острые лейкозы, вызванные химиотерапией, обсуждаемые ниже, могут первоначально проявляться как сидеробластная анемия [22].
Анемия устраняется пироксидином или отменой изониазида. Хлорамфеникол, редко используемый в настоящее время, вызывает обратимое подавление эритропоэза и образование кольцевидных сидеробластов [17]. Линезолид, пеницилламин и дигидрохлорид триэтилентетрамина (хелатирующий агент, используемый для лечения болезни Вильсона) вызывают обратимую СА [19–21]. Миелодисплазии и вторичные острые лейкозы, вызванные химиотерапией, обсуждаемые ниже, могут первоначально проявляться как сидеробластная анемия [22].
7. Апластическая анемия
Апластическая анемия (АА), характеризующаяся панцитопенией с гипоцеллюлярным поражением костного мозга, может быть наследственной или приобретенной. Приобретенная апластическая анемия чаще всего является идиопатической, но может быть вторичной по отношению к воздействию токсинов, облучения, вирусов и лекарств. АА может развиваться как прямой ответ на воздействие, но также может развиваться косвенно, через иммунно-опосредованные механизмы. Исторически сложилось так, что лекарственно-индуцированную АА трудно отличить от идиопатических форм заболевания, поскольку при наличии редких сообщений о случаях трудно установить причинно-следственную связь [23]. С иммунологической точки зрения отсутствие антител при апластической анемии свидетельствует о том, что лекарства не служат простыми гаптенами в инициации апластической недостаточности костного мозга.
С иммунологической точки зрения отсутствие антител при апластической анемии свидетельствует о том, что лекарства не служат простыми гаптенами в инициации апластической недостаточности костного мозга.
Лекарства, вызывающие АА, включают противоревматические препараты, антитиреоидные препараты, противотуберкулезные препараты, НПВП и противосудорожные препараты. Упомянутые конкретные препараты включают хлорамфеникол, бутазон, сульфонамид, соли золота, пеницилламин, амидопирин, триметоприм/сульфаметоксазол, метимазол и фелбамат [24–27].
Многие препараты, вызывающие апластическую анемию, также чаще могут вызывать легкое угнетение костного мозга, что позволяет предположить, что предварительное повреждение может иногда (возможно, связанное с метаболизмом хозяина) прогрессировать до более серьезного повреждения. Лечение и прогноз лекарственно-индуцированной апластической анемии аналогичны идиопатическим случаям [23].
8. Чистая эритроцитарная аплазия
Чистая эритроцитарная аплазия (PRCA) характеризуется нормоцитарной анемией, ретикулоцитопенией и отсутствием зрелых костномозговых эритроидных клеток-предшественников.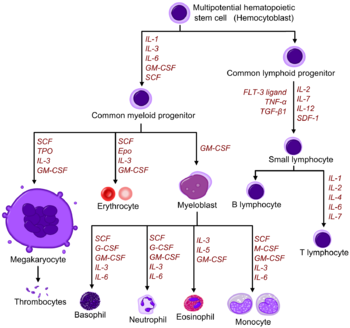 PRCA отличается от апластической анемии относительно нормальным числом лейкоцитов и тромбоцитов. Он может быть врожденным или приобретенным. Приобретенная PRCA может быть идиопатической или вторичной, либо острой, самокупирующейся патологией, либо персистирующей, хронической рефрактерной анемией. PRCA может возникать в связи с тимомой, лимфоидным раком, парвовирусом, ревматоидным артритом, беременностью и приемом лекарств.
PRCA отличается от апластической анемии относительно нормальным числом лейкоцитов и тромбоцитов. Он может быть врожденным или приобретенным. Приобретенная PRCA может быть идиопатической или вторичной, либо острой, самокупирующейся патологией, либо персистирующей, хронической рефрактерной анемией. PRCA может возникать в связи с тимомой, лимфоидным раком, парвовирусом, ревматоидным артритом, беременностью и приемом лекарств.
PRCA можно заразиться при воздействии ряда лекарств, включая иммунодепрессанты (азатиоприн, FK506, антитимоцитарный глобулин), антибактериальные препараты (линезолид, изониазид, рифампицин, хлорамфеникол), противовирусные препараты (интерферон-альфа, ламивудин, зидовудин), флударабин, противосудорожные препараты (дифенилдрантоин, карбамазепин, вальпоровая кислота), а также хлорохин, аллопуринол, рибавирин и золото [28, 29].
Кроме того, сообщалось, что PRCA развивается после длительного воздействия рекомбинантного человеческого эритропоэтина (rHuEPO), особенно торговой марки Eprex, преимущественно используемой в Европе [30–33]. Отмена rHuEPO с последующим лечением иммунодепрессантами (циклоспорином А) в течение нескольких месяцев делала пациентов отрицательными к антителам к ЭПО и независимыми от трансфузий. PRCA, по-видимому, происходит преимущественно при подкожном введении у пациентов с почечной недостаточностью. Частота этого осложнения снизилась, по-видимому, в результате изменений в рецептуре и обращении, которые могли снизить иммуногенность [33].
Отмена rHuEPO с последующим лечением иммунодепрессантами (циклоспорином А) в течение нескольких месяцев делала пациентов отрицательными к антителам к ЭПО и независимыми от трансфузий. PRCA, по-видимому, происходит преимущественно при подкожном введении у пациентов с почечной недостаточностью. Частота этого осложнения снизилась, по-видимому, в результате изменений в рецептуре и обращении, которые могли снизить иммуногенность [33].
9. Иммунная тромбоцитопения
При иммунной тромбоцитопении пурпура (ИТП) разрушение тромбоцитов вызывается связыванием антител с тромбоцитами, что приводит к их клиренсу ретикулоэндотелиальной системой (РЭС), а также к некоторой степени снижения продукции. ИТП может быть идиопатическим или связанным с вирусными инфекциями, аутоиммунными заболеваниями, лимфопролиферативными заболеваниями или лекарствами [34, 35].
Классическими причинами медикаментозной тромбоцитопении являются хинин и хининоподобные препараты [36].Тромбоцитопения обычно внезапная, тяжелая и может сопровождаться кровотечением. Тромбоцитопения, вызванная этими препаратами, вызвана антителами, которые не реагируют в отсутствие препарата, но связываются с эпитопами на мембране тромбоцитов, гликопротеинами IIb/IIIa или Ib/IX, когда присутствует сенсибилизирующий препарат. Ванкомицин также может быть связан с выраженной тромбоцитопенией и доказуемыми лекарственно-зависимыми антителами в сыворотке [37]. У пациентов с почечной недостаточностью может возникать длительная тромбоцитопения, вероятно, из-за замедленного клиренса препарата.Другие препараты, связанные с иммунной тромбоцитопенией, включают противомикробные препараты (сульфаниламиды, рифампин, линезолид), противовоспалительные препараты, противоопухолевые препараты, антидепрессанты, бензодиазепины, противосудорожные препараты (карбамазепин, фенитоин, вальпроевая кислота), а также сердечные и антигипертензивные препараты [34, 35]. Хотя ИТП обычно развивается быстро, обычно она проходит после прекращения лечения и зависит от препарата.
Тромбоцитопения, вызванная этими препаратами, вызвана антителами, которые не реагируют в отсутствие препарата, но связываются с эпитопами на мембране тромбоцитов, гликопротеинами IIb/IIIa или Ib/IX, когда присутствует сенсибилизирующий препарат. Ванкомицин также может быть связан с выраженной тромбоцитопенией и доказуемыми лекарственно-зависимыми антителами в сыворотке [37]. У пациентов с почечной недостаточностью может возникать длительная тромбоцитопения, вероятно, из-за замедленного клиренса препарата.Другие препараты, связанные с иммунной тромбоцитопенией, включают противомикробные препараты (сульфаниламиды, рифампин, линезолид), противовоспалительные препараты, противоопухолевые препараты, антидепрессанты, бензодиазепины, противосудорожные препараты (карбамазепин, фенитоин, вальпроевая кислота), а также сердечные и антигипертензивные препараты [34, 35]. Хотя ИТП обычно развивается быстро, обычно она проходит после прекращения лечения и зависит от препарата.
Хорошо известно, что гепарин связан с тромбоцитопенией, иногда с артериальным или венозным тромбозом, который обычно представляет гораздо большую угрозу, чем риск кровотечения [38, 39]. Гепарин-индуцированная иммунная тромбоцитопения вызывается антителами против комплекса гепарина и тромбоцитарного фактора 4 (PF4), что может привести к активации тромбоцитов и инициации тромбозов. Хотя гепарин также может индуцировать более легкую неиммуноопосредованную тромбоцитопению, иммунная версия потенциально более тяжелая. Гепарин-индуцированная тромбоцитопения следует за воздействием как нефракционированного, так и низкомолекулярного гепарина, но менее распространена при применении последнего. Обычно задержка составляет 5–10 дней у впервые подвергшихся воздействию гепарина пациентов, но тромбоцитопения может развиться в течение нескольких часов у пациентов, подвергшихся недавнему воздействию гепарина, но все еще имеющих антитела к PF4, или в течение нескольких дней у лиц, подвергшихся предшествующему воздействию, у которых развился анамнестический ответ.Иногда могут возникать венозная гангрена, некроз кожи и острые реакции анафилактического типа на гепарин. В соответствующих клинических условиях диагноз подтверждается наличием антигепариновых антител, которые можно обнаружить с помощью ряда анализов.
Гепарин-индуцированная иммунная тромбоцитопения вызывается антителами против комплекса гепарина и тромбоцитарного фактора 4 (PF4), что может привести к активации тромбоцитов и инициации тромбозов. Хотя гепарин также может индуцировать более легкую неиммуноопосредованную тромбоцитопению, иммунная версия потенциально более тяжелая. Гепарин-индуцированная тромбоцитопения следует за воздействием как нефракционированного, так и низкомолекулярного гепарина, но менее распространена при применении последнего. Обычно задержка составляет 5–10 дней у впервые подвергшихся воздействию гепарина пациентов, но тромбоцитопения может развиться в течение нескольких часов у пациентов, подвергшихся недавнему воздействию гепарина, но все еще имеющих антитела к PF4, или в течение нескольких дней у лиц, подвергшихся предшествующему воздействию, у которых развился анамнестический ответ.Иногда могут возникать венозная гангрена, некроз кожи и острые реакции анафилактического типа на гепарин. В соответствующих клинических условиях диагноз подтверждается наличием антигепариновых антител, которые можно обнаружить с помощью ряда анализов. К ним относятся более чувствительные серологические анализы (например, с помощью ELISA) и функциональные, более специфичные анализы, такие как измерение высвобождения серотонина тромбоцитами C-14 в присутствии гепарина и сыворотки. В дополнение к прекращению использования гепарина лечение включает антикоагулянтную терапию для снижения риска тромбоза, обычно вначале аргатробан, бивалрудин или лепирудин с переходом на варфарин.Антикоагулянтную терапию следует продолжать в течение нескольких недель даже после нормализации числа тромбоцитов из-за высокого риска тромбоза в течение этого времени.
К ним относятся более чувствительные серологические анализы (например, с помощью ELISA) и функциональные, более специфичные анализы, такие как измерение высвобождения серотонина тромбоцитами C-14 в присутствии гепарина и сыворотки. В дополнение к прекращению использования гепарина лечение включает антикоагулянтную терапию для снижения риска тромбоза, обычно вначале аргатробан, бивалрудин или лепирудин с переходом на варфарин.Антикоагулянтную терапию следует продолжать в течение нескольких недель даже после нормализации числа тромбоцитов из-за высокого риска тромбоза в течение этого времени.
Абциксимаб (химерный Fab-фрагмент) и эптифибатид и тирофибан (ингибиторы-миметики лигандов) часто используются после коронарной ангиопластики для уменьшения тромбоза за счет нарушения функции тромбоцитов посредством ингибирования взаимодействия GP IIb/IIIa-фибриноген. Однако в дополнение к желаемой дисфункции тромбоцитов они могут вызывать тяжелую тромбоцитопению у небольшого процента пациентов, вероятно, через механизм, опосредованный антителами, зависящий от лекарств [40]. Это может начаться в течение нескольких часов или дней и обычно проходит спонтанно через 2–5 дней. Это может произойти при начальной или последующей инфузии. Большинство пациентов выздоравливают без осложнений, хотя иногда могут возникать сильные кровотечения. Переливание тромбоцитов может быть назначено, если есть значительное кровотечение.
Это может начаться в течение нескольких часов или дней и обычно проходит спонтанно через 2–5 дней. Это может произойти при начальной или последующей инфузии. Большинство пациентов выздоравливают без осложнений, хотя иногда могут возникать сильные кровотечения. Переливание тромбоцитов может быть назначено, если есть значительное кровотечение.
10. Тромботические микроангиопатии
Тромботические микроангиопатии (ТМА) проявляются тромбоцитопенией, микроангиопатической гемолитической анемией и симптомами окклюзии микрососудов.Они возникают из-за избыточной агрегации тромбоцитов. ТМА часто ассоциируется с низким уровнем металлопротеазы ADAMTS13, которая индуцирует расщепление фактора фон Виллебранда (vWF). Тромботическая тромбоцитопеническая пурпура (ТТП) и гемолитико-уремический синдром (ГУС) являются основными тромботическими микроангиопатиями. ТМА может быть семейной, идиопатической или приобретенной вследствие воздействия токсинов, беременности, инфекций (например, ВИЧ, некоторых шигелл и кишечной палочки) и лекарств 90–284.
Хотя лекарственно-индуцированная ТМА хорошо задокументирована, ее механизм точно не определен [41–44].Чаще всего предполагают иммуноопосредованные или прямые факторы токсичности. У некоторых пациентов с лекарственной ТМА присутствуют аутоантитела к протеазе ADAMTS13, у некоторых пациентов частота ТМА, по-видимому, является дозозависимой, а во многих случаях «намеки» на механизм вообще отсутствуют.
Одним из препаратов, обычно вызывающих ТМА, является иммунодепрессант циклоспорин А (ЦиА). CyA-индуцированная ТМА часто наблюдается у пациентов с трансплантацией (твердой или жидкой), а также у пациентов, получающих лечение по поводу ревматоидного артрита и увеита.Предполагается, что механизм заключается в дозозависимой токсичности. ТМА обычно проходит после уменьшения или прекращения лечения CyA.
Другие препараты, связанные с ТМА, включают химиотерапевтические агенты митомицин-С, гемцитабин и цисплатин, а также α -интерферон и такролимус [41–43]. У пациентов с метастатической аденокарциномой может быть трудно отличить лекарственно-индуцированную ТМА от анемии, тромбоцитопении и микроангиопатии, связанных с карциноматозом. Митомицин-С является известным нефротоксином, и есть доказательства того, что его механизм индуцирования ТМА представляет собой дозозависимое прямое токсическое действие на эндотелий.
Митомицин-С является известным нефротоксином, и есть доказательства того, что его механизм индуцирования ТМА представляет собой дозозависимое прямое токсическое действие на эндотелий.
Тиенопиридины, антиагреганты тиклопидин и реже клопидогрель также участвуют в индукции ТМА [44]. TPA, связанная с тиклопидином, с большей вероятностью возникает после как минимум двух недель терапии, связана с низкими уровнями ADAMTS13 с очевидными аутоантителами и приносит пользу от терапии плазмаферезом. Клопидогрел-индуцированная ТМА, как правило, возникает в течение первых двух недель лечения, с меньшей вероятностью связана с низкими уровнями ADAMTS13 и аутоантителами и с меньшей вероятностью приносит пользу от плазмафереза.
Хинин также может вызывать ТМА. Механизм иммуноопосредованный. У пациентов с индуцированной хинином ТМА были обнаружены антитела против эндотелиальных клеток, лимфоцитов и гранулоцитов, а также хининзависимые антитела, включая IgG или IgM, реагирующие с гликопротеинами тромбоцитов Ib/IX или IIb/IIIa. ТМА обычно разрешается отменой хинина вместе с плазмаферезом [45].
ТМА обычно разрешается отменой хинина вместе с плазмаферезом [45].
11. Дисфункция тромбоцитов
Нарушения функции тромбоцитов могут быть обнаружены у пациентов с удлиненным временем кровотечения, но нормальным количеством тромбоцитов.Хотя индуцирование дисфункции тромбоцитов для снижения риска тромбоза часто является желаемой целью некоторых препаратов (таких как аспирин, клопидогрель и ингибиторы анти-GP IIb/IIIa), это также может быть нежелательным побочным эффектом [46].
Ацетилирование циклооксигеназы 1 (ЦОГ 1) приводит к нарушению синтеза важного агониста тромбоцитов тромбоксана. Аспирин необратимо ацетилирует ЦОГ-1, так что его действие сохраняется даже после прекращения циркуляции препарата. Это контрастирует с неселективными нестероидными противовоспалительными препаратами, которые обратимо ацетилируют ЦОГ-1.Имеются некоторые данные о дозозависимом влиянии аспирина на агрегацию тромбоцитов [47].
Флуоксетин и некоторые трициклические антидепрессанты вызывают дисфункцию путем ингибирования захвата серотонина. Некоторые препараты могут нарушать адгезию или агрегацию тромбоцитов, в том числе высокие дозы пенилинов и других β-лактамных антибиотиков, химиотерапевтические препараты, такие как митрамицин и даунорубицин, иммунодепрессанты и фенотиазины [46].
Некоторые препараты могут нарушать адгезию или агрегацию тромбоцитов, в том числе высокие дозы пенилинов и других β-лактамных антибиотиков, химиотерапевтические препараты, такие как митрамицин и даунорубицин, иммунодепрессанты и фенотиазины [46].
12. Гиперкоагуляция
Гиперкоагуляция со склонностью к артериальному и венозному тромбозу может быть наследственной или приобретенной.Наследственные тромбофилические состояния включают, среди прочего, фактор Лейдена, мутацию протромбина G20210A и дефицит белков или антитромбина III. Приобретенные состояния гиперкоагуляции могут быть вторичными по отношению к неподвижности, хирургическому вмешательству, травме, беременности, антифосфолипидному синдрому, раку и лекарственным препаратам.
Селективные ингибиторы ЦОГ-2 с меньшим потенциалом кровотечения и желудочно-кишечной токсичности, чем традиционные ингибиторы ЦОГ, стали широко использоваться в качестве анальгетиков и противовоспалительных средств, а также были исследованы на предмет их потенциального эффекта снижения риска полипов и колоректального рака. Однако в нескольких исследованиях было обнаружено, что целекоксиб, рофекоксиб и вальдекоксиб связаны с учащением тромботических сердечно-сосудистых событий [48–50]. Эти результаты привели к добровольному отзыву рофекоксиба с мирового рынка и стали предметом пристального внимания в отношении фармацевтической политики и политики FDA.
Однако в нескольких исследованиях было обнаружено, что целекоксиб, рофекоксиб и вальдекоксиб связаны с учащением тромботических сердечно-сосудистых событий [48–50]. Эти результаты привели к добровольному отзыву рофекоксиба с мирового рынка и стали предметом пристального внимания в отношении фармацевтической политики и политики FDA.
Эритропоэтин связан с повышенным риском тромбообразования. В то время как эритропоэтин заметно улучшает анемию почечной недостаточности, направляя уровни гемоглобина на высокий нормальный уровень, он был связан с более высокой сердечно-сосудистой заболеваемостью и смертностью, чем с более низкими целевыми уровнями [51].Также были подняты вопросы о безопасности эритропоэтина у больных раком. Метаанализ действительно показал повышенный риск тромбообразования у пациентов, получавших лечение, а некоторые исследования показали повышенный риск смерти [52]. Руководство по более ограниченному и более безопасному использованию этих препаратов у онкологических больных находится в процессе модификации.
Гормональная терапия, включая оральные контрацептивы, заместительную гормональную терапию и тамоксифен (селективный модулятор рецепторов эстрогена с некоторой агонистической активностью) связана с повышенным риском тромбообразования.При приеме пероральных контрацептивов риск артериального и венозного тромбоза может увеличиваться с возрастом, генетическими тромбофилиями, курением и использованием некоторых типов связанных прогестинов [53]. Исследование Women’s Health Initiative показало, что использование комбинированного эстрогена и прогестина вдвое увеличивает риск венозного тромбоза по сравнению с плацебо-контролем [54]. Было обнаружено, что для химиопрофилактики рака молочной железы ралоксифен имеет более низкий риск тромбоза, а также рака матки, чем тамоксифен, и, следовательно, может быть более безопасным препаратом в этих условиях [55].Аналогичным образом, ингибиторы ароматазы, такие как анастразол, летрозол или экземестан, используемые для лечения раннего или распространенного рака молочной железы, демонстрируют более низкий риск тромбообразования, чем тамоксифен [56].
Адъювантная химиотерапия рака молочной железы с CMF (циклофосфамид, метотрексат, фторурацил), более старый режим, редко используемый в настоящее время, был связан с гиперкоагуляцией [57–59]. У пациентов, получавших CMF, могут быть снижены уровни белков-ингибиторов и [57]. Тромбоз у пациенток, получающих адъювантную химиотерапию, возможно, стал менее распространенным отчасти из-за изменения используемых типов химиотерапии, более короткой продолжительности химиотерапии, менее частого использования тамоксифена у пациенток в постменопаузе и менее частого использования сопутствующей (в отличие от последовательной химиотерапии). ) химиотерапия и тамоксифен [58].
Тромботические осложнения были связаны с аспарагиназой, используемой для лечения острого лимфобластного лейкоза [60–62]. Могут возникать артериальные и венозные тромбозы (включая церебральные венозные синусы). L-аспарагиназа ингибирует синтез белка за счет гидролиза незаменимой аминокислоты аспарагина, вызывает снижение синтеза антитромбина III, протеина и протеина, что приводит к повышенному риску тромбообразования.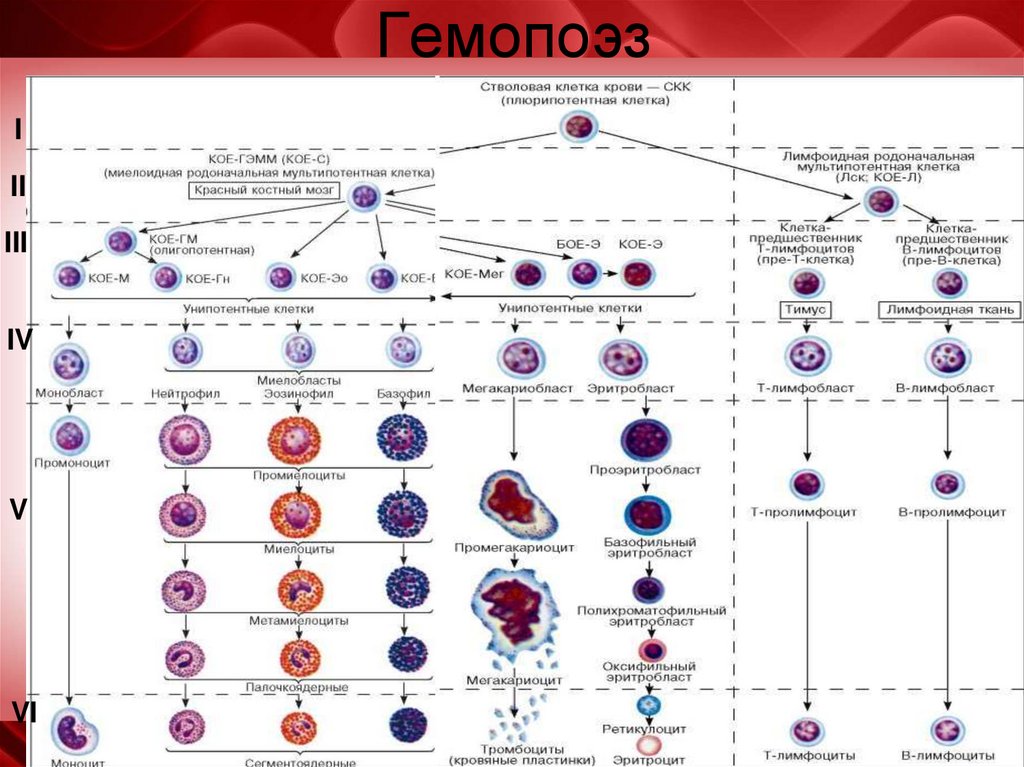
Талидомид и леналидомид, применяемые при множественной миеломе, связаны с повышенным риском тромбообразования при использовании в комбинации с глюкокортикоидами [63].Рекомендуются различные профилактические меры, включая варфарин, гепарин и аспирин. Применение менее интенсивной схемы введения дексаметазона один раз в неделю снижает риск тромбообразования по сравнению со стандартной 4-дневной схемой введения высоких доз в комбинации с леналидомидом [63].
Тромбоз, вызванный приемом варфарина или гепарина, может быть связан с некрозом кожи. Варфарин-индуцированный некроз кожи часто связан с уже существующими тромбофилическими состояниями, такими как дефицит белка или антитромбина III [64].Терапия заключается в отмене варфарина, назначении витаминов и антикоагулянтной терапии гепарином. Однако гепарин также может вызывать некроз кожи, который может быть частью синдрома гепарин-индуцированной тромбоцитопении [65].
Бевацизумаб, моноклональное антитело против сосудистого эндотелиального фактора роста, используется при метастатическом раке толстой кишки, легкого и молочной железы, что связано с повышенным артериальным тромботическим риском, особенно у пожилых людей, уже предрасположенных к сердечно-сосудистым событиям [66].
13. Циркулирующие антикоагулянты
Циркулирующие антикоагулянты ингибируют факторы свертывания крови, вызывая избыточное кровотечение. Аутоантитела, такие как приобретенные ингибиторы к фактору VIII, могут быть идиопатическими или вторичными по отношению к наследственной гемофилии, послеродовому состоянию, другим аутоиммунным заболеваниям, злокачественным новообразованиям или лекарственным препаратам. У пациентов наблюдается кровотечение как синдром приобретенной гемофилии с низким уровнем F VIII: и выраженными ингибиторами F VIII. Причастные лекарства включают антибиотики, психотропные средства, флударабин и интерферон [67].Активность антител исчезает при прекращении приема препарата или при применении иммунодепрессантов. Приобретенный ингибитор фактора XIII, который сшивает и стабилизирует фибрин, связан с изониазидом [68].
Волчаночный антикоагулянт и антифосфолипидные антитела могут быть вызваны такими препаратами, как хлорпромазин, гидралазин, фенитоин, хинин и прокаинамид [69, 70]. В этих случаях существует связь с гиперкоагуляцией, а не с кровотечением.
В этих случаях существует связь с гиперкоагуляцией, а не с кровотечением.
14.Гипопротромбинемия
Гипопротромбинемия с удлинением ПВ/МНО чаще всего возникает из-за дефицита витаминов или заболеваний печени. Некоторые лекарства, такие как антибиотики широкого спектра действия, связаны с гипопротромбинемией, обычно у пациентов, которые также истощены. Сообщения связывают сульфаниламиды, ампициллин, хлорамфеникол, тетрациклины и цефокситин с дефицитом витамин-зависимых факторов свертывания крови [71]. Цефалоспорины могут быть связаны с гипопротромбинемией, особенно с боковой цепью N-метилтиотетразола (NMTT) (например,g., моксалактам, цефоперазон), хотя они больше не используются широко [72].
У пациентов, принимающих варфарин, многие препараты, особенно антибиотики, вызывают усиление кровотечения. Отмечается, что систематической работы по этому вопросу мало, основными источниками являются отчеты о клинических случаях [73]. Тем не менее, очевидно, что многие препараты влияют на кумадин, изменяя фармакокинетику или динамику (например, антибиотики, особенно хинолоны, макролиды и азолы), в то время как другие повышают риск кровотечения по своим собственным механизмам (например, антибиотики). г., аспирин, гепарин, тиклопидин и НПВП). При назначении этих препаратов пациентам, принимающим варфарин, необходим тщательный мониторинг и коррекция дозы.
г., аспирин, гепарин, тиклопидин и НПВП). При назначении этих препаратов пациентам, принимающим варфарин, необходим тщательный мониторинг и коррекция дозы.
15. Агранулоцитоз/нейтропения
Лекарственная нейтропения может возникать при приеме различных анальгетиков, психотропных, противосудорожных, антитиреоидных, антигистаминных, противоревматических, желудочно-кишечных, противомикробных, сердечно-сосудистых и, как ожидается, химиотерапевтических препаратов. [74–76]. Иммуноопосредованные механизмы связаны с некоторыми лекарствами, такими как пенициллины, которые действуют как гаптены, индуцирующие образование антител против нейтрофилов.Клозапин ускоряет апоптоз нейтрофилов, а пропитиоурацил вызывает комплементопосредованную деструкцию нейтрофилов. Лекарства, такие как бета-лактамные антибиотики, карбамазепин и вальпроат, обладают дозозависимым ингибированием гранулопоэза. Препараты с прямым токсическим действием на миелоидные предшественники включают тиклопидин, булсуфан, метамизол, этосуксимид и хлорпромазин.
Лечение лекарственно-индуцированной нейтропении включает отмену препарата, покрытие антибиотиками, когда это необходимо, и все более широкое введение рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора (rhG-CSF).Использование КСФ может уменьшить продолжительность нейтропении, частоту инфекции и, возможно, смертность, особенно у пациентов с глубокой нейтропенией [76]. Смертность, хотя и ниже, чем в прошлом, по-прежнему составляет около 5%.
Ритуксимаб, антитело к CD20, используемое для лечения В-клеточных лимфопролиферативных заболеваний и доброкачественных аутоиммунных заболеваний, может вызывать нейтропению, обычно с отсроченным началом [77].
16. Нейтрофилия
Нейтрофилия может быть связана с миелопролиферативными заболеваниями, но чаще возникает в результате инфекции или воспаления.Лекарства также могут вызывать лейкоцитоз. Глюкокортикоиды вызывают нейтрофилию, индуцируя высвобождение нейтрофилов из костного мозга [78]. Несмотря на изменчивость, глюкокортикоиды обычно не вызывают избыточный лейкоцитоз или сдвиг влево. Такое повышение количества лейкоцитов или увеличение количества полос может свидетельствовать о наличии инфекции [79]. Адреномиметики и адреналин вызывают нейтрофилию, высвобождая нейтрофилы из маргинального пула [78]. Литий вызывает легкую нейтрофилию и использовался для лечения нейтропении до появления CSF [80].
Такое повышение количества лейкоцитов или увеличение количества полос может свидетельствовать о наличии инфекции [79]. Адреномиметики и адреналин вызывают нейтрофилию, высвобождая нейтрофилы из маргинального пула [78]. Литий вызывает легкую нейтрофилию и использовался для лечения нейтропении до появления CSF [80].
Лейкоцитоз обычно наблюдается при приеме Г/ГМ-КСФ, который часто назначают для уменьшения тяжести и продолжительности нейтропении, вызванной химиотерапией. Синдром Свита (острый фебрильный нейтрофильный дерматоз), характеризующийся болезненными эритематозными поражениями кожи, лихорадкой и нейтрофилией, может быть вызван такими препаратами, как триметоприм-сульфаметоксазол, другие антибиотики и гранулоцитарный колониестимулирующий фактор [81]. Синдром также может быть идиопатическим или паранеопластическим.
17. Эозинофилия
Эозинофилия может быть следствием как внутренних гематологических нарушений, так и вторичной по отношению к различным системным заболеваниям и аллергенам, включая лекарства [82]. Лекарства, наиболее часто связанные с этим заболеванием, включали пенициллины, сульфаты, аллопуринол, фенитоин, карбамазепин и золото. Лекарственная сыпь с эозинофилией и системными симптомами (синдром DRESS) описывает связь эозинофилии с сыпью, лихорадкой и поражением внутренних органов, таким как пневмонит, гепатит, нефрит, аденопатия или кардит [83]. DRESS чаще всего ассоциируется с антибиотиками и противосудорожными препаратами, но также могут быть вовлечены и другие агенты.
Лекарства, наиболее часто связанные с этим заболеванием, включали пенициллины, сульфаты, аллопуринол, фенитоин, карбамазепин и золото. Лекарственная сыпь с эозинофилией и системными симптомами (синдром DRESS) описывает связь эозинофилии с сыпью, лихорадкой и поражением внутренних органов, таким как пневмонит, гепатит, нефрит, аденопатия или кардит [83]. DRESS чаще всего ассоциируется с антибиотиками и противосудорожными препаратами, но также могут быть вовлечены и другие агенты.
18. Полицитемия
Полицитемия может быть первичной (истинная полицитемия) или вторичной вследствие курения, хронической гипоксии, некоторых опухолей или лекарств.Медикаментозная полицитемия может наблюдаться при избыточном использовании рчЭПО или анаболических стероидов. Злоупотребление обоими типами препаратов спортсменами может быть связано с повышенным риском тромбообразования [84]. Использование диуретиков с уменьшением объема может способствовать развитию псевдополицитемии, когда гематокрит повышается из-за гемоконцентрации, но истинная масса эритроцитов не увеличивается.
19. Миелодисплазия и острый лейкоз
Миелодиспластические синдромы (МДС) и острый миелоидный лейкоз (ОМЛ) представляют собой клональные нарушения кроветворения, связанные с цитопенией, нарушением созревания костного мозга и, в конечном итоге, с нерегулируемой пролиферацией бластов.Многие случаи МДС перерастают в ОМЛ, и, хотя эти два заболевания различны, они имеют непрерывный спектр.
Большинство случаев МДС и ОМЛ являются идиопатическими, но воздействие токсинов и радиации может увеличить риск. Лекарства также могут вызывать МДС [85, 86]. Алкилирующие агенты (такие как азотистый иприт, циклофосфамид, мелфалан, бусуфлан, хлорамбуцил) являются наиболее часто упоминаемыми виновниками. Риск связан с общей дозой, продолжительностью и конкретным типом алкилирующего агента. Прокарбазин и нитрозомочевины также связаны с миелодисплазией и лейкемией.До развития -МДС или ОМЛ может существовать латентный период продолжительностью 2–8 лет. Лейкемии, индуцированной этими агентами, обычно предшествует миелодиспластический синдром. Эти лейкозы морфологически обычно представляют собой FAB M1 или M2. Типичны сложные хромосомные аномалии, обычно с делециями хромосом 5 и 7 и трисомией 8.
Эти лейкозы морфологически обычно представляют собой FAB M1 или M2. Типичны сложные хромосомные аномалии, обычно с делециями хромосом 5 и 7 и трисомией 8.
Отчетливый синдром вторичного лейкоза связан с ингибиторами топоизомеразы II, которые включают эпиподофиллотоксины (этопозид и тенипозид), антрациклины (дауномицин, эпирубицин и доксорубицин.) и митоксантрон. Лейкемия с этими агентами имеет более короткий латентный период, чем связанный с алкилирующими агентами, часто менее 2 лет и обычно проявляется без предшествующего МДС. Морфологически обычно наблюдаются острые миеломоноцитарные лейкозы с кариотипической аномалией, включающей 11q23.
Описан также связанный с лечением острый промиелоцитарный лейкоз, чаще всего в сочетании с ингибиторами topo II [87]. Они также имеют относительно короткий латентный период после лечения без предшествующей предлейкемической фазы.Как и de novo APL, (15; 17) с PML-RAR часто встречаются альфа-перегруппировки. Исходы лечения относительно благоприятны при лечении как ОПЛ de novo, в отличие от плохого прогноза, наблюдаемого при других типах ОМЛ.
У пациенток, получающих адъювантную химиотерапию по поводу рака молочной железы, риск острого лейкоза увеличивается с возрастом, интенсивностью терапии и применением лучевой терапии молочной железы [88]. Многие из этих пациентов получали как алкилирующие агенты, так и антрациклины, оба из которых являются лейкемогенными.Кроме того, в некоторых [89], но не во всех исследованиях [90] был отмечен повышенный риск ОМЛ у больных раком молочной железы, получавших Г-КСФ вместе с адъювантной химиотерапией.
Трансплантация стволовых клеток, используемая при высоком риске, рецидивах и рефрактерных гематологических злокачественных новообразованиях, связана с риском вторичного МДС и лейкемии. Остается неясным, вызвано ли заболевание предтрансплантационной терапией или самой трансплантацией.
Радиоиммунотерапия, разработанная для неходжкинской лимфомы, может быть связана с некоторым риском лейкемогенеза.Однако, как и в случае с пациентами, перенесшими трансплантацию, некоторый риск может быть связан с повреждением стволовых клеток в результате предшествующего лечения или, возможно, с повышенным риском, связанным с самим основным заболеванием. Небольшое количество пациентов, получавших только радиоиммунотерапию, показало, по-видимому, низкий риск развития лейкемии [93].
Небольшое количество пациентов, получавших только радиоиммунотерапию, показало, по-видимому, низкий риск развития лейкемии [93].
20. Выводы
Широкий спектр лекарственно-индуцированных гематологических синдромов опосредуется различными механизмами, включая иммунные эффекты, взаимодействия с ферментативными путями и прямое ингибирование кроветворения.В таблице представлены рассмотренные выше гематологические синдромы, вызванные лекарственными препаратами. Предоставление доказательств того, что лекарство вызывает тот или иной гематологический синдром, часто невозможно. Многие пациенты одновременно получают несколько препаратов, что затрудняет установление причинно-следственной связи. Повторный прием препарата, подозреваемого в токсичности, обычно не рекомендуется. Для некоторых препаратов, таких как гепарин, хинидин и ванкомиин, были проведены испытания in vitro и выяснены механизмы цитопении. Однако такое тестирование не всегда возможно, учитывая, что для большинства из них не существует стандартизированных коммерчески доступных анализов и что реакции могут быть связаны с метаболитами, а не с более легко тестируемыми исходными соединениями.
По мере развития медицины старые лекарства устаревают и заменяются новыми препаратами. Многие препараты, ранее ассоциировавшиеся с гематологической токсичностью (например, пенициллин, альфа-метил-допа, хинидин, золото и хлорамфеникал), больше не используются. Однако обнаружено, что новые препараты связаны с их собственной потенциальной гематологической токсичностью (например, клопидогель, линезолид, рибавирин, ритуксимаб и ингибиторы GPIIb/IIIa). Кроме того, в дополнение к классической цитопении, вызванной лекарственными препаратами, мы все чаще наблюдаем тромбоз как общую тему с рядом разнообразных агентов (например,г., гепарин, ингибиторы ЦОГ-2, бевацизумаб, заместительная гормональная терапия, тамоксифен, эритропоэтин, талидомид и леналидомид). Врачи самых разных специальностей должны понимать гематологические последствия лекарств и быть готовыми к возникновению и коррекции этих явлений у своих пациентов.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Prime PabMed | [Механизмы цитостатического повреждения и регенерации гемопоэза]
Цитирование
Гольдберг Э Д. , и другие. «[Механизмы гемопоэза, цитостатического повреждения и регенерации]». Вестник Российской академии медицинских наук, 1998, с. 6-10.
, и другие. «[Механизмы гемопоэза, цитостатического повреждения и регенерации]». Вестник Российской академии медицинских наук, 1998, с. 6-10.
Гольдберг Э.Д., Дыгай А.М., Зданов В.В. Механизмы цитостатического повреждения и регенерации кроветворения. Вестн Росс Акад Мед Наук . 1998.
Гольдберг Э.Д., Дыгай А.М., Зданов В.В. (1998). Механизмы цитостатического повреждения и регенерации кроветворения. Вестник Российской академии медицинских наук , (10), 6-10.
Гольдберг Э.Д., Дыгай А.М., Зданов В.В. Механизмы цитостатического повреждения и регенерации кроветворения. Вестн Росс Акад Мед Наук. 1998;(10)6-10. PubMed PMID: 9846103.
TY — JOUR
T1 — [Механизмы цитостатического повреждения и регенерации гемопоэза].
AU — Гольдберг, Э Д,
АУ — Дыгай,А М,
АУ — Зданов В В,
PY — 10.12.1998/опубликовано
PY — 10 декабря 1998 г. / Медлайн
PY — 1998/12/10/антрез
СП — 6
ЭП — 10
JF — Вестник Российской академии медицинских наук
JO — Вестн Росс Акад Мед Наук
ИС — 10
N2 — костномозговое кроветворение, состояние коммитированного пула клеток-предшественников и характер их взаимодействия с элементами гемопоэзиндуцирующего микроокружения (ГИМ), уровень гуморальных стимуляторов секреции изучали после однократного введения 5-фторурацила (5 -ФУ), циклофосфамид (ЦФ) или адриамицин (А) мышам в максимально переносимых дозах. Показано, что цитостатические изменения в восстановлении кроветворения зависят в первую очередь от отношений пролиферации-дифференциации в кроветворных клетках, что, в свою очередь, определяется состоянием клеток ГИМ после цитостатического воздействия. Повышенная функциональная активность элементов ГИМ в ответ на повреждение кроветворной ткани, вызванное А или КФ, способствует быстрому восстановлению кроветворения, которое значительно ускоряется при использовании рекомбинантного колониестимулирующего фактора (КСФ) и, в меньшей степени, глициррама, растительного препарата.В то же время 5-ФУ, вызывая длительную гипоплазию костного мозга, нарушал функцию клеток микроокружения. Использование этой модели продемонстрировало более низкую эффективность ЦСЖ по сравнению с глициррамом, нормализовавшим структуру ГИМ.
СН — 0869-6047
УР — https://www.unboundmedicine.com/medline/citation/9846103/%5bmechanisms_of_hemopoiesis_cytostatic_damage_and_regeneration%5d_
L2 — https://medlineplus.gov/stemcells.
Показано, что цитостатические изменения в восстановлении кроветворения зависят в первую очередь от отношений пролиферации-дифференциации в кроветворных клетках, что, в свою очередь, определяется состоянием клеток ГИМ после цитостатического воздействия. Повышенная функциональная активность элементов ГИМ в ответ на повреждение кроветворной ткани, вызванное А или КФ, способствует быстрому восстановлению кроветворения, которое значительно ускоряется при использовании рекомбинантного колониестимулирующего фактора (КСФ) и, в меньшей степени, глициррама, растительного препарата.В то же время 5-ФУ, вызывая длительную гипоплазию костного мозга, нарушал функцию клеток микроокружения. Использование этой модели продемонстрировало более низкую эффективность ЦСЖ по сравнению с глициррамом, нормализовавшим структуру ГИМ.
СН — 0869-6047
УР — https://www.unboundmedicine.com/medline/citation/9846103/%5bmechanisms_of_hemopoiesis_cytostatic_damage_and_regeneration%5d_
L2 — https://medlineplus.gov/stemcells. html
ДБ — ПРАЙМ
ДП — Свободная медицина
Скорая помощь —
html
ДБ — ПРАЙМ
ДП — Свободная медицина
Скорая помощь —
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера для приема файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.

- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.

 р-ра д/в/в и п/к введения 1000 МЕ: фл. 1, 5 или 10 шт.
р-ра д/в/в и п/к введения 1000 МЕ: фл. 1, 5 или 10 шт. р-ра д/в/в и п/к введения 4000 МЕ: фл. 1, 5 или 10 шт.
р-ра д/в/в и п/к введения 4000 МЕ: фл. 1, 5 или 10 шт. 150 мг/10 мл: амп. 1 шт.
150 мг/10 мл: амп. 1 шт.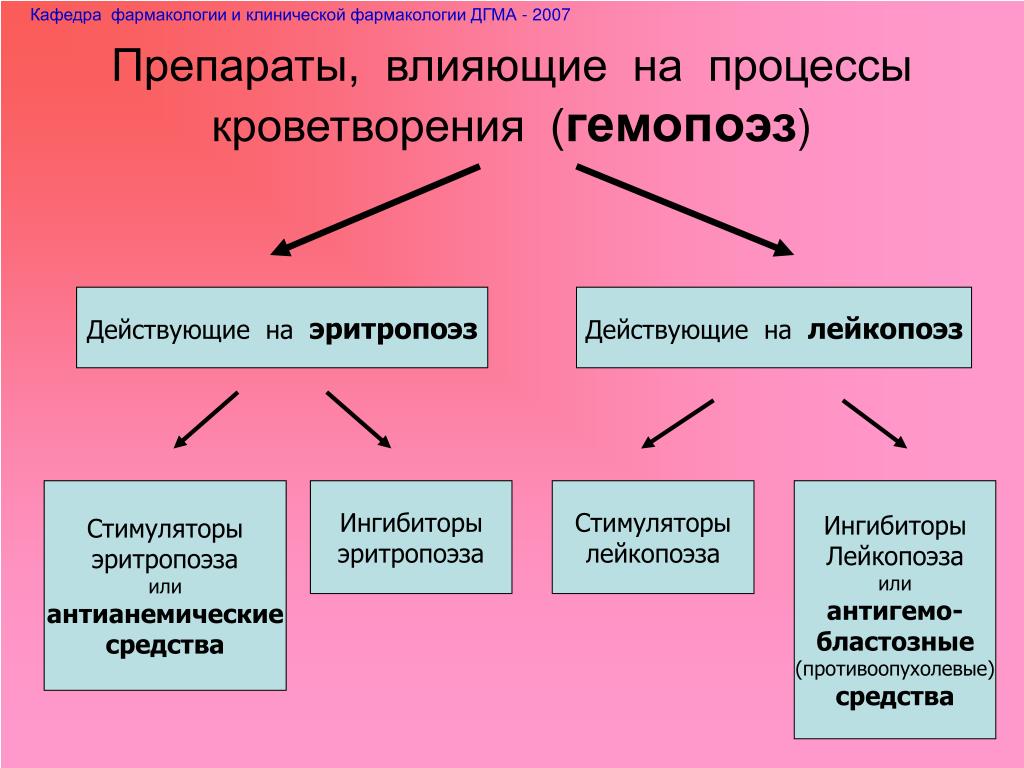 5 и 10 шт., флаконы 1 или 5 шт.
5 и 10 шт., флаконы 1 или 5 шт. 5 или 10 шт.
5 или 10 шт. 5 или 10 шт., флаконы 1 или 5 шт.
5 или 10 шт., флаконы 1 или 5 шт. 5 или 10 шт., флаконы 1 или 5 шт.
5 или 10 шт., флаконы 1 или 5 шт. 5 или 10 шт., 1 мл шприц 1, 5 или 6 шт.
5 или 10 шт., 1 мл шприц 1, 5 или 6 шт. 75 мг/5 мл: амп. 5 шт.
75 мг/5 мл: амп. 5 шт. , флаконы 50 шт.
, флаконы 50 шт. 10 000 МЕ/1 мл: амп. 5, 10, 50 или 100 шт., фл. 5, 10, 50 или 100 шт.
10 000 МЕ/1 мл: амп. 5, 10, 50 или 100 шт., фл. 5, 10, 50 или 100 шт. Антибиотики, аспирин, NSAIDS
Антибиотики, аспирин, NSAIDS