Расположение клеток кровь человека: Вид клеток и ядра (крови человека) Наличие межклеточного вещества (крови человека)
Вид клеток и ядра (крови человека) Наличие межклеточного вещества (крови человека)
Укажи соответствие между Классом животного и его признаками и запиши обозначающие их буквы (в алфавитном порядке, без пробелов): речной рак — ; пчела … — . Е — отделы тела: голова, грудь и брюшко. В — дышат при помощи жабр. П — имеют антеннальные железы. З — имеют 3 пары ходильных конечностей. К — дыхание трахейное. У — тело состоит из головогруди и брюшка.
до папоротей належитьа)щитник чоловічий б)спірогира в)зозулин льон
ПОМОГИТЕ СРОЧНО ДАЮ 15 БАЛЛОВ!!!!
Найцікавіший організм
Биология 15 баллов ПОМОГИТЕ пожалуйстаВопросы для самоконтроля:1. Выберите все правильные ответы.Плод у представителей семейства Крестоцветные:а) стру
… чокб) бобв) стручочекг) орешекд) семянкае) коробочка2. Выберите один правильный ответ.Плод у представителей семейства Сложноцветные:а) коробочкаб) орешекв) семянкаг) ягода.3. Выберите все правильные ответы.Представители семейства Розоцветные:а) черемухаб) полыньв) ромашкаг) клеверд) репае) вишня.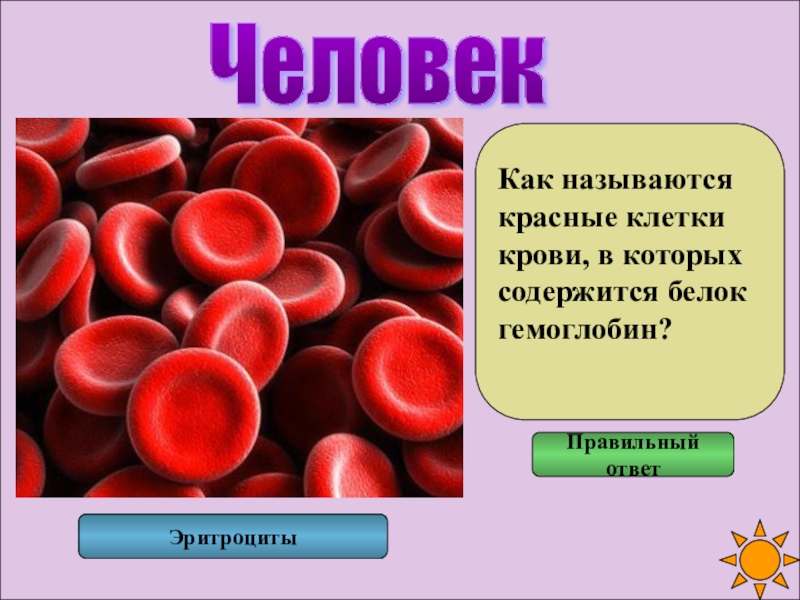
Культурные сообщества состоят в основном: А) из одинаковых растений, искусственно выведенных видов;Б) из природных сообществ, адаптированных к определ … енным условиям;В) из культурных растений и сорных трав;Г) из культурных растений и искусственных видов.
Характерные признаки сообществ:А) луга, пустыни, тундра;Б) состав, участие видов, время развития, доминирование видов, ярусность;В) индивидуальные изм … енения, приспособление к условиям среды;Г) сезонные изменения, вмешательство человека, климатические факторы
порівняти симбіоз і мутуалізм,срочно!!!!
Уяви, що ти кухар і ти помічаєш, що частина продуктів, що ти мав приготувати, покрита пліснявою. Чому неможна просто зрізати уражені частини з харчів … та використовувати неуражені?
1) Испуга.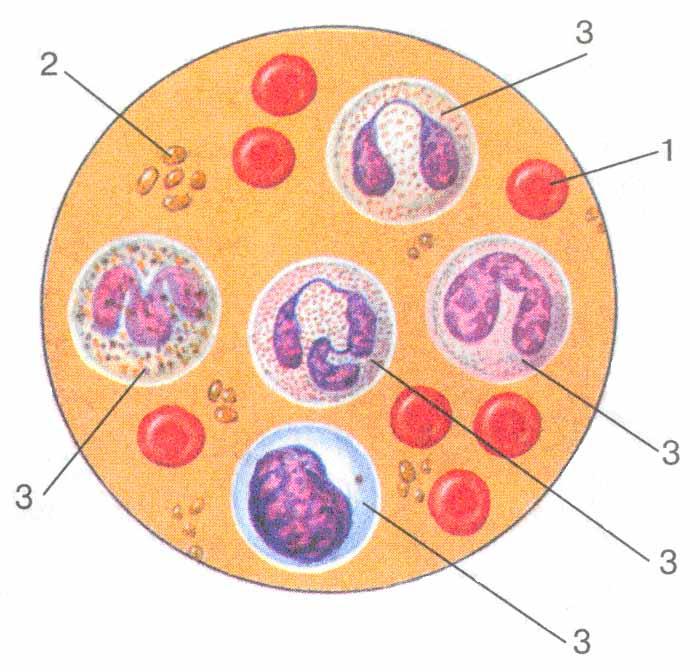 .ые кони ск..кали пр..жав уши храпяк..сясь на р..скаты грозы обг..нявшие коляску тосправа, то слева. (К. Паустовский) 2) Я стоял в степиподн
… яв голову и слушал песню ра(с, ссыпавшуюся снеба золотым дождём. (Д. Мамин-Сибиряк) 3) Там ли-пы в несколько обхватов спр..вляют в сумр..ке ал,ллей в..ршины друг от друга спрятав свой двухсот-летний юб..лей. (Б. Пастернак), 4) Как дымкой дальполей з..крыв на (пол) часа прошёл вн..запный дождьк..сыми пол..сами и снова гл..боко с..неют н..бесанад осв..жё..ыми лесами. (И. Бунин)
.ые кони ск..кали пр..жав уши храпяк..сясь на р..скаты грозы обг..нявшие коляску тосправа, то слева. (К. Паустовский) 2) Я стоял в степиподн
… яв голову и слушал песню ра(с, ссыпавшуюся снеба золотым дождём. (Д. Мамин-Сибиряк) 3) Там ли-пы в несколько обхватов спр..вляют в сумр..ке ал,ллей в..ршины друг от друга спрятав свой двухсот-летний юб..лей. (Б. Пастернак), 4) Как дымкой дальполей з..крыв на (пол) часа прошёл вн..запный дождьк..сыми пол..сами и снова гл..боко с..неют н..бесанад осв..жё..ыми лесами. (И. Бунин)
О чем расскажут клетки крови? — Статья педиатра Детской поликлиники Литфонда
В крови содержатся различные типы клеток, выполняющих совершенно разные функции – от переноса кислорода до выработки защитного иммунитета. Для того, чтобы понимать, изменения формулы крови при различных заболеваниях, необходимо знать, какие функции выполняет каждый тип клеток.
Некоторые из этих клеток никогда в норме не покидают кровеносное русло, другие же для исполнения своего предназначения выходят в другие ткани организма, в которых обнаруживается воспаление или повреждение.
Клетки крови можно разделить на красные и белые – эритроциты и лейкоциты. Эритроциты всю свою жизнь – около 120 дней – циркулируют по кровеносным сосудам и переносят кислород и углекислый газ. Эритроциты составляют основную массу клеток крови. В процессе своего созревания они узко специализируются для выполнения своей самой главной функции – снабжение тканей организма кислородом и удаление углекислого газа.
Для этого они теряют все «лишние» клеточные элементы, приобретают специальную вогнутую форму, позволяющую им проникать в самые мелкие и изогнутые капилляры, и заполняют свою цитоплазму молекулами гемоглобина, способного обратимо связывать кислород. При различных заболеваниях может изменяться как форма, размер, количество эритроцитов, так и уровень гемоглобина. Для постановки правильного диагноза иногда приходится проводить дополнительные тесты, позволяющие выявить нарушения в строении мембраны эритроцита или наличие патологических форм гемоглобина.
Лейкоциты – белые клетки крови – борются с инфекциями и переваривают остатки разрушенных клеток, выходя для этого через стенки небольших кровеносных сосудов в ткани. Лейкоциты делятся на три главные группы: гранулоциты, моноциты и лимфоциты.
Среди гранулоцитов есть нейтрофилы, эозинофилы и базофилы. Внутри гранулоцитов содержатся многочисленные пузырьки и гранулы с биологически-активным содержимым. Нейтрофилы захватывают, убивают и переваривают микроорганизмы бактерии. Базофилы выделяют гистамин, который вовлечен в реакции воспалительного ответа. Эозинофилы участвуют в разрушении паразитов и в аллергических реакциях.
Моноциты, вместе с нейтрофилами, являются главными «санитарами организма», так как их основная функция – удаление обломков старых, отживших, свое клеток, и инородных элементов. Для этого моноциты, выходя из кровеносного русла, становятся макрофагами, которые значительно больше по размерам и дольше живут, чем нейтрофилы.
Лимфоциты являются главными клетками, опосредующими иммунный ответ. Они представлены двумя главными классами:
- B-лимфоциты производят антитела,
- T-лимфоциты убивают клетки, инфицированные вирусом, и регулируют активность других лейкоцитов.
Кроме того, существуют лимфоциты – естественные (природные) киллеры, способные убивать опухолевые клетки.
Тромбоциты содержаться в крови в большом количестве. По своей сути, они не являются обычными целыми клетками, а представляют собой мелкие клеточные фрагменты, отделившиеся от гигантских клеток мегакариоцитов. Мегакариоциты не циркулируют в крови, а находятся в костном мозге, где от них и отделяются «клеточные пластинки» – тромбоциты. Тромбоциты способны прилипать к внутренней поверхности поврежденного сосуда, выступая в качестве организатора заплатки, помогая восстановить целостность сосудистой стенки в процессе свертывания крови.
Образование и созревание большинства клеток крови (гемопоэз) происходит у взрослого человека в костном мозге, где из уникальной стволовой клетки образуется все разнообразие кровяных клеток.
Запись на прием педиатра по телефону +7(495)150-60-03
Возврат к списку
Клетки крови человека под микроскопом
Назад к списку
Если вы рассмотрели все доступные предметы под микроскопом, то сейчас самое время усложнить технику наблюдения и расширить исследуемые объекты.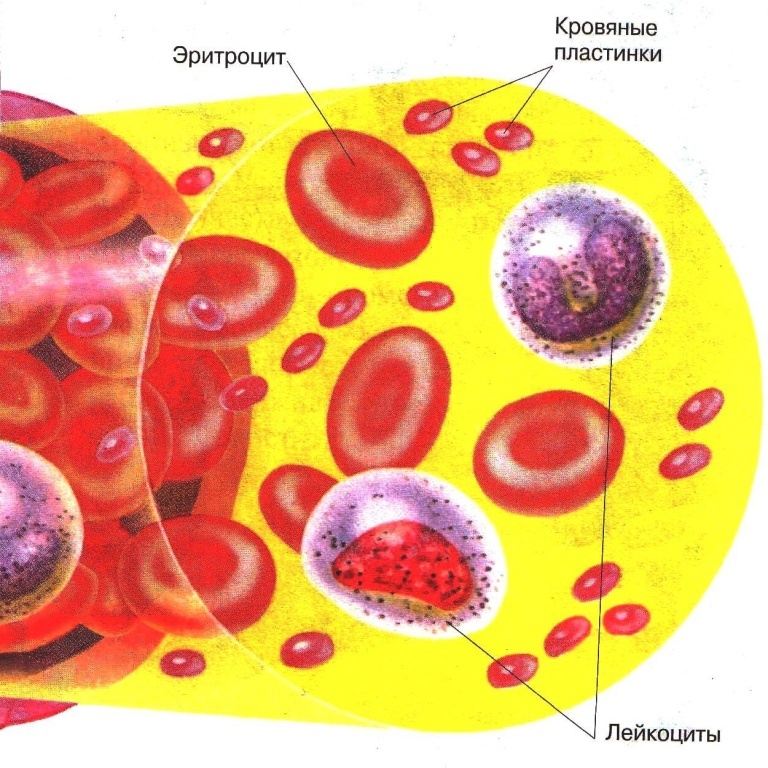 С помощью прибора можно заглянуть в ту часть природы, из которой состоим мы. Рассмотрим, как выглядят наши клетки крови под микроскопом.
С помощью прибора можно заглянуть в ту часть природы, из которой состоим мы. Рассмотрим, как выглядят наши клетки крови под микроскопом.
Оборудование
Чтобы исследовать кровь, используют разные методы окраски материала: по Романовскому-Гимзе (самый распространенный), по Маю-Грюнвальду, по Паппенгейму или по Райту. Окраска помогает выделить структуру клетки и способствует более детальному ее рассмотрению. Для этого нужно приобрести готовый красящий раствор или порошок, состоящий из азура и эозина. Они всегда есть в продаже в специализированных магазинах.
Исследуют кровь в домашних условиях с помощью светового микроскопа, используя разное увеличение. Например, при 150х можно рассмотреть множество мелких клеток.
При среднем увеличении от 400х – 600х различаются эритроциты и среди них лейкоциты.
Для более глубокого изучения используют увеличение от 1000х и более. В этом случае можно детально рассмотреть структуру каждой клетки.
В этом случае можно детально рассмотреть структуру каждой клетки.
Как выглядят клетки крови под микроскопом?
Наша кровь состоит из нескольких видов клеток, выполняющих три основные функции:
- доставляют кислород к органам и тканям;
- защищают от вредных микроорганизмов;
- поддерживают постоянную внутреннюю среду.
Эритроциты под микроскопом
Самая многочисленная группа круглых клеток —
Лейкоциты под микроскопом
Среди огромного количества эритроцитов вы увидите лейкоциты: лимфоциты, моноциты, базофилы, нейтрофилы и эозинофилы. Подробно их можно разглядеть при увеличении не менее 1000х. Лейкоциты защищают организм человека от различных заболеваний, вызванных вирусами, бактериями, грибками. В борьбе с ними многие лейкоциты погибают.
Лейкоциты защищают организм человека от различных заболеваний, вызванных вирусами, бактериями, грибками. В борьбе с ними многие лейкоциты погибают.
Малый лимфоцит
Средний лимфоцит
Моноцит
Базофил
Сегментоядерный нейтрофил
Эозинофил
Тромбоциты под микроскопом
Тромбоциты отвечают за свертываемость крови. Это очень маленькие круглые клетки. Если у вас профессиональный микроскоп с увеличением больше 1000х, то вы их точно увидите.
Мы предоставили небольшой материал о том, как выглядят клетки крови человека под микроскопом с фото, но настоящее исследование с использованием собственного прибора этого не заменит. Если микроскопия станет вашим хобби, то вы откроете для себя потрясающие вещи! Например, вы когда-нибудь задумывались над тем, почему СОЭ (скорость оседания эритроцитов) выше нормы у больного человека? Рассмотрите воспаленную кровь и найдете ответ! Сколько удивительных открытий можно сделать прямо сейчас!
Здесь даже не нужно покупать очень сложное и дорогостоящее оборудование (пусть этим занимаются лаборатории!), но стоит задуматься о приобретении доступной оптической техники среднего класса.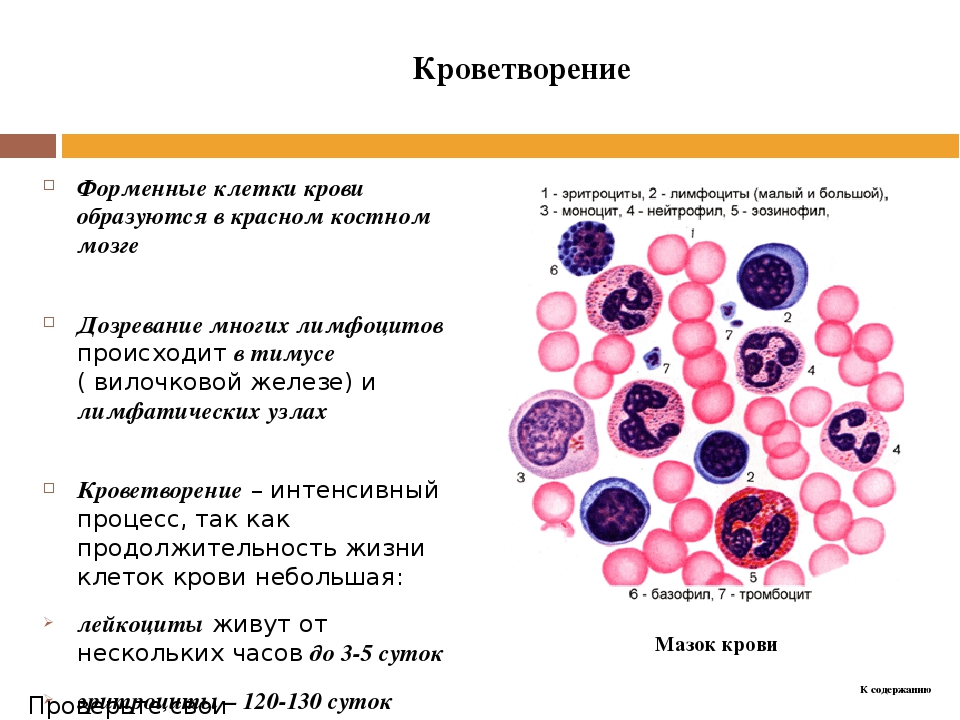 Такая покупка даст потрясающую возможность открыть для себя тайны микромира, не доступного нашему глазу!
Такая покупка даст потрясающую возможность открыть для себя тайны микромира, не доступного нашему глазу!
Предлагаем вашему вниманию микроскопы интернет-магазина Veber.ru, с помощью которых вы сможете изучить клетки крови в мельчайших подробностях:
Назад к списку
Выращивание клеток крови поставили на поток
Wellcome Images / flickr.com
Биологи придумали способ получать жизнеспособные эритроциты in vitro в количествах, пригодных для клинического применения. Для этого они создали «бессмертную» линию клеток-предшественников эритроцитов. Статья опубликована в журнале Nature Communications.
Для этого они создали «бессмертную» линию клеток-предшественников эритроцитов. Статья опубликована в журнале Nature Communications.
Ранее красные кровяные клетки пытались получать, дифференцируя стволовые клетки, полученные от доноров. Такие клетки плюрипотентны (способны дифференцироваться в любой тип клеток организма), поэтому для получения именно эритроцитов необходимо прибегать к сложным манипуляциям. Такой способ работает, но дает небольшое количество клеток, из-за чего приходится брать у доноров кровь много раз.
Другой подход заключается в том, что бы использовать не плюрипотентные клетки, а унипотентные — способные дифференцироваться только в один тип клеток. Если культивировать унипотентные предшественники эритроцитов, можно не заботиться о контроле их дифференцировки. Однако в отличие от стволовых, количество делений таких клеток ограничено, поэтому их необходимо иммортализовать — модифицировать так, чтобы они делились бесконечно.
Этим подходом и занялись ученые из Бристольского университета. Они взяли клетки костного мозга и генетически модифицировали их, добавив гены папилломавируса человека, которые позволяют клетке делиться неограниченно. Затем авторы работы индуцировали переход клеток в предшественники эритроцитов. Ход дифференцировки новой клеточной линии, названной BEL-A (Bristol Erythroid Line Adult), не отличается от соответствующих стадий развития плюрипотентных клеток. Отличий в морфологии эритроцитов также не обнаружено.
Они взяли клетки костного мозга и генетически модифицировали их, добавив гены папилломавируса человека, которые позволяют клетке делиться неограниченно. Затем авторы работы индуцировали переход клеток в предшественники эритроцитов. Ход дифференцировки новой клеточной линии, названной BEL-A (Bristol Erythroid Line Adult), не отличается от соответствующих стадий развития плюрипотентных клеток. Отличий в морфологии эритроцитов также не обнаружено.
Если клинические испытания пройдут успешно, то выращенные эритроциты станут ценным материалом для переливаний. Это снизит риск передачи инфекционных заболеваний, а также поможет в первую очередь больным с редкими группами крови. Линии иммортализованных предшественников могут быть созданы для любой группы крови.
Анна Образцова
Что такое стволовые клетки?
Стволовые клетки способны становится любой клеткой в теле (организме). Одной из их главных особенностей является их способность к самообновлению или увеличению количества в организме. Стволовые клетки могут становиться клетками крови, сердечной ткани, кожи, мускулов, мозга и т.д.
Одной из их главных особенностей является их способность к самообновлению или увеличению количества в организме. Стволовые клетки могут становиться клетками крови, сердечной ткани, кожи, мускулов, мозга и т.д.Есть разные стволовые клетки, но все их виды имеют способность превращаться в разные виды клеток.
Вид стволовых клеток которыми богата пуповина такой же как и костный мозг. Этот тип клеток дает рост всем кровяным клеткам и является фундаментом нашей иммунной системы.
Красные кровяные тельца поставляют кислород.
Белые кровяные тельца борются с инфекциями.
Тромбоциты обеспечивают заживление тканей.
Пуповинная кровь остается в вене во время родов. Она богата стволовыми клетками и ее сохраняют для последующих медицинских нужд. Эти клетки способны лечить более 80 заболеваний и уже были использованы в качестве 30000 трансплантаций по всему миру.
Преимущества стволовых клеток из пуповинной крови
Стволовые клетки из пуповинной крови имеют огромное преимущество перед другими клетками (например по сравнению со стволовыми клетками из костной ткани):- Легко собирать.

- При заборе нет риска ни для матери, ни для ребенка.
- Они легче приживаются в организме.
- Снижают риск отторжения при пересадке ребенку и лучше приживаются при пересадке близким родственникам.
- Снижается риск заражения при пересадке.
- Способны преодолевать гематоэнцефалический барьер и дифференцироваться в нейроны и другие клетки головного мозга, которые могут играть важную роль при лечении некоторых заболеваний мозга.
Вышеуказанная 5 характеристика является причиной, почему стволовые пуповинной крови клетки окрестили «привилегированные», потому что они еще не подвержены воздействию большинства заболеваний и загрязнений окружающей средой, что лучше использовать при трансплантации , по сравнению со стволовыми клетками из костной ткани взрослого человека.
Наиболее важно и то, что эти клетки идеально подходят для пересадки именно Вашему ребенку и подходят его ближайшим родственникам в соотношении 1 к 4 (25%). Еще очень важно заметить, что идеальное совпадение не гарантирует, что они будут полезны при лечении всех заболеваний.
Вирус Трансплантат против хозяина (РТПХ), может возникать непредсказуемо, когда клетки донора начинают атаковать получателя трансплантата и это может быть смертельным, по разным оценкам, это происходит в 60-80 процентов трансплантаций, где донор и реципиент не являются родственниками.
Про стволовые клетки из пуповинной ткани.
Пуповинная ткань сама по себе — это богатый источник стволовых клеток называемых мезенхимальными. У мезенхимальных стволовых клеток есть много уникальных функций, включая способность ингибировать воспаление после повреждения ткани, секретировать факторы роста, которые способствуют репарации тканей, а также дифференцироваться во многие другие типы клеток, включая нервные клетки, костные клетки, жировые клетки и хрящи. Мезенхимальные стволовые клетки все чаще используются в регенеративной медицине для широкого диапазона применений, включая болезни сердца и почек, ALS, заживление ран и лечении аутоиммунных заболеваний.
Мезенхимальные стволовые клетки все чаще используются в регенеративной медицине для широкого диапазона применений, включая болезни сердца и почек, ALS, заживление ран и лечении аутоиммунных заболеваний.
Вся информация, представленная на сайте на русском языке, носит справочный характер и не может быть использована в медицинских или иных целях
Показатели клинического анализа крови — Лаборатория KDL
Гемоглобин (Hb)– один из главных показателей общего анализа крови. Снижение концентрации гемоглобина довольно частое явление, которое можно встретить в любом возрасте. Именно гемоглобин придает крови такой красный цвет. А необходим он нам для доставки кислорода из легких в наши органы – мозг, сердце, мышцы и другие. Поэтому, если у вас есть одышка уже при незначительной физической нагрузке, постоянная слабость, апатия — стоит обратить внимание именно на этот на показатель. В последнее время врачи рекомендуют думать о возможной анемии уже при гемоглобине ниже 120 г/л у женщин, а у мужчин ниже 130 г/л.
Эритроциты (RBC) – показатель числа эритроцитов, измеряется в количестве клеток на литр крови. Это самый многочисленный тип клеток. Главная задача эритроцитов — нести в себе гемоглобин. Если снижается количество эритроцитов, например, из-за дефицита витамина В12 или фолиевой кислоты (а именно эти витамины нужны для синтеза этих клеток), то гемоглобина в крови также будет не хватать, даже при хорошем запасе железа (ферритина).
Гематокрит (HCT) — объем всех клеток крови, % объемного содержания клеток в крови. При повышении гематокрита за черту 50% риск тромбоза из-за сгущения крови возрастает. В гематологических анализаторах это расчетный показатель т.е. прямым образом на него влияют количество эритроцитов и их средний объем.
Средний объем эритроцитов (MCV) — MCV может быть низким (при микроцитарной анемии), нормальным (при нормоцитарной анемии) или высоким (при макроцитарной анемии). Маленькие эритроциты (микроцитоз) – является распространенным лабораторным нарушением, которое является классическим признаком дефицита железа или талассемии. По мере прогрессирования анемии новые эритроциты становятся все меньше и меньше, поэтому показатель MCV может служить маркером давности анемии. При ранней железодефицитной анемии MCV может быть нормальным, поскольку измеренное MCV отражает объем клеток, продуцированных за предшествующие 120 дней (срок жизни эритроцитов). Для диагностики скрытого дефицита железа врач может назначить вам анализ на ферритин. Анемия возникает, так как без молекулы железа костный мозг не может построить молекулу гемоглобина.
Маленькие эритроциты (микроцитоз) – является распространенным лабораторным нарушением, которое является классическим признаком дефицита железа или талассемии. По мере прогрессирования анемии новые эритроциты становятся все меньше и меньше, поэтому показатель MCV может служить маркером давности анемии. При ранней железодефицитной анемии MCV может быть нормальным, поскольку измеренное MCV отражает объем клеток, продуцированных за предшествующие 120 дней (срок жизни эритроцитов). Для диагностики скрытого дефицита железа врач может назначить вам анализ на ферритин. Анемия возникает, так как без молекулы железа костный мозг не может построить молекулу гемоглобина.
Среднее содержание гемоглобина в эритроците (MCH) –довольно стабильная величина, которая не зависит от возраста. Этот индекс пришел на смену устаревшему цветовому показателю (ЦП). Снижение MCH также говорит о нехватке железа. Повышение может быть признаком гиперхромной анемии.
Средняя концентрация гемоглобина в эритроците (MCHC).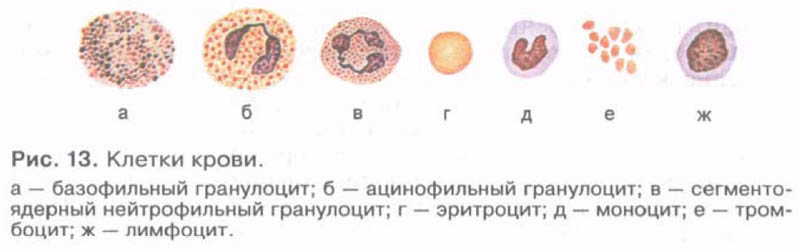 Повышение MCHC при сниженном MCV может предполагать наследственный микросфероцитоз – заболевание при котором наблюдается повышенное разрушение эритроцитов и может быть желтушность.
Повышение MCHC при сниженном MCV может предполагать наследственный микросфероцитоз – заболевание при котором наблюдается повышенное разрушение эритроцитов и может быть желтушность.
Ширина распределения эритроцитов по объему (RDW) — показатель анизоцитоза (разного размера эритроцитов). До появления гематологических анализаторов гетерогенность размера эритроцитов исторически определялась качественным исследованием мазков периферической крови. RDW указывает насколько сильно эритроциты различаются по размеру. Увеличивается при дефиците железа, фолиевой кислоты или витамина В12.
Тромбоциты (PLT) — самые маленькие клетки крови, но не менее важные чем эритроциты и лейкоциты. Необходимы они нам для свертывания крови. При их снижении в анализе ниже 30 самопроизвольно появляются на коже синяки, так проявляется повышенная кровоточивость. При повышении количества тромбоцитов в первую очередь надо исключать железодефицитную анемию и воспалительную реакцию (сделать анализ на С-реактивный белок).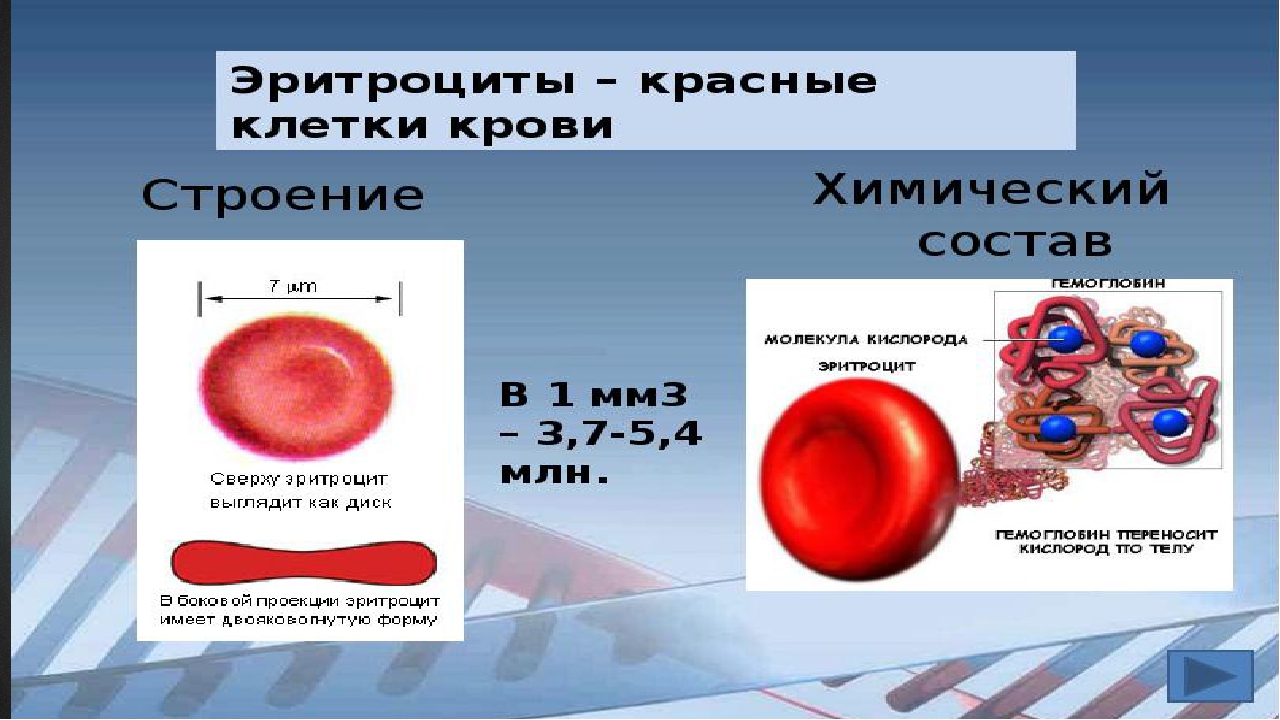
MPV – средний объем тромбоцитов. Значение MPV повышается в период активного производства тромбоцитов. А уменьшение объема тромбоцитов говорит о возможных проблемах с костным мозгом. На показатель MPV стоит обращать внимание только при снижении количества тромбоцитов и отсутствии агрегации.
PCT – тромбокрит, или % объема всех тромбоцитов в крови. Чем выше тромбокрит, тем больше риск тромбоза.
PDW — ширина распределения тромбоцитов по объему. PDW также как и MPV используется для диагностики причины снижения тромбоцитов.
Лейкоциты – самый главный показатель нашей иммунной системы. Снижение числа лейкоцитов может быть связано с вирусными инфекциями, токсическим воздействием на организм, приемом некоторых лекарств. Увеличение количества лейкоцитов может говорить об воспалительной реакции, острой инфекции, лейкозе. В этом случае особое внимание нужно обратить на лейкоцитарную формулу, то есть сделать клинический анализ крови с лейкоформулой.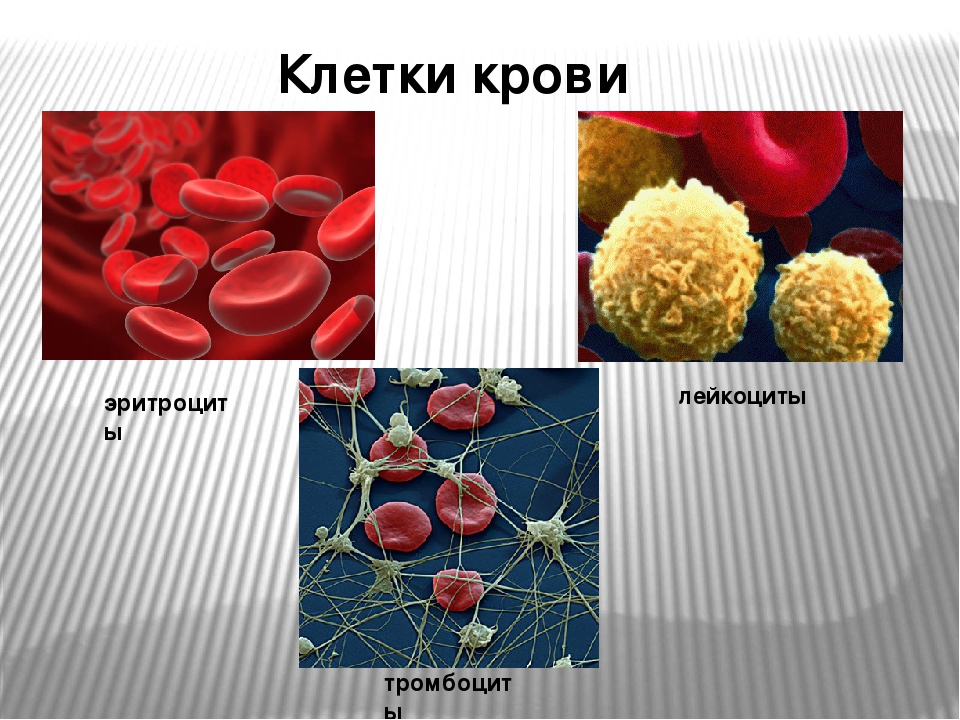
Поделиться статьей:
Остались вопросы?Разделение частиц методом центрифугирования — Beckman Coulter
Центрифугирование позволяет не только значительно ускорить процесс осаждения, но и разделить суспензию частиц на фракции в зависимости от их размера, плотности и коэффициента седиментации.
Разделение осаждением
Поле центробежных сил можно использовать для разделения частиц, входящих в состав смеси, – например, клеток в составе крови.
Кровь состоит из плазмы (которая представляет собой водный раствор большого количества компонентов) и нескольких типов суспендированных частиц: эритроцитов, лейкоцитов и тромбоцитов.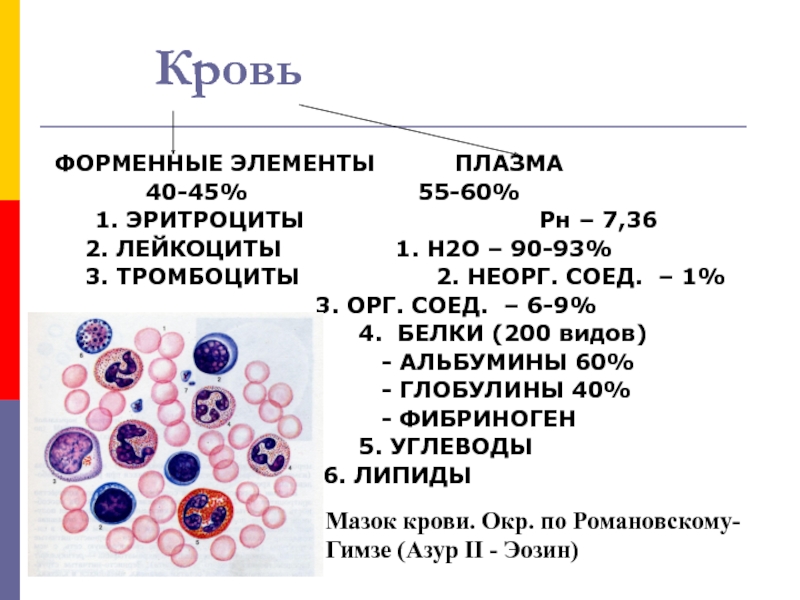 Эти клетки – относительно большие биологические объекты, и они достаточно велики для того, чтобы за ночь при условии отсутствия тромбообразования отделиться от плазмы и осесть под действием одной лишь силы тяжести Земли. Но процесс осаждения можно ускорить: если центрифугировать кровь при 1 500 х g, то разделение клеток и плазмы произойдет за 10 мин.
Эти клетки – относительно большие биологические объекты, и они достаточно велики для того, чтобы за ночь при условии отсутствия тромбообразования отделиться от плазмы и осесть под действием одной лишь силы тяжести Земли. Но процесс осаждения можно ускорить: если центрифугировать кровь при 1 500 х g, то разделение клеток и плазмы произойдет за 10 мин.
Почему в центробежном поле это происходит так быстро? Потому что сила, которая перемещает каждую клетку от центра вращения к периферии, во много раз больше (в 1 500 раз в примере выше) ее собственного веса в нормальном гравитационном поле Земли.
Все клетки оседают по-разному: крупные быстрее мелких. Поэтому клетки, у которых имеется достаточная разница в размере и скорости седиментации, можно отделить друг от друга.
Например, тромбоциты намного меньше эритроцитов и лейкоцитов, поэтому их можно отделить от этих клеток крови. Все, что для этого нужно, – выбрать правильную комбинацию относительного центробежного ускорения (RCF) и времени центрифугирования.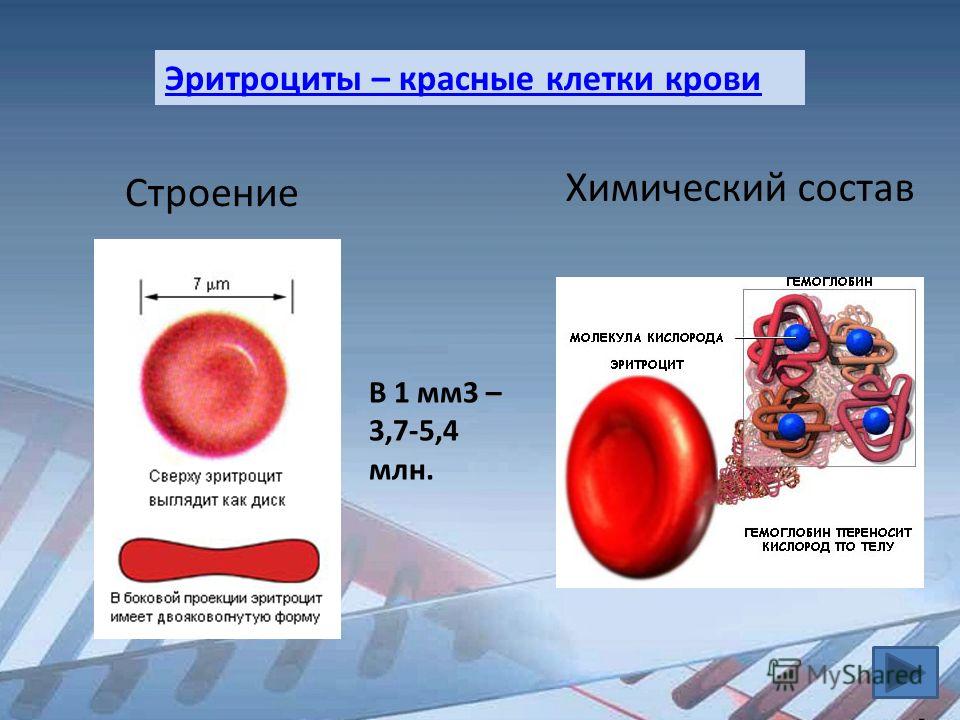 Если центрифугировать кровь при 2 900 х g всего 3 минуты, тромбоциты, в отличие от крупных клеток, не успеют осесть на дно, и их можно будет собрать из верхней фракции, которая будет представлять собой обогащенную тромбоцитами плазму.
Если центрифугировать кровь при 2 900 х g всего 3 минуты, тромбоциты, в отличие от крупных клеток, не успеют осесть на дно, и их можно будет собрать из верхней фракции, которая будет представлять собой обогащенную тромбоцитами плазму.
На дне пробирки или контейнера в результате центрифугирования образуется осадок или седимент частиц. Жидкость над осадком называется супернатантом. Из него можно собрать достаточно чистую фракцию самых маленьких частиц (см. рис.). При этом осадок из более крупных частиц всегда будет содержать самые мелкие частицы, которые находились на дне пробирки еще до начала центрифугирования. Варьируя скорость и время центрифугирования, можно разделить и собрать из смеси частицы разных размеров. Этот метод называется «дифференциальным центрифугированием».
Осаждение частиц в поле центробежных сил
Разделение по плотности
Плотность – еще одна физическая характеристика частиц и клеток, которую можно использовать с целью их разделения.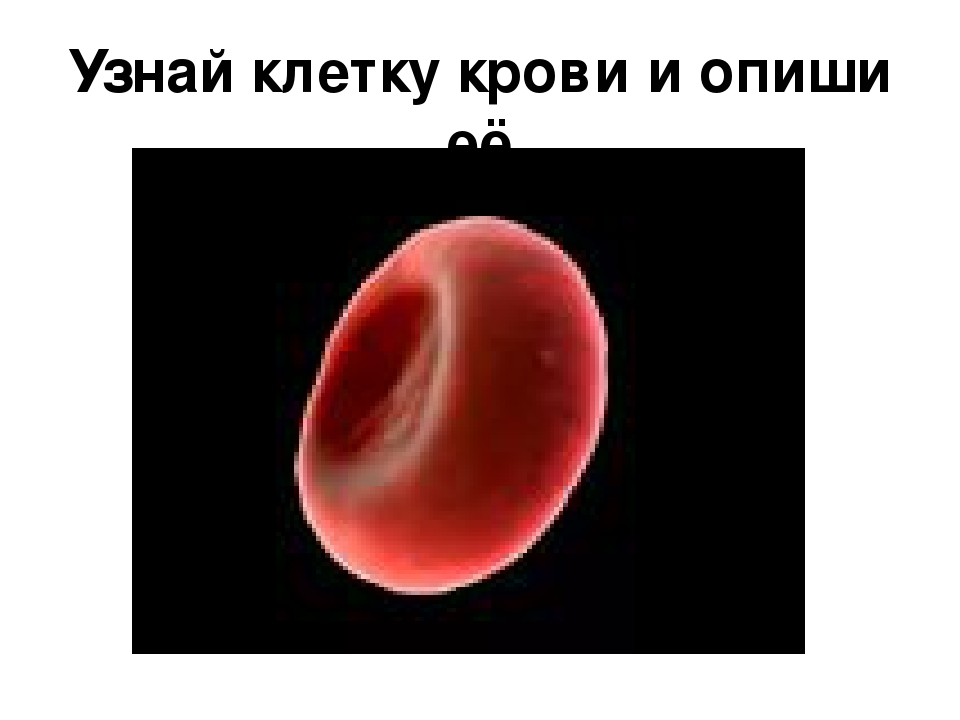
Давайте сравним яблоко и камень, имеющие одинаковые размеры и форму. В воде такой камень будет тонуть, а фрукт – плавать. Единица объема камня имеет гораздо большую массу, чем единица объема яблока. Если сказать по-другому, плотность камня выше плотности яблока. Плотность выражается в единицах массы, приходящейся на единицу объема, например, в граммах на миллилитры (г/мл). Плотность воды равна 1 г/мл.
Центробежные силы способны разделить частицы, даже слабо отличающиеся по плотности. Все, что для этого нужно, — подобрать плотность жидкости, в которой будет происходить осаждение таким образом, чтобы менее плотные частицы в ней всплывали, а более плотные – тонули.
Такой метод часто используется для отделения лимфоцитов (разновидность лейкоцитов). Они схожи по размерам с клетками крови других типов и поэтому не могут быть отделены обычным методом осаждения. Однако плотность лимфоцитов ниже, чем у других клеток. Если образец крови нанести поверх жидкости с плотностью 1 077 г/мл, а затем центрифугировать, то лимфоциты сформируют плавучий бэнд, отделенный от большинства других белых и красных клеток, которые, имея плотность выше 1 077 г/мл, сформируют осадок на дне пробирки.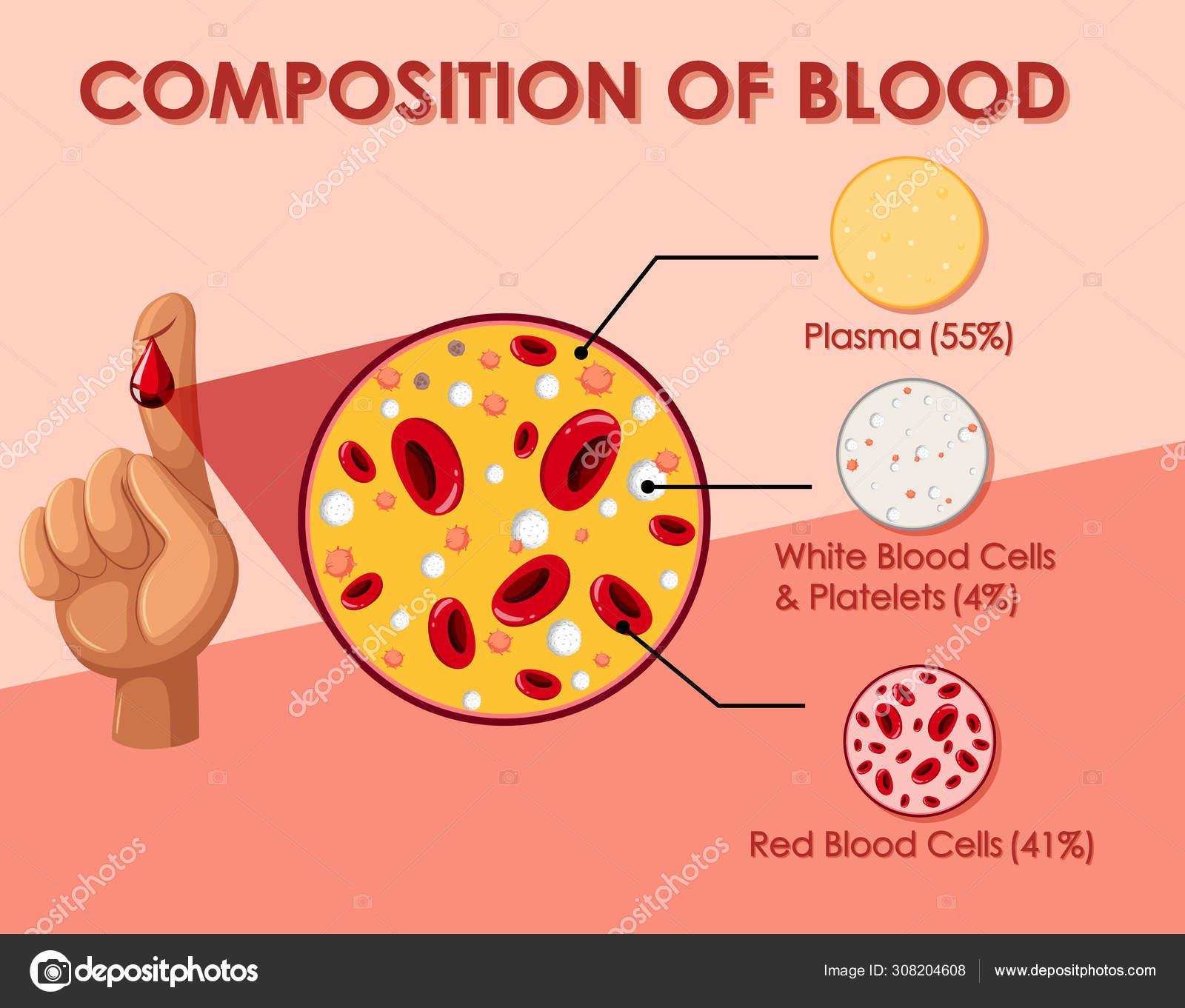 Плазма и тромбоциты, имеющие самую низкую плотность, переместятся в верхнюю часть пробирки, как показано на рисунке.
Плазма и тромбоциты, имеющие самую низкую плотность, переместятся в верхнюю часть пробирки, как показано на рисунке.
Разделение лимфоцитов по плотности: слева – пробирка до центрифугирования, справа – пробирка после центрифугирования
Образованиеклеток крови | Описание, процесс и типы клеток крови
Образование клеток крови , также называемое гематопоэз или гематопоэз , непрерывный процесс, при котором клеточные компоненты крови пополняются по мере необходимости. Клетки крови делятся на три группы: красные кровяные тельца (эритроциты), белые кровяные тельца (лейкоциты) и тромбоциты крови (тромбоциты). Лейкоциты подразделяются на три большие группы: гранулоциты, лимфоциты и моноциты.
Подробнее по этой теме
кровь: клетки крови
В кроветворной ткани происходит непрерывный процесс образования клеток крови (кроветворения). В развивающемся эмбрионе первые …
В развивающемся эмбрионе первые …
Клетки крови образуются не в самом кровотоке, а в определенных кроветворных органах, особенно в костном мозге определенных костей. У взрослого человека костный мозг производит все эритроциты, 60–70 процентов лейкоцитов (т.е.е. гранулоциты) и все тромбоциты. Лимфатические ткани, особенно тимус, селезенка и лимфатические узлы, производят лимфоциты (составляющие 20–30 процентов белых клеток). Ретикулоэндотелиальные ткани селезенки, печени, лимфатических узлов и других органов продуцируют моноциты (4-8 процентов лейкоцитов). Тромбоциты, которые представляют собой небольшие клеточные фрагменты, а не полные клетки, образуются из кусочков цитоплазмы гигантских клеток (мегакариоцитов) костного мозга.
Мазок костного мозга с миелоцитамиМазок костного мозга показывает скопление эритроидных клеток (A), нейтрофильных миелоцитов (B и C) и ранние нейтрофильные метамиелоциты (D).
Unifformed Services University of the Health Sciences (USUHS) В человеческом эмбрионе первым местом кроветворения является желточный мешок. Позднее в эмбриональном периоде печень становится наиболее важным органом, формирующим эритроциты, но вскоре на смену ей приходит костный мозг, который во взрослой жизни является единственным источником как эритроцитов, так и гранулоцитов.И красные, и белые кровяные тельца возникают в результате серии сложных, постепенных и последовательных превращений из примитивных стволовых клеток, которые обладают способностью образовывать любой из предшественников клетки крови. Клетки-предшественники — это стволовые клетки, которые достигли той стадии, когда они готовы к формированию определенного вида новых клеток крови.
Позднее в эмбриональном периоде печень становится наиболее важным органом, формирующим эритроциты, но вскоре на смену ей приходит костный мозг, который во взрослой жизни является единственным источником как эритроцитов, так и гранулоцитов.И красные, и белые кровяные тельца возникают в результате серии сложных, постепенных и последовательных превращений из примитивных стволовых клеток, которые обладают способностью образовывать любой из предшественников клетки крови. Клетки-предшественники — это стволовые клетки, которые достигли той стадии, когда они готовы к формированию определенного вида новых клеток крови.
Микрофотография круглой агрегации тромбоцитов (увеличение в 1000 раз).
Д-р Ф. Гилберт / Центры по контролю и профилактике заболеваний (CDC) (Номер изображения: 6645) У нормального взрослого человека в костном мозге вырабатываются эритроциты около полулитра (почти одной пинты) крови. каждую неделю.Ежедневно вырабатывается почти 1 процент эритроцитов в организме, и точно поддерживается баланс между производством эритроцитов и удалением стареющих эритроцитов из кровообращения. Скорость образования клеток крови варьируется в зависимости от человека, но типичное производство может составлять в среднем 200 миллиардов эритроцитов в день, 10 миллиардов лейкоцитов в день и 400 миллиардов тромбоцитов в день.
Скорость образования клеток крови варьируется в зависимости от человека, но типичное производство может составлять в среднем 200 миллиардов эритроцитов в день, 10 миллиардов лейкоцитов в день и 400 миллиардов тромбоцитов в день.
Структура и функции крови
Опишите структуру и функцию крови в организме
Кровь важна для регулирования pH тела, температуры, осмотического давления, циркуляции питательных веществ и удаления отходов, распределения гормонов из эндокринных желез и устранения избыточного тепла; он также содержит компоненты для свертывания крови.Кровь состоит из нескольких компонентов, включая эритроциты, лейкоциты, тромбоциты и плазму, которая содержит факторы свертывания и сыворотку.
Цели обучения
- Определить роль крови в организме
- Сравните красные и белые кровяные тельца
- Опишите основные компоненты крови
Роль крови в организме
Кровь, как и человеческая кровь, показанная на рисунке 1, важна для регуляции систем организма и гомеостаза. Кровь помогает поддерживать гомеостаз, стабилизируя pH, температуру, осмотическое давление и устраняя избыточное тепло. Кровь поддерживает рост, распределяя питательные вещества и гормоны, а также удаляя отходы. Красные кровяные тельца содержат гемоглобин, связывающий кислород. Эти клетки доставляют кислород клеткам и удаляют углекислый газ.
Кровь помогает поддерживать гомеостаз, стабилизируя pH, температуру, осмотическое давление и устраняя избыточное тепло. Кровь поддерживает рост, распределяя питательные вещества и гормоны, а также удаляя отходы. Красные кровяные тельца содержат гемоглобин, связывающий кислород. Эти клетки доставляют кислород клеткам и удаляют углекислый газ.
Кровь играет защитную роль, транспортируя факторы свертывания и тромбоцитов. предотвращает потерю крови после травмы. Кровь также переносит агентов борьбы с болезнями, лейкоцитов к местам заражения.Эти клетки, включая нейтрофилы, моноциты, лимфоциты, эозинофилы и базофилы, участвуют в иммунном ответе.
Рис. 1. Показаны клетки и клеточные компоненты крови человека.
Красные кровяные тельца
Красные кровяные тельца , или эритроциты ( erythro — = «красный»; — cyte = «клетка»), представляют собой специализированные клетки, которые циркулируют по телу, доставляя кислород к клеткам; они образуются из стволовых клеток костного мозга.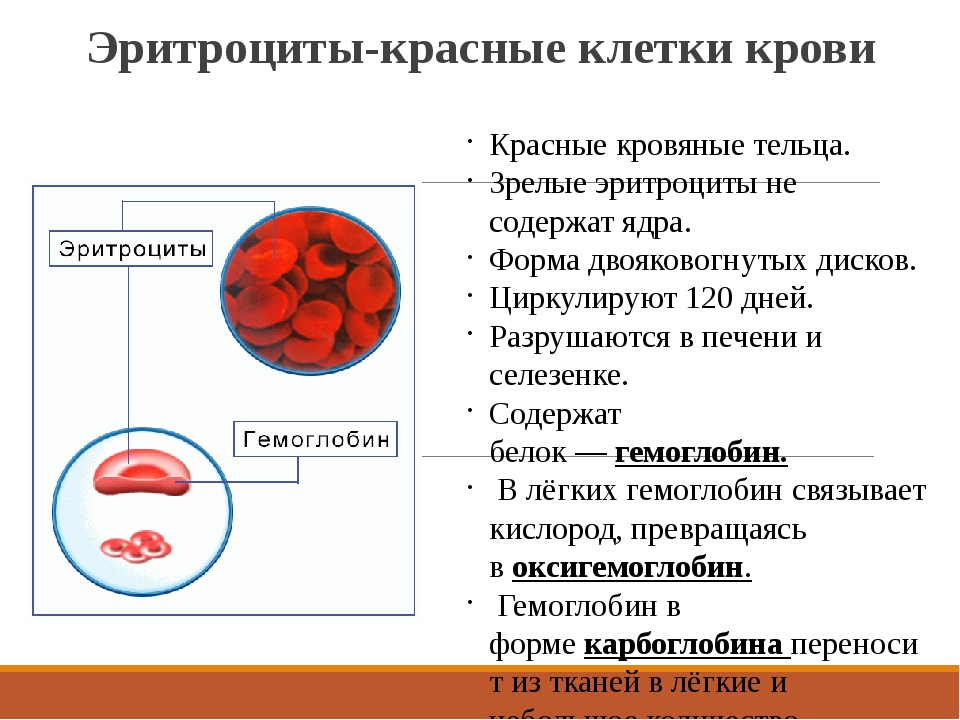 У млекопитающих эритроциты представляют собой небольшие двояковогнутые клетки, которые в зрелом возрасте не содержат ядра или митохондрий и имеют размер всего 7-8 мкм.У птиц и нептичьих рептилий ядро все еще сохраняется в красных кровяных тельцах.
У млекопитающих эритроциты представляют собой небольшие двояковогнутые клетки, которые в зрелом возрасте не содержат ядра или митохондрий и имеют размер всего 7-8 мкм.У птиц и нептичьих рептилий ядро все еще сохраняется в красных кровяных тельцах.
Красный цвет крови обусловлен железосодержащим белком гемоглобином, как показано на рисунке 2а. Основная задача этого белка — переносить кислород, но он также переносит и углекислый газ. Гемоглобин упакован в красные кровяные тельца из расчета около 250 миллионов молекул гемоглобина на клетку. Каждая молекула гемоглобина связывает четыре молекулы кислорода, так что каждый эритроцит несет один миллиард молекул кислорода.В пяти литрах крови человеческого тела содержится примерно 25 триллионов эритроцитов, которые могут нести до 25 секстиллионов (25 × 10 21 ) молекул кислорода в организме в любое время. У млекопитающих недостаток органелл в эритроцитах оставляет больше места для молекул гемоглобина, а недостаток митохондрий также препятствует использованию кислорода для метаболического дыхания.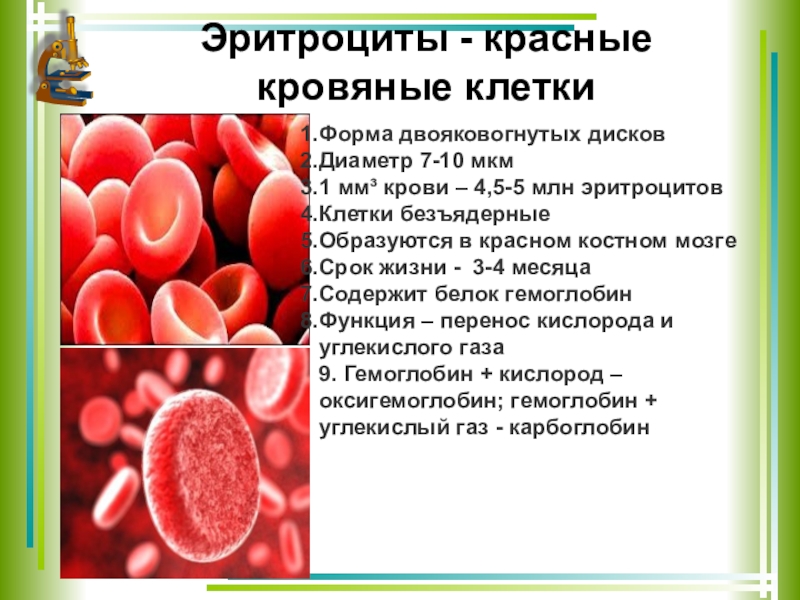 Только у млекопитающих есть безъядерные эритроциты, а у некоторых млекопитающих (например, верблюды) даже есть ядерные эритроциты.Преимущество ядерных эритроцитов в том, что эти клетки могут подвергаться митозу. Безъядерные эритроциты метаболизируются анаэробно (без кислорода), используя примитивный метаболический путь для производства АТФ и повышения эффективности транспорта кислорода.
Только у млекопитающих есть безъядерные эритроциты, а у некоторых млекопитающих (например, верблюды) даже есть ядерные эритроциты.Преимущество ядерных эритроцитов в том, что эти клетки могут подвергаться митозу. Безъядерные эритроциты метаболизируются анаэробно (без кислорода), используя примитивный метаболический путь для производства АТФ и повышения эффективности транспорта кислорода.
Не все организмы используют гемоглобин как средство переноса кислорода. Беспозвоночные, которые используют гемолимфу, а не кровь, используют разные пигменты для связывания с кислородом. Эти пигменты используют медь или железо для кислорода. У беспозвоночных есть множество других респираторных пигментов.Гемоцианин, сине-зеленый медьсодержащий белок, показанный на рисунке 2b, обнаружен у моллюсков, ракообразных и некоторых членистоногих. Хлорокруорин, железосодержащий пигмент зеленого цвета, встречается у четырех семейств полихет трубчатых червей. Гемеритрин, красный железосодержащий белок, обнаруженный у некоторых многощетинковых червей и кольчатых червей, показан на рисунке 2c. Несмотря на название, гемеритрин не содержит гемовой группы, и его способность переносить кислород мала по сравнению с гемоглобином.
Несмотря на название, гемеритрин не содержит гемовой группы, и его способность переносить кислород мала по сравнению с гемоглобином.
Рисунок 2.У большинства позвоночных (а) гемоглобин доставляет кислород в организм и удаляет некоторое количество углекислого газа. Гемоглобин состоит из четырех белковых субъединиц, двух альфа-цепей и двух бета-цепей, а также группы гема, с которой связано железо. Железо обратимо связывается с кислородом и при этом окисляется от Fe 2+ до Fe 3+ . У большинства моллюсков и некоторых членистоногих (б) гемоцианин доставляет кислород. В отличие от гемоглобина, гемолимфа не переносится клетками крови, а свободно плавает в гемолимфе.Медь вместо железа связывает кислород, придавая гемолимфе сине-зеленый цвет. У кольчатых червей, таких как дождевые черви и некоторых других беспозвоночных, (c) гемеритрин переносит кислород. Подобно гемоглобину, гемеритрин переносится в клетки крови и имеет связанное с ним железо, но, несмотря на свое название, гемеритрин не содержит гема.
Небольшой размер и большая площадь поверхности красных кровяных телец обеспечивают быструю диффузию кислорода и углекислого газа через плазматическую мембрану. В легких выделяется углекислый газ, а кровь забирает кислород.В тканях кислород выделяется из крови, а углекислый газ направляется обратно в легкие. Исследования показали, что гемоглобин также связывает закись азота (NO). NO — это сосудорасширяющее средство, которое расслабляет кровеносные сосуды и капилляры и может способствовать газообмену и прохождению эритроцитов через узкие сосуды. Нитроглицерин, сердечное лекарство от стенокардии и сердечных приступов, превращается в NO, чтобы помочь расслабить кровеносные сосуды и увеличить поток кислорода через тело.
Характерной чертой красных кровяных телец является их гликолипидная и гликопротеиновая оболочка; это липиды и белки, к которым прикреплены молекулы углеводов.У людей поверхностные гликопротеины и гликолипиды в эритроцитах различаются у разных людей, производя разные группы крови, такие как A, B и O.![]() Средняя продолжительность жизни красных кровяных телец составляет 120 дней, за это время они распадаются. и перерабатывается в печени и селезенке фагоцитирующими макрофагами, типом белых кровяных телец.
Средняя продолжительность жизни красных кровяных телец составляет 120 дней, за это время они распадаются. и перерабатывается в печени и селезенке фагоцитирующими макрофагами, типом белых кровяных телец.
Лейкоциты
Белые кровяные тельца, также называемые лейкоцитами (лейко = белые), составляют примерно один процент от объема клеток крови.Роль белых кровяных телец очень отличается от роли красных кровяных телец: они в первую очередь участвуют в иммунном ответе, чтобы идентифицировать и нацеливать патогены, такие как вторгшиеся бактерии, вирусы и другие чужеродные организмы. Лейкоциты образуются постоянно; некоторые живут часами или днями, а некоторые живут годами.
Морфология белых кровяных телец значительно отличается от эритроцитов. Они имеют ядра и не содержат гемоглобина. Различные типы лейкоцитов идентифицируются по их микроскопическому виду после гистологического окрашивания, и каждый из них выполняет свою специализированную функцию.Две основные группы, обе показаны на рисунке 3, — это гранулоциты, которые включают нейтрофилы, эозинофилы и базофилы, и агранулоциты, которые включают моноциты и лимфоциты.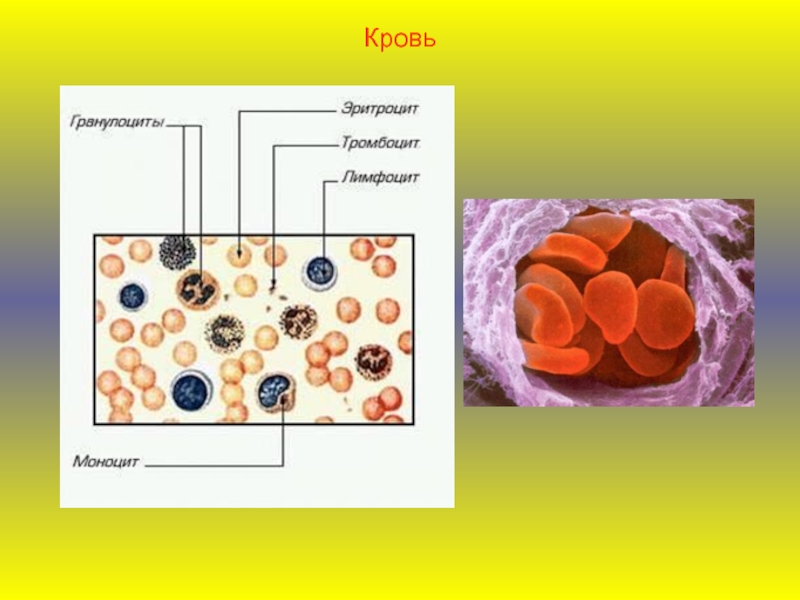
Рис. 3. (a) Гранулоциты, включая нейтрофилы, эозинофилы и базофилы, характеризуются лопастным ядром и зернистыми включениями в цитоплазме. Гранулоциты обычно первыми реагируют на травму или инфекцию. (b) Агранулоциты включают лимфоциты и моноциты. Лимфоциты, включая В- и Т-клетки, отвечают за адаптивный иммунный ответ.Моноциты дифференцируются в макрофаги и дендритные клетки, которые, в свою очередь, реагируют на инфекцию или травму.
Гранулоциты содержат гранулы в цитоплазме; агранулоциты названы так из-за отсутствия гранул в их цитоплазме. Некоторые лейкоциты становятся макрофагами, которые либо остаются на одном месте, либо перемещаются по кровотоку и собираются в местах инфекции или воспаления, где их привлекают химические сигналы от инородных частиц и поврежденных клеток. Лимфоциты являются первичными клетками иммунной системы и включают В-клетки, Т-клетки и естественные клетки-киллеры.В-клетки уничтожают бактерии и инактивируют их токсины. Они также вырабатывают антитела.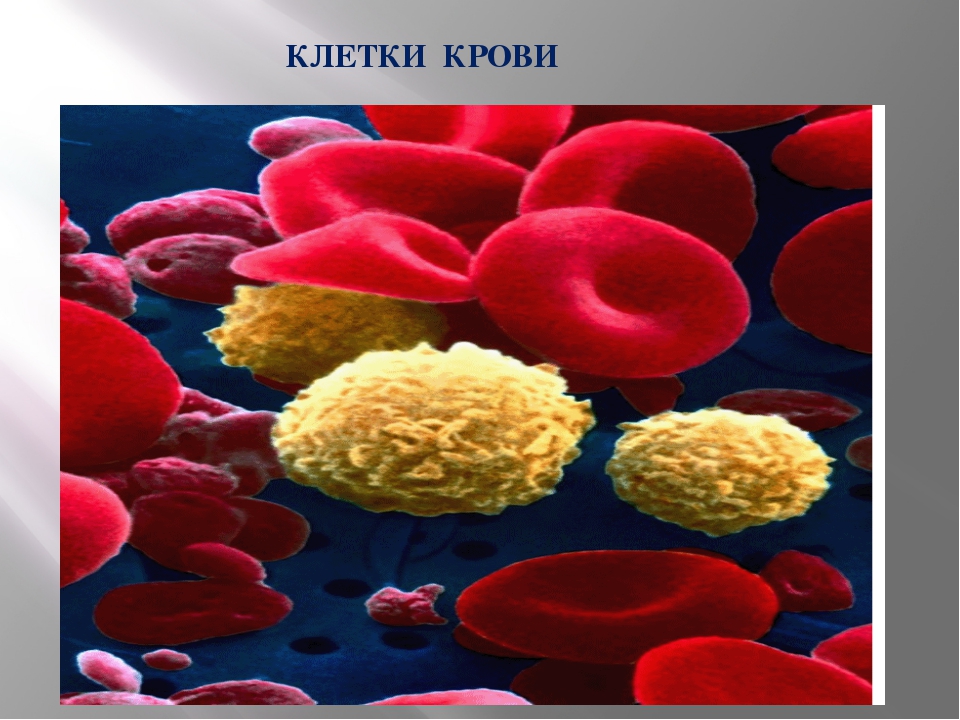 Т-клетки атакуют вирусы, грибки, некоторые бактерии, трансплантированные клетки и раковые клетки. Т-клетки атакуют вирусы, выделяя токсины, убивающие вирусы. Естественные клетки-киллеры атакуют множество инфекционных микробов и определенные опухолевые клетки.
Т-клетки атакуют вирусы, грибки, некоторые бактерии, трансплантированные клетки и раковые клетки. Т-клетки атакуют вирусы, выделяя токсины, убивающие вирусы. Естественные клетки-киллеры атакуют множество инфекционных микробов и определенные опухолевые клетки.
Одна из причин, по которой ВИЧ представляет собой серьезную проблему управления, заключается в том, что вирус напрямую нацелен на Т-клетки, проникая через рецептор. Попав внутрь клетки, ВИЧ затем размножается с помощью собственного генетического механизма Т-клетки.После репликации вируса ВИЧ он передается непосредственно от инфицированной Т-клетки к макрофагам. Наличие ВИЧ может оставаться нераспознанным в течение длительного периода времени, прежде чем проявятся полные симптомы болезни
Компоненты крови
Гемоглобин отвечает за распределение кислорода и, в меньшей степени, углекислого газа по кровеносной системе человека, позвоночных и многих беспозвоночных. Однако кровь — это больше, чем белки. Кровь — это термин, используемый для описания жидкости, которая движется по сосудам, и включает плазмы, (жидкая часть, которая содержит воду, белки, соли, липиды и глюкозу), а также клетки (красные и белые клетки) и фрагменты клеток. называется тромбоцитов .Плазма крови на самом деле является доминирующим компонентом крови и содержит воду, белки, электролиты, липиды и глюкозу. Клетки несут ответственность за перенос газов (эритроциты) и иммунную реакцию (белый цвет). Тромбоциты отвечают за свертывание крови. Межклеточная жидкость, окружающая клетки, отделена от крови, но в гемолимфе они объединены. У человека клеточные компоненты составляют примерно 45 процентов крови и 55 процентов жидкой плазмы. Кровь составляет 20 процентов внеклеточной жидкости человека и восемь процентов веса.
называется тромбоцитов .Плазма крови на самом деле является доминирующим компонентом крови и содержит воду, белки, электролиты, липиды и глюкозу. Клетки несут ответственность за перенос газов (эритроциты) и иммунную реакцию (белый цвет). Тромбоциты отвечают за свертывание крови. Межклеточная жидкость, окружающая клетки, отделена от крови, но в гемолимфе они объединены. У человека клеточные компоненты составляют примерно 45 процентов крови и 55 процентов жидкой плазмы. Кровь составляет 20 процентов внеклеточной жидкости человека и восемь процентов веса.
Тромбоциты и факторы свертывания
Кровь должна свернуться для заживления ран и предотвращения чрезмерной кровопотери. Маленькие фрагменты клеток, называемые тромбоцитами (тромбоцитами), притягиваются к месту раны, где они прикрепляются, расширяя множество выступов и высвобождая их содержимое. Это содержимое активирует другие тромбоциты, а также взаимодействует с другими факторами свертывания, которые превращают фибриноген, водорастворимый белок, присутствующий в сыворотке крови, в фибрин (не растворимый в воде белок), вызывая свертывание крови. Для работы многих факторов свертывания крови необходим витамин К, а дефицит витамина К может привести к проблемам со свертыванием крови. Многие тромбоциты сходятся и слипаются в месте раны, образуя тромбоцитарную пробку (также называемую фибриновым сгустком), как показано на рисунке 4b. Пробка или сгусток сохраняется в течение нескольких дней и останавливает потерю крови. Тромбоциты образуются в результате распада более крупных клеток, называемых мегакариоцитами, как показано на рисунке 4a. На каждый мегакариоцит образуется 2000–3000 тромбоцитов, при этом в каждом кубическом миллиметре крови присутствует от 150 000 до 400 000 тромбоцитов.Каждая пластинка имеет форму диска и имеет диаметр 2–4 мкм. Они содержат множество мелких пузырьков, но не содержат ядра.
Для работы многих факторов свертывания крови необходим витамин К, а дефицит витамина К может привести к проблемам со свертыванием крови. Многие тромбоциты сходятся и слипаются в месте раны, образуя тромбоцитарную пробку (также называемую фибриновым сгустком), как показано на рисунке 4b. Пробка или сгусток сохраняется в течение нескольких дней и останавливает потерю крови. Тромбоциты образуются в результате распада более крупных клеток, называемых мегакариоцитами, как показано на рисунке 4a. На каждый мегакариоцит образуется 2000–3000 тромбоцитов, при этом в каждом кубическом миллиметре крови присутствует от 150 000 до 400 000 тромбоцитов.Каждая пластинка имеет форму диска и имеет диаметр 2–4 мкм. Они содержат множество мелких пузырьков, но не содержат ядра.
Рис. 4. (a) Тромбоциты образуются из крупных клеток, называемых мегакариоцитами. Мегакариоцит распадается на тысячи фрагментов, которые становятся тромбоцитами. (b) Тромбоциты необходимы для свертывания крови. Тромбоциты собираются на участке раны вместе с другими факторами свертывания, такими как фибриноген, с образованием фибринового сгустка, который предотвращает потерю крови и позволяет ране зажить.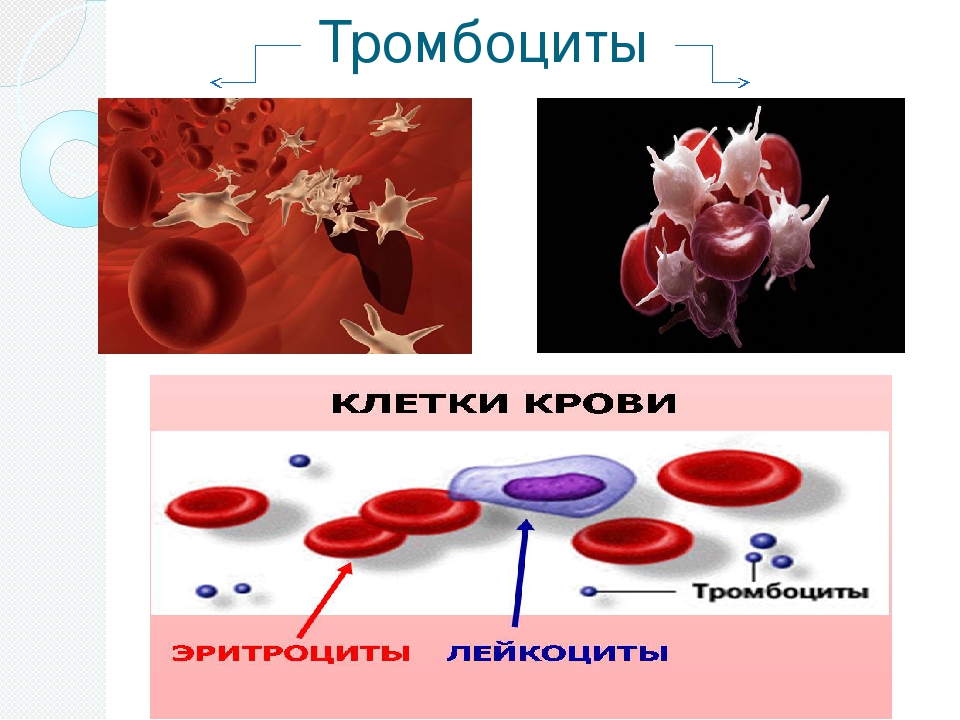
Плазма и сыворотка
Жидкий компонент крови называется плазмой, и он отделяется путем вращения или центрифугирования крови при высоких оборотах (3000 об / мин или выше). Клетки крови и тромбоциты разделяются центробежными силами на дно пробирки с образцом. Верхний жидкий слой, плазма, на 90% состоит из воды и различных веществ, необходимых для поддержания pH тела, осмотической нагрузки и защиты организма. Плазма также содержит факторы свертывания и антитела.
Плазменный компонент крови без факторов свертывания называется сывороткой . Сыворотка похожа на интерстициальную жидкость, в которой правильный состав ключевых ионов, действующих как электролиты, необходим для нормального функционирования мышц и нервов. К другим компонентам сыворотки относятся белки, которые помогают поддерживать pH и осмотический баланс, придавая крови вязкость. Сыворотка также содержит антитела, специализированные белки, которые важны для защиты от вирусов и бактерий.Липиды, включая холестерин, также переносятся в сыворотке вместе с различными другими веществами, включая питательные вещества, гормоны, метаболические отходы, а также внешние вещества, такие как лекарства, вирусы и бактерии.
Сывороточный альбумин человека является наиболее распространенным белком в плазме крови человека и синтезируется в печени. Альбумин, составляющий примерно половину белка сыворотки крови, переносит гормоны и жирные кислоты, буферизует pH и поддерживает осмотическое давление. Иммуноглобин представляет собой белковое антитело, вырабатываемое слизистой оболочкой, и играет важную роль в опосредованном антителами иммунитете.
Типы крови, связанные с белками на поверхности красных кровяных телец
Красные кровяные тельца покрыты антигенами, состоящими из гликолипидов и гликопротеинов. Состав этих молекул определяется генетикой, которая эволюционировала с течением времени. У людей разные поверхностные антигены сгруппированы в 24 разные группы крови с более чем 100 различными антигенами на каждом эритроците. Две наиболее известные группы крови — это ABO, показанная на рисунке 5, и резус-система.Поверхностные антигены в группе крови ABO представляют собой гликолипиды, называемые антигеном A и антигеном B. Люди с группой крови A имеют антиген A, люди с группой крови B имеют антиген B, люди с группой крови AB имеют оба антигена, а люди с группой крови O не имеют ни одного антигена. Антитела, называемые агглютиноугенами, обнаруживаются в плазме крови и реагируют с антигенами A или B, если они смешаны. При объединении крови типа A и типа B агглютинация (слипание) крови происходит из-за антител в плазме, которые связываются с противоположным антигеном; это вызывает образование тромбов, которые коагулируют в почках, вызывая почечную недостаточность.Кровь типа O не имеет ни антигенов A, ни B, поэтому кровь типа O можно сдавать всем группам крови. Отрицательная кровь типа O — универсальный донор. Положительная кровь типа AB является универсальным акцептором, поскольку она имеет антиген как A, так и B. Группы крови ABO были открыты в 1900 и 1901 годах Карлом Ландштейнером в Венском университете.
Люди с группой крови A имеют антиген A, люди с группой крови B имеют антиген B, люди с группой крови AB имеют оба антигена, а люди с группой крови O не имеют ни одного антигена. Антитела, называемые агглютиноугенами, обнаруживаются в плазме крови и реагируют с антигенами A или B, если они смешаны. При объединении крови типа A и типа B агглютинация (слипание) крови происходит из-за антител в плазме, которые связываются с противоположным антигеном; это вызывает образование тромбов, которые коагулируют в почках, вызывая почечную недостаточность.Кровь типа O не имеет ни антигенов A, ни B, поэтому кровь типа O можно сдавать всем группам крови. Отрицательная кровь типа O — универсальный донор. Положительная кровь типа AB является универсальным акцептором, поскольку она имеет антиген как A, так и B. Группы крови ABO были открыты в 1900 и 1901 годах Карлом Ландштейнером в Венском университете.
Группа крови резус была впервые обнаружена у макак-резусов. У большинства людей есть резус-антиген (Rh +), и у них нет анти-резус-антител в крови. Те немногие люди, у которых нет резус-антигена и являются резус-фактором, могут развить анти-резус-антитела при контакте с Rh + кровью.Это может произойти после переливания крови или после того, как Rh– женщина родила Rh + ребенка. Первое воздействие обычно не вызывает реакции; однако при втором воздействии в крови накопилось достаточно антител, чтобы вызвать реакцию, вызывающую агглютинацию и разрушение эритроцитов. Инъекция может предотвратить эту реакцию.
Те немногие люди, у которых нет резус-антигена и являются резус-фактором, могут развить анти-резус-антитела при контакте с Rh + кровью.Это может произойти после переливания крови или после того, как Rh– женщина родила Rh + ребенка. Первое воздействие обычно не вызывает реакции; однако при втором воздействии в крови накопилось достаточно антител, чтобы вызвать реакцию, вызывающую агглютинацию и разрушение эритроцитов. Инъекция может предотвратить эту реакцию.
Рис. 5. Эритроциты человека могут иметь на своей поверхности гликопротеины типа A или B, оба гликопротеина в сочетании (AB) или ни один из них (O). Гликопротеины служат антигенами и могут вызывать иммунный ответ у человека, которому переливают незнакомые антигены.Кровь типа O, не содержащая антигенов A или B, не вызывает иммунного ответа при введении человеку любой группы крови. Таким образом, O считается универсальным донором. Люди с кровью типа AB могут принимать кровь любой группы крови, а группа AB считается универсальным акцептором.
Вкратце: Структура и функции крови
Красные кровяные тельца — это специализированные клетки, которые содержат гемоглобин и циркулируют по телу, доставляя кислород к клеткам.Лейкоциты участвуют в иммунном ответе, чтобы идентифицировать вторгшиеся бактерии, вирусы и другие чужеродные организмы и бороться с ними; они также перерабатывают ненужные компоненты, такие как старые эритроциты.
Тромбоциты и факторы свертывания крови вызывают превращение растворимого белка фибриногена в нерастворимый белок фибрин в месте раны, образуя пробку. Плазма на 90% состоит из воды и различных веществ, таких как факторы свертывания крови и антитела. Сыворотка — это плазменный компонент крови без факторов свертывания.
Проверьте свое понимание Ответьте на вопросы ниже, чтобы увидеть, насколько хорошо вы понимаете темы, затронутые в предыдущем разделе. В этой короткой викторине , а не засчитываются в вашу оценку в классе, и вы можете пересдавать ее неограниченное количество раз.
В этой короткой викторине , а не засчитываются в вашу оценку в классе, и вы можете пересдавать ее неограниченное количество раз.
Используйте этот тест, чтобы проверить свое понимание и решить, следует ли (1) изучить предыдущий раздел дальше или (2) перейти к следующему разделу.
фактов о крови и клетках крови
Эта информация объясняет различные части вашей крови и их функции.
Ваша кровь доставляет кислород и питательные вещества ко всем клеткам вашего тела. Клетки крови также борются с инфекцией и останавливают кровотечение.
Большинство клеток крови производится в костном мозге. Их постоянно производят и заменяют. Продолжительность жизни клетки крови до ее замены называется продолжительностью ее жизни.
Ваша кровь состоит из 4 частей: эритроцитов, лейкоцитов, тромбоцитов и плазмы.
Части вашей крови
Эритроциты (эритроциты)
Красные кровяные тельца переносят кислород из легких в ткани. Они также возвращают углекислый газ в легкие.
Они также возвращают углекислый газ в легкие.
Красные кровяные тельца составляют почти половину вашей крови. Продолжительность жизни эритроцита составляет около 120 дней.
Лейкоциты (лейкоциты)
Лейкоциты борются с инфекциями и являются важной частью вашей иммунной системы. Они составляют очень небольшую часть вашей крови (менее 1%).
Есть 3 типа лейкоцитов: гранулоциты, моноциты и лимфоциты. У каждого типа есть важная роль.
- Существует 3 типа гранулоцитов:
- Нейтрофилы помогают бороться с бактериальными и грибковыми инфекциями.
- Базофилы являются частью иммунного ответа вашего организма. Их точная функция неизвестна.
- Эозинофилы помогают бороться с инфекциями, вызванными паразитами.
- Моноциты разрушаются и удаляют из вашего тела инородные организмы и умирающие клетки.
- Лимфоциты составляют вашу иммунную систему.
Продолжительность жизни белых кровяных телец может варьироваться от часов до лет.
Тромбоциты (тромбоциты)
Тромбоциты — это небольшие части клеток. Их основная функция — остановить кровотечение. Они составляют очень небольшую часть вашей крови (менее 1%). Продолжительность жизни тромбоцитов составляет от 9 до 12 дней.
Плазма
Плазма — это бледно-желтая жидкая часть вашей крови, которая содержит все ваши кровяные тельца. Он составляет чуть более половины всей вашей крови.
Плазма помогает перемещать воду, питательные вещества, минералы, лекарства и гормоны по всему телу. Он также переносит продукты жизнедеятельности в почки. Затем почки отфильтровывают продукты жизнедеятельности из крови. Плазма состоит из воды, белков, липидов (жиров). Он переносит воду, жирорастворимые питательные вещества и другие вещества в разные органы и из них.
18.3 Эритроциты — анатомия и физиология
Цели обучения
К концу этого раздела вы сможете:
Обсудить структуру и функцию эритроцитов (красных кровяных телец) и гемоглобина
- Описать анатомию эритроцитов
- Объясните состав и функцию гемоглобина
- Обсудите различные этапы жизненного цикла эритроцита
Эритроцит , широко известный как красные кровяные тельца (или эритроциты), на сегодняшний день является наиболее распространенным формованным элементом: одна капля крови содержит миллионы эритроцитов и только тысячи лейкоцитов (Рисунок 18.3.1). В частности, у мужчин содержится около 5,4 миллиона эритроцитов на микролитр ( µ л) крови, а у женщин — примерно 4,8 миллиона на µ L. Фактически, по оценкам, эритроциты составляют около 25 процентов от общего количества клеток в организме. . Это маленькие клетки со средним диаметром 7–8 микрометров ( µ м). Основная функция эритроцитов — забирать кислород из легких и транспортировать его к тканям организма, а также собирать углекислый газ тканями и транспортировать его в легкие.Хотя лейкоциты обычно покидают кровеносные сосуды для выполнения своих защитных функций, движение эритроцитов из кровеносных сосудов является ненормальным.
Рисунок 18.3.1 Сводка сформированных элементов в кровиПо мере созревания эритроцита в красном костном мозге он вытесняет свое ядро и большинство других своих органелл. В течение первых дней или двух, когда он находится в кровотоке, незрелый эритроцит, известный как ретикулоцит , обычно все еще будет содержать остатки органелл.Ретикулоциты должны составлять примерно 1-2 процента от количества эритроцитов и обеспечивать приблизительную оценку скорости образования эритроцитов. Аномально низкий или высокий уровень ретикулоцитов указывает на отклонения в продукции этих эритроцитов. Эти остатки органелл быстро отслаиваются, поэтому циркулирующие эритроциты имеют мало внутренних структурных компонентов клетки. В отсутствие митохондрий эритроциты полагаются на анаэробное дыхание. Это означает, что они не используют кислород, который они транспортируют, поэтому они могут доставить его в ткани.У них также отсутствует эндоплазматическая сеть, и они не синтезируют белки. Однако эритроциты содержат некоторые структурные белки, которые помогают клеткам крови поддерживать свою уникальную структуру и позволяют им изменять свою форму, чтобы протиснуться через капилляры. Сюда входит белковый спектрин, белковый элемент цитоскелета.
Эритроциты — двояковогнутые диски; то есть они пухлые на периферии и очень тонкие в центре (рис. 18.3.2). Поскольку в них отсутствует большинство органелл, внутри больше места для присутствия молекул гемоглобина, которые, как вы вскоре увидите, переносят газы.Двояковогнутая форма также обеспечивает большую площадь поверхности, на которой может происходить газообмен, по сравнению с ее объемом; сфера аналогичного диаметра будет иметь меньшее отношение площади поверхности к объему. В капиллярах кислород, переносимый эритроцитами, может диффундировать в плазму, а затем через стенки капилляров, достигая клеток, в то время как часть углекислого газа, производимого клетками в качестве продукта жизнедеятельности, диффундирует в капилляры и поглощается ими. эритроциты. Капиллярные русла чрезвычайно узкие, что замедляет прохождение эритроцитов и предоставляет расширенные возможности для газообмена.Однако пространство внутри капилляров может быть настолько маленьким, что, несмотря на свой небольшой размер, эритроциты иногда складываются сами по себе, чтобы пройти через них. К счастью, их структурные белки, такие как спектрин, гибкие, что позволяет им складываться, а затем снова отскакивать, когда они попадают в более широкий сосуд.
Рисунок 18.3.2 — Форма красных кровяных телец: Эритроциты представляют собой двояковогнутые диски с очень мелкими центрами. Эта форма оптимизирует соотношение площади поверхности к объему, облегчая газообмен.Это также позволяет им складываться при движении по узким кровеносным сосудам.Гемоглобин — большая молекула, состоящая из белков и железа. Он состоит из четырех свернутых цепей белка глобина , обозначенных альфа 1 и 2 и бета 1 и 2 (рис. 18.3.3 a ). Каждая из этих молекул глобина связана с молекулой красного пигмента под названием гем , который содержит ион железа (Fe 2+ ) (рис. 18.3.3 b ).
Рисунок 18.3.3 — Гемоглобин: (a) Молекула гемоглобина содержит четыре глобиновых белка, каждый из которых связан с одной молекулой железосодержащего пигментного гема. (б) Один эритроцит может содержать 300 миллионов молекул гемоглобина и, следовательно, более 1 миллиарда молекул кислорода.Каждый ион железа в геме может связываться с одной молекулой кислорода, следовательно, каждая молекула гемоглобина может переносить четыре молекулы кислорода. Отдельный эритроцит может содержать около 300 миллионов молекул гемоглобина и может связываться и транспортировать до 1.2 миллиарда молекул кислорода.
В легких гемоглобин поглощает кислород, который связывается с ионами железа, образуя оксигемоглобин . Ярко-красный насыщенный кислородом гемоглобин перемещается в капилляры тканей тела, где он высвобождает некоторые молекулы кислорода, становясь более темно-красным дезоксигемоглобин . Выделение кислорода зависит от потребности в кислороде окружающих тканей, поэтому гемоглобин редко оставляет весь свой кислород позади. В это время диоксид углерода (CO 2 ) попадает в кровоток.Около 76 процентов CO 2 растворяется в плазме, часть его остается в виде растворенного CO 2 , а остальная часть образует бикарбонат. Около 23–24 процентов его связывается с аминокислотами в гемоглобине, образуя молекулу, известную как карбаминогемоглобин . Из капилляров гемоглобин переносит CO 2 обратно в легкие.
Изменения в уровнях эритроцитов могут существенно повлиять на способность организма эффективно доставлять кислород к тканям.Избыточное производство эритроцитов вызывает состояние, называемое полицитемией. Основным недостатком полицитемии является не отсутствие достаточного количества кислорода в тканях, а, скорее, повышенная вязкость крови, которая затрудняет циркуляцию крови в сердце. Неэффективный гематопоэз приводит к недостаточному количеству эритроцитов и приводит к одной из нескольких форм анемии. У пациентов с недостаточным гемоглобином ткани могут не получать достаточного количества кислорода, что приводит к другой форме анемии.
При определении оксигенации тканей наибольший интерес в здравоохранении представляет процент насыщения; то есть процент участков гемоглобина, занятых кислородом в крови пациента. Клинически это значение обычно обозначается просто как «процент насыщения». Процент насыщения обычно контролируется с помощью устройства, известного как пульсоксиметр, который прикладывают к тонкой части тела, обычно к кончику пальца пациента. Устройство работает, посылая через палец световые волны двух разных длин (одна красная, другая инфракрасная) и измеряя свет с помощью фотодетектора на выходе.Гемоглобин по-разному поглощает свет в зависимости от его насыщения кислородом. Устройство калибрует количество света, полученного фотодетектором, по количеству, поглощенному частично оксигенированным гемоглобином, и представляет данные как процент насыщения. Нормальные показания пульсоксиметра находятся в диапазоне 95–100 процентов. Более низкие проценты отражают гипоксемию или низкий уровень кислорода в крови. Термин «гипоксия» является более общим и просто относится к низкому уровню кислорода. Уровень кислорода также контролируется непосредственно по свободному кислороду в плазме, обычно после артериальной палочки.Когда применяется этот метод, количество присутствующего кислорода выражается в единицах парциального давления кислорода или просто pO 2 и обычно регистрируется в миллиметрах ртутного столба, мм рт.
Рецепторы насыщения кислородом находятся в почках, что является идеальным местом для контроля насыщения, поскольку почки фильтруют около 180 литров (~ 380 пинт) крови у среднего взрослого каждый день. В ответ на гипоксемию в почки проникает меньше кислорода, что приводит к гипоксии почечных клеток, где фактически контролируется концентрация кислорода.Интерстициальные фибробласты в почках секретируют ЭПО, что приводит к увеличению продукции эритроцитов и, в конечном итоге, к восстановлению уровня кислорода. В петле отрицательной обратной связи по мере увеличения насыщения кислородом секреция ЭПО падает, и наоборот, тем самым поддерживая гомеостаз. Население, живущее на большой высоте с изначально более низким уровнем кислорода в атмосфере, естественно, поддерживает более высокий гематокрит, чем люди, живущие на уровне моря. Следовательно, люди, путешествующие на большие высоты, могут испытывать симптомы гипоксемии, такие как усталость, головная боль и одышка, в течение нескольких дней после прибытия.В ответ на гипоксемию почки секретируют ЭПО, чтобы увеличить производство эритроцитов до тех пор, пока гомеостаз снова не будет достигнут. Чтобы избежать симптомов гипоксемии или высотной болезни, альпинисты обычно отдыхают от нескольких дней до недели или более в нескольких лагерях, расположенных на увеличивающейся высоте, чтобы обеспечить повышение уровня ЭПО и, следовательно, количества эритроцитов. При восхождении на самые высокие вершины, такие как Mt. Эверест и К2 в Гималаях, многие альпинисты полагаются на баллонный кислород, когда они приближаются к вершине.
Производство:Производство эритроцитов в костном мозге происходит с поразительной скоростью — более 2 миллионов клеток в секунду. Для того чтобы это производство происходило, необходимо наличие определенного количества сырья в достаточных количествах. К ним относятся те же питательные вещества, которые необходимы для производства и поддержания любой клетки, такие как глюкоза, липиды и аминокислоты. Однако для производства эритроцитов также необходимы несколько микроэлементов:
- Железо: Мы сказали, что каждая гемовая группа в молекуле гемоглобина содержит ион микроэлемента железа.В среднем усваивается менее 20 процентов потребляемого нами железа. Гемовое железо из продуктов животного происхождения, таких как мясо, птица и рыба, усваивается более эффективно, чем негемовое железо из растительной пищи. После абсорбции железо становится частью общего запаса железа в организме. Костный мозг, печень и селезенка могут хранить железо в белковых соединениях , ферритине и гемосидерине . Ферропортин транспортирует железо через плазматические мембраны клеток кишечника и из мест его хранения в тканевую жидкость, где оно попадает в кровь.Когда ЭПО стимулирует выработку эритроцитов, железо высвобождается из хранилища, связывается с трансферрином и переносится в красный костный мозг, где оно прикрепляется к предшественникам эритроцитов.
- Медь: Микроэлемент, медь является компонентом двух белков плазмы, гефестина и церулоплазмина. Без этого гемоглобин не мог бы вырабатываться должным образом. Гефестин, расположенный в ворсинках кишечника, обеспечивает всасывание железа клетками кишечника. Церулоплазмин переносит медь.Оба обеспечивают окисление железа из Fe 2+ в Fe 3+ , форму, в которой оно может быть связано со своим транспортным белком, трансферрином, для транспортировки к клеткам организма. В состоянии дефицита меди транспорт железа для синтеза гема снижается, и железо может накапливаться в тканях, что в конечном итоге может привести к повреждению органов.
- Цинк: Микроэлемент цинка действует как кофермент, который способствует синтезу гемовой части гемоглобина.
- Витамины группы В: Витамины группы В, фолиевая кислота и витамин В 12 действуют как коферменты, способствующие синтезу ДНК.Таким образом, оба имеют решающее значение для синтеза новых клеток, в том числе эритроцитов.
Деградация:
Эритроциты живут в кровообращении до 120 дней, после чего изношенные клетки удаляются миелоидными фагоцитарными клетками, называемыми макрофагами , расположенными в основном в костном мозге, печени и селезенке. Компоненты гемоглобина разрушенных эритроцитов далее обрабатываются следующим образом:
- Глобин, белковая часть гемоглобина, расщепляется на аминокислоты, которые могут быть отправлены обратно в костный мозг для использования в производстве новых эритроцитов.Гемоглобин, который не подвергается фагоцитозу, расщепляется в кровотоке, высвобождая альфа- и бета-цепи, которые удаляются из кровотока почками.
- Железо, содержащееся в гемовой части гемоглобина, может храниться в печени или селезенке, прежде всего в форме ферритина или гемосидерина, или переноситься через кровоток с трансферрином в красный костный мозг для переработки в новые эритроциты.
- Часть гема, не содержащая железа, разлагается на продукт жизнедеятельности биливердин , зеленый пигмент, а затем на другой продукт отходов, билирубин , желтый пигмент.Билирубин связывается с альбумином и перемещается с кровью в печень, которая использует его для производства желчи — соединения, выделяемого в кишечнике для эмульгирования пищевых жиров. В толстом кишечнике бактерии расщепляют билирубин отдельно от желчи и превращают его в уробилиноген, а затем в стеркобилин. Затем он выводится из организма с калом. Антибиотики широкого спектра действия обычно также уничтожают эти бактерии и могут изменить цвет фекалий. Почки также удаляют циркулирующий билирубин и другие побочные продукты метаболизма, такие как уробилин, и выделяют их с мочой.
Пигменты разложения, образовавшиеся в результате разрушения гемоглобина, можно увидеть в различных ситуациях. В месте травмы биливердин из поврежденных эритроцитов дает некоторые из драматических цветов, связанных с синяками. При нарушении функции печени билирубин не может быть эффективно удален из кровообращения, и тело приобретает желтоватый оттенок, связанный с желтухой. Стеркобилины в фекалиях дают типичный коричневый цвет, связанный с этими отходами. А желтый цвет мочи связан с уробилинами.
Жизненный цикл эритроцитов представлен на Рисунке 18.3.4.
Рисунок 18.3.4 — Жизненный цикл эритроцитов: эритроцитов вырабатываются в костном мозге и отправляются в кровоток. В конце своего жизненного цикла они уничтожаются макрофагами, а их компоненты перерабатываются.Размер, форма и количество эритроцитов, а также количество молекул гемоглобина могут иметь большое влияние на здоровье человека. Когда количество эритроцитов или гемоглобина недостаточное, общее состояние называется анемией .Существует более 400 типов анемии, и более 3,5 миллионов американцев страдают этим заболеванием. Анемии можно разделить на три основные группы: анемии, вызванные кровопотерей, анемии, вызванные неправильным или сниженным образованием эритроцитов, и анемии, вызванные чрезмерным разрушением эритроцитов. Клиницисты часто используют две группы в диагностике: кинетический подход фокусируется на оценке образования, разрушения и удаления эритроцитов, тогда как морфологический подход исследует сами эритроциты, уделяя особое внимание их размеру.Распространенным тестом является средний объем тельца (MCV), который измеряет размер. Клетки нормального размера называются нормоцитами, клетки меньшего размера — микроцитами, а клетки большего размера — макроцитами. Подсчет ретикулоцитов также важен и может выявить недостаточное производство эритроцитов. Эффекты различных анемий широко распространены, потому что уменьшение количества эритроцитов или гемоглобина приведет к снижению уровня кислорода, доставляемого к тканям организма. Поскольку кислород необходим для функционирования тканей, анемия вызывает утомляемость, вялость и повышает риск инфицирования.Дефицит кислорода в головном мозге снижает способность ясно мыслить и может вызвать головные боли и раздражительность. Недостаток кислорода вызывает у пациента одышку, хотя сердце и легкие работают тяжелее в ответ на его дефицит.
Анемии кровопотери довольно просты. Помимо кровотечения из ран или других повреждений, эти формы анемии могут быть вызваны язвами, геморроем, воспалением желудка (гастритом) и некоторыми видами рака желудочно-кишечного тракта. Чрезмерное употребление аспирина или других нестероидных противовоспалительных препаратов, таких как ибупрофен, может вызвать язвы и гастрит.Потенциальными причинами также являются обильная менструация и потеря крови во время родов.
Анемии, вызванные нарушением или снижением выработки эритроцитов, включают серповидно-клеточную анемию, железодефицитную анемию, авитаминозную анемию, а также заболевания костного мозга и стволовых клеток.
- Характерное изменение формы эритроцитов наблюдается в серповидно-клеточной анемии (также называемой серповидно-клеточной анемией). Это генетическое заболевание, вызванное выработкой гемоглобина аномального типа, называемого гемоглобином S, который доставляет меньше кислорода к тканям и заставляет эритроциты принимать серповидную (или серповидную) форму, особенно при низких концентрациях кислорода (рис.3.5). Эти клетки аномальной формы могут затем оседать в узких капиллярах, потому что они не могут складываться сами по себе, чтобы протиснуться через них, блокируя кровоток к тканям и вызывая множество серьезных проблем от болезненных суставов до задержки роста и даже слепоты и нарушений мозгового кровообращения (инсульты). ). Серповидно-клеточная анемия — это генетическое заболевание, которое особенно встречается у лиц африканского происхождения.
- Железодефицитная анемия является наиболее распространенным типом и возникает, когда количество доступного железа недостаточно для производства достаточного количества гема. Это состояние может возникать у людей с дефицитом железа в рационе и особенно часто встречается у подростков и детей, а также у веганов и вегетарианцев. Кроме того, железодефицитная анемия может быть вызвана либо неспособностью усваивать и транспортировать железо, либо медленным хроническим кровотечением.
- Витаминно-дефицитные анемии обычно связаны с недостаточностью витамина B12 и фолиевой кислоты.
- Мегалобластная анемия связана с дефицитом витамина B12 и / или фолиевой кислоты и часто связана с диетами с дефицитом этих основных питательных веществ. Отсутствие мяса или жизнеспособного альтернативного источника, а также переварка или употребление недостаточного количества овощей могут привести к недостатку фолиевой кислоты.
- Пагубная анемия вызвана плохой абсорбцией витамина B12 и часто наблюдается у пациентов с болезнью Крона (тяжелое кишечное заболевание, часто лечатся хирургическим путем), хирургическим удалением кишечника или желудка (обычно при некоторых операциях по снижению веса), кишечными паразитами, и СПИД.
- Беременность, некоторые лекарства, чрезмерное употребление алкоголя и некоторые заболевания, такие как целиакия, также связаны с дефицитом витаминов. Очень важно обеспечить достаточное количество фолиевой кислоты на ранних сроках беременности, чтобы снизить риск неврологических дефектов, в том числе расщелины позвоночника, когда нервная трубка не закрывается.
- Различные болезненные процессы также могут препятствовать производству и образованию эритроцитов и гемоглобина. Если миелоидные стволовые клетки являются дефектными или заменяются раковыми клетками, будет произведено недостаточное количество эритроцитов.
- Апластическая анемия — это состояние, при котором наблюдается недостаточное количество стволовых клеток эритроцитов. Апластическая анемия часто передается по наследству или может быть вызвана радиацией, лекарствами, химиотерапией или инфекцией.
- Талассемия — это унаследованное заболевание, обычно встречающееся у людей с Ближнего Востока, Средиземноморья, Африки и Юго-Восточной Азии, при котором созревание эритроцитов не происходит нормально. Самая тяжелая форма называется анемией Кули.
- Воздействие свинца из промышленных источников или даже пыль от кусочков краски железосодержащих красок или керамики, которая не была должным образом глазурована, также может привести к разрушению красного костного мозга.
- Различные болезненные процессы также могут приводить к анемии. К ним относятся хронические заболевания почек, часто связанные со снижением выработки ЭПО, гипотиреоз, некоторые формы рака, волчанка и ревматоидный артрит.
В отличие от анемии повышенное количество эритроцитов называется полицитемией и обнаруживается при повышенном гематокрите пациента. Это может происходить временно у обезвоженного человека; при недостаточном водопотреблении или чрезмерных потерях воды объем плазмы падает.В результате повышается гематокрит. По причинам, упомянутым ранее, легкая форма полицитемии является хронической, но нормой для людей, живущих на больших высотах. Некоторые элитные спортсмены тренируются на большой высоте специально для того, чтобы вызвать это явление. Наконец, тип заболевания костного мозга, называемый истинной полицитемией (от греческого vera = «истинный»), вызывает чрезмерное производство незрелых эритроцитов. Истинная полицитемия может привести к опасному повышению вязкости крови, повышению артериального давления и затруднению перекачки крови сердцем по всему телу.Это относительно редкое заболевание, которое чаще встречается у мужчин, чем у женщин, и чаще встречается у пожилых пациентов старше 60 лет.
Обзор главы
Эритроциты — самые распространенные в крови форменные элементы — красные двояковогнутые диски, заполненные соединением, переносящим кислород, называемым гемоглобином. Молекула гемоглобина содержит четыре белка глобина, связанных с молекулой пигмента, называемой гемом, который содержит ион железа. В кровотоке железо поглощает кислород в легких и отдает его тканям; Затем аминокислоты в гемоглобине переносят углекислый газ из тканей обратно в легкие.Эритроциты живут в среднем всего 120 дней, и поэтому их необходимо постоянно восстанавливать. Изношенные эритроциты фагоцитируются макрофагами, и их гемоглобин расщепляется. Продукты распада перерабатываются или удаляются как отходы: глобин расщепляется на аминокислоты для синтеза новых белков; железо хранится в печени или селезенке или используется костным мозгом для производства новых эритроцитов; а остатки гема превращаются в билирубин или другие продукты жизнедеятельности, которые поглощаются печенью и выводятся с желчью или выводятся почками.Анемия — это дефицит эритроцитов или гемоглобина, тогда как полицитемия — это избыток эритроцитов.
Обзорные вопросы
Вопросы о критическом мышлении
1. У молодой женщины в течение нескольких лет наблюдается необычно обильное менструальное кровотечение. Она придерживается строгой веганской диеты (без продуктов животного происхождения). По какому заболеванию она подвержена риску и почему?
2. У пациента талассемия — генетическое заболевание, характеризующееся аномальным синтезом белков глобина и чрезмерным разрушением эритроцитов.Этот пациент страдает желтухой и имеет повышенный уровень билирубина в крови. Объясните связь.
Глоссарий
- анемия
- дефицит эритроцитов или гемоглобина
- билирубин
- Желтоватый желчный пигмент, образующийся при удалении железа из гема и его дальнейшем распаде на отходы
- биливердин
- зеленый желчный пигмент, образующийся при разложении не содержащей железа части гема в отходы; превращается в билирубин в печени
- карбаминогемоглобин
- соединение диоксида углерода и гемоглобина, и один из путей, которым диоксид углерода переносится в кровь
- дезоксигемоглобин
- Молекула гемоглобина без связанной с ней молекулы кислорода
- эритроцит
- (также эритроцит) зрелая миелоидная кровяная клетка, которая состоит в основном из гемоглобина и функционирует в основном в транспортировке кислорода и углекислого газа
- ферритин
- белковая запасная форма железа, обнаруженная в костном мозге, печени и селезенке
- глобин
- гемсодержащий глобулярный белок, входящий в состав гемоглобина
- гем
- красный железосодержащий пигмент, с которым связывается кислород в гемоглобине
- гемоглобин
- кислородпереносящее соединение в эритроцитах
- гемосидерин
- белковая форма хранения железа, обнаруженная в костном мозге, печени и селезенке
- гипоксемия
- уровень насыщения крови кислородом ниже нормы (обычно <95 процентов)
- макрофаг
- фагоцитарная клетка миелоидной линии; Созревший моноцит
- оксигемоглобин
- Молекула гемоглобина, с которой связан кислород
- полицитемия
- Повышенный уровень гемоглобина, адаптивный или патологический
- ретикулоцитов
- незрелый эритроцит, который все еще может содержать фрагменты органелл
- серповидноклеточная анемия
- (также серповидно-клеточная анемия) наследственное заболевание крови, при котором молекулы гемоглобина деформированы, что приводит к разрушению эритроцитов, которые принимают характерную серповидную форму
- талассемия
- наследственное заболевание крови, при котором созревание эритроцитов не происходит нормально, что приводит к аномальному образованию гемоглобина и разрушению эритроцитов
- трансферрин
- Белок плазмы, который обратимо связывается с железом и распределяет его по организму
Решения
Ответы на вопросы о критическом мышлении
- Она подвержена риску анемии, потому что ее необычно обильное менструальное кровотечение приводит к чрезмерной потере эритроцитов каждый месяц.В то же время ее веганская диета означает, что она не имеет диетических источников гемового железа. Негемовое железо, которое она потребляет с растительной пищей, усваивается не так хорошо, как гемовое железо.
- Билирубин — это продукт распада не содержащего железа компонента гема, который отщепляется от глобина при разложении эритроцитов. Чрезмерное разрушение эритроцитов приведет к накоплению чрезмерного билирубина в крови. Билирубин — это желтоватый пигмент, высокий уровень которого в крови может проявляться пожелтением кожи.
Под микроскопом: кровь | Управление науки и общества
Кровь человека содержит множество различных компонентов, от лейкоцитов до тромбоцитов, но наиболее распространенным компонентом, безусловно, являются эритроциты.
Более известные как эритроциты, красные кровяные тельца составляют 70% клеток взрослого человека по количеству. Они служат единой цели: транспортировать кислород из легких во все другие части тела и возвращать углекислый газ в легкие для выдоха. Для этого у них есть несколько уникальных функций.
У млекопитающих, в то время как эритроциты содержат ядро и другие органеллы, прежде чем они полностью созреют, они выдавливают или выталкивают эти органеллы. Не имея ядра, красные кровяные тельца не могут создавать белки или делиться, но могут хранить гемоглобин, железосодержащую молекулу, которая связывает кислород и углекислый газ.Каждый эритроцит может содержать около 270 миллионов молекул гемоглобина, каждая из которых может связывать 4 молекулы кислорода. В общей сложности ваши эритроциты содержат около 2,5 граммов железа.
Красные кровяные тельца имеют форму пончиков, в которых не сформировано отверстие. Это двояковогнутые диски, форма которых позволяет им протискиваться через мелкие капилляры. Это также обеспечивает высокое отношение площади поверхности к объему, позволяя газам эффективно диффундировать в них и из них.
Тело взрослого человека производит около 2 единиц.4 миллиона эритроцитов каждую секунду, в основном в костном мозге. Эритроцит будет оставаться в обращении в течение 100-120 дней, совершая полный оборот тела за 60 секунд. Они транспортируют вдыхаемый кислород к клеткам и возвращают углекислый газ в легкие для выдоха.
По истечении этого периода мембрана эритроцита претерпевает изменение, которое позволяет его распознать с помощью лейкоцита, называемого макрофагом, который разрушает его. Многие компоненты, включая железо, перерабатываются и используются для производства большего количества красных кровяных телец.Основной компонент, не подлежащий вторичной переработке, распадается на билирубин, который выводится с мочой и желчью. Хотя, если вырабатывается слишком много билирубина, его желтый цвет может вызвать изменение цвета кожи, как это наблюдается при желтухе.
Окись углерода имеет в 250 раз большее сродство связывания с гемоглобином, чем с кислородом, что означает, что если присутствует какой-либо окись углерода, он будет связываться с гемоглобином, а не с кислородом. Вот почему окись углерода представляет собой такую опасность, поскольку она снижает способность нашего организма доставлять кислород нашим клеткам.По этой же причине многие курильщики испытывают одышку, поскольку окись углерода, которую они вдыхают во время курения, превосходит кислород за участки связывания гемоглобина. У заядлых курильщиков до 20% участков связывания кислорода могут быть заблокированы монооксидом углерода.
Поскольку он не имеет цвета и запаха, часто эффекты окиси углерода не замечаются, пока они не становятся действительно серьезными. Чтобы избежать пугающей ситуации, каждый дом должен быть оборудован детектором угарного газа.
@AdaMcVean
границ | От эритробластов до зрелых красных кровяных телец: клиренс органелл у млекопитающих
Введение
Зрелые эритроциты (эритроциты) являются результатом тонко регулируемого процесса, называемого эритропоэзом, который производит 2 миллиона эритроцитов каждую секунду у здоровых взрослых людей (Palis, 2014).Стандартная модель эритропоэза начинается с гемопоэтических стволовых клеток (ГСК) в костном мозге (КМ), приводящих к мультипотентным предшественникам, которые переходят к эритроид-коммитированным предшественникам в зрелые эритроциты. Эта иерархическая взаимосвязь, однако, подвергается сомнению, демонстрируя большую пластичность для потенциальных судеб клеток, с несколькими исследованиями на мышах (Adolfsson et al., 2005) и недавними новыми данными на людях (Notta et al., 2016).
Созревание из предшественников, связанных с эритроидом, называется терминальным эритропоэзом и происходит в костном мозге внутри эритробластических островков, которые состоят из центрального макрофага, окруженного эритробластами, и заканчивается в кровотоке, где ретикулоциты завершают свое созревание в течение 1-2 дней.Во время этой фазы проэритробласты (Pro-E) претерпевают морфологические изменения, такие как уменьшение размера клеток и конденсация хроматина, продуцируют специфические белки, такие как гемоглобин, и демонстрируют сниженную пролиферативную способность давать начало базофильным (Baso-E), полихроматофильным ( Поли-Е) и ортохроматофильные (Орто-Е) эритробласты последовательно. Несмотря на то, что известно несколько факторов роста, регулирующих эритропоэз, Epo является основным регулятором эритропоэза, управляющим пролиферацией и дифференцировкой предшественников эритроцитов, предотвращая апоптоз эритробластов (Koury and Bondurant, 1990; Ji et al., 2011). Взаимодействие макрофагов и эритробластов в BM является важным, поскольку макрофаги облегчают пролиферацию и дифференцировку и обеспечивают железо эритробластам (de Back et al., 2014).
В конце терминального созревания эритробласты млекопитающих вытесняют свои ядра и теряют все свои органеллы, такие как аппарат Гольджи, эндоплазматический ретикулум (ER), митохондрии и рибосомы. После изгнания его ядра созревание ретикулоцитов продолжается, теряя 20-30% поверхности клетки (Waugh et al., 1997; Da Costa et al., 2001) и устранение любых оставшихся мембраносвязанных цитозольных органелл посредством пути, объединенного с аутофагией / экзосомами (Blanc et al., 2005).
В то время как обширная литература посвящена общим механизмам эритропоэза (Palis, 2014), этот обзор фокусируется на механизмах и молекулярных акторах, участвующих во время клиренса органелл и ремоделирования мембран, чтобы продуцировать полностью функциональные двояковогнутые зрелые эритроциты. Рисунок 1 суммирует наиболее хорошо охарактеризованные этапы клиренса органелл на протяжении терминальной дифференцировки эритробластов.
Рисунок 1 . Окончательное созревание эритробластов. (A) На стадии эритробласта активируются два Ulk1-опосредованных аутофагических пути, обеспечивающих клиренс органелл: Atg5 / 7-зависимый путь с протеолитической Atg4-зависимой активацией MAPLC3, связанного с микротрубочками белка 1 светового канала 3 (LC3 ) и независимый от Atg5 / 7 путь, не связанный с белком LC3. Активация LC3 позволяет ему внедряться в мембрану фагофора, начиная поглощение органелл посредством распознавания сигнала убиквитина или путем прямого связывания специализированных рецепторов на мембране органелл.В неэритроидных клетках Rab9a важен для образования фагофора во время Atg5 / 7-независимого аутофагического пути. После образования аутофагосомы ее слияние с лизосомой позволяет расщеплять органеллы гидролитическими ферментами. В процессе энуклеации образуются пиреноциты и ретикулоциты, которые все еще содержат некоторые органеллы, которые необходимо удалить для окончательного созревания в эритроцит. (B) На этой стадии нежелательные мембранные белки, такие как рецептор трансферрина (TfR), интернализуются посредством эндоцитоза и вытесняются посредством экзоцитоза из мультивезикулярных структур тела.Двойные положительные везикулы по гликофорину A (GPA) / LC3, содержащие остатки органелл, также обнаруживаются в ретикулоцитах, что указывает на взаимодействие между путями эндоцитоза (GPA + ) и аутофагией (LC3 + ) для удаления органелл. Однако остается неизвестным, как аутофагосомы взаимодействуют с мультивезикулярными тельцами (MVB) по тому же пути рециклинга мембранных белков или отпочкования непосредственно из плазматической мембраны после слияния с эндоцитарными пузырьками.
Энуклеация
Наиболее впечатляющим аспектом эритропоэза млекопитающих является образование энуклеированных клеток.Энуклеация происходит в ортохроматических эритробластах, продуцирующих клетки двух типов: ретикулоциты и пиреноциты [ядро, окруженное крошечным слоем цитоплазмы и плазматической мембраной (ПМ)]. Пиреноциты быстро устраняются макрофагами эритробластического острова, где воздействие фосфатидилсерина действует как сигнал «съешь меня» (Yoshida et al., 2005).
Среди изменений, происходящих во время терминальной дифференцировки, для энуклеации важны остановка клеточного цикла, хроматин и ядерная конденсация, а также ядерная поляризация.Кроме того, изгнание ядра, как полагают, зависит от реорганизации адгезионных белков через PM и взаимодействия макрофагов (Lee et al., 2004; Soni et al., 2006). Фактор транскрипции KFL1 необходим для энуклеации (Parkins et al., 1995; Magor et al., 2015), регулируя экспрессию белков клеточного цикла, деацетилаз, каспаз и белков ядерных мембран (Gnanapragasam et al., 2016; Gnanapragasam and Бикер, 2017).
Конденсация ядер и хроматина необходима для энуклеации (Popova et al., 2009; Ji et al., 2010) и зависит от статуса ацетилирования гистонов h4 и h5 под контролем гистоновых ацетилтрансфераз (HATs) и гистондеацетилаз (HDACs). Соответственно, Gcn5, белок HAT, подавляется, а ацетилирование гистонов h4K9 и h5K5 снижается во время эритропоэза плода мыши. Кроме того, Gcn5 активируется c-Myc, который, как известно, снижается во время поздней фазы эритропоэза (Jayapal et al., 2010). С помощью той же модели было показано, что роль белка HDAC2 важна не только для конденсации хроматина, но и для образования сократительного актинового кольца (CAR), которое участвует в ядерном пикнозе (Ji et al., 2010). Более того, недавно было показано, что основные гистоны высвобождаются через отверстие ядра, которое индуцируется зависимым от активности каспазы 3 расщеплением ламина B и конденсацией хроматина (Gnanapragasam and Bieker, 2017).
Многие исследования демонстрируют зависимость энуклеации от клеточного цикла (Gnanapragasam and Bieker, 2017). Интересно, что индуцированный циклином фактор транскрипции E2F-2, который является прямой мишенью для KLF1 во время терминального эритропоэза, по-видимому, играет роль в энуклеации, индуцируя экспрессию CRIK (Citron Rho-взаимодействующая киназа).Вдали от своих обычных мишеней, связанных с организацией микротрубочек и цитокинезом, CRIK участвует в ядерной конденсации (Swartz et al., 2017).
Элементы цитоскелета играют важную роль в энуклеации эритробластов, действуя аналогично цитокинезу, но асимметрично. В частности, как наблюдали с помощью электронной и иммунофлуоресцентной микроскопии, актиновые филаменты (F-актин) конденсируются позади экструдированного ядра с образованием CAR. Использование цитохалазина D, ингибитора F-актина, вызывает полную блокировку энуклеации (Koury et al., 1989). Более того, образование CAR зависит от Rac1 GTPase и от mDia2, расположенного ниже эффектора Rho GTPase, поскольку подавление этих двух белков нарушает образование CAR и блокирует энуклеацию эритробластов (Ji et al., 2008).
Что касается других элементов цитоскелета, фармакологическое ингибирование виментина не влияет на энуклеацию, что согласуется с его уменьшением во время эритропоэза человека (Dellagi et al., 1983). Однако нарушение регуляции микротрубочек снижает скорость энуклеации.Микротрубочки образуют корзину вокруг ядра (Koury et al., 1989), которая смещается около PM на поздних стадиях эритробластов, указывая тем самым, что эта сеть д. Быть существенной для поляризации ядра. Недавно была показана важность молекулярного моторного динеина, который обеспечивает однонаправленное движение к минус-концу микротрубочек. Кроме того, активность PI3K индуцируется полимерами микротрубочек, улучшает эффективность поляризации и способствует перемещению ядер. Однако ингибирование PI3K не блокирует, а только задерживает энуклеацию мышей (Wang et al., 2012).
В 2010 году группа Криспино наблюдала с помощью электронной микроскопии образование везикул вблизи места экструзии ядра как в первичных мышиных, так и в человеческих эритробластах, предполагая, что другой механизм способствует энуклеации. Кроме того, как показывает генетическая инвалидность, клатрин необходим для образования пузырьков (Keerthivasan et al., 2010). Совсем недавно было показано, что сурвивин необходим для энуклеации эритробластов, но вместо воздействия на цитокинез через хромосомный пассажирский комплекс, сурвивин способствует энуклеации посредством взаимодействия с EPS15 и клатрином (Keerthivasan et al., 2012).
Очевидно, мы все еще находимся в начале раскрытия молекулярных игроков, участвующих в процессе энуклеации. Более того, как показано в Таблице 1, большинство молекулярных игроков было идентифицировано у мышей, и у нас все еще отсутствует демонстрация того, что эти игроки также участвуют в эритропоэзе человека.
Таблица 1 . Сравнение исследований на эритроидных клетках человека или мышей или на других клеточных моделях.
Митохондриальный зазор
Основным механизмом клиренса митохондрий является митофагия, селективный тип аутофагии, который делает возможной деградацию поврежденных митохондрий.Важность этого процесса подчеркивается знанием того, что нарушение функции митохондрий вызывает увеличение продукции активных форм кислорода, что, в свою очередь, может вызвать повреждение клеточных компонентов (белков, нуклеиновых кислот и липидов) и вызвать гибель клеток (Lee et al. ., 2012).
Во время регулярных процессов аутофагии стресс или недостаток питательных веществ активирует APM-активированную протеинкиназу (AMPK), запуская два убиквитин-зависимых пути (рис. 1A). Один из них позволяет собирать фагофор и включает несколько белков, связанных с аутофагией (Atg), таких как Atg5 и Atg7.Другой нацелен на активацию и липидирование LC3 (MAPLC3, связанный с микротрубочками белок 1 световой канал 3) с помощью Atg4, белка, регулируемого окислительно-восстановительным процессом. Atg4 и Atg7 кооперируются, чтобы конъюгировать LC3 с фосфатидилэтаноламином в липидном бислое мембраны, происходящем из сайта контакта ER-митохондрий (Tooze and Yoshimori, 2010; Hamasaki et al., 2013). Затем удлиненный фагофор привлекается для поглощения мишеней через адаптерные белки, содержащие LC3-взаимодействующую область (LIR), которая формирует аутофагосому с двойной мембраной, которая сливается с лизосомой, инициируя деградацию компонентов аутофагосомы.
При повреждении или деполяризации митохондрий белки митохондриальной мембраны обнажаются и действуют как маяк для рекрутирования мембран фагофоров (Liu et al., 2014). Примером является PINK1 (P-TEN-индуцированная киназа 1) рекрутирование Паркина. После деполяризации митохондрий PINK1 накапливается в OMM (внешней митохондриальной мембране) и вызывает митохондриальную транслокацию паркина, убиквитинлигазы E3 типа RBR (промежуточное кольцо) путем прямого фосфорилирования (Kim et al., 2008; Нарендра и др., 2010). Стабилизация Parkin в OMM ведет к полиубиквитинированию многих белков, вызывая деление митохондрий и остановку подвижности, а также рекрутирование фагофоров за счет взаимодействия с p62 / SQSTM1, белком, содержащим LIR (Geisler et al., 2010). В отличие от обычной индукции митофагии, целевые митохондрии во время созревания эритробластов полностью функциональны. BNIP3L / NIX, интегральный белок OMM, содержащий только Bh4, впервые идентифицированный в ретикулоцитах мыши, по-видимому, является основным митохондриальным белком, участвующим во время терминальной дифференцировки (Schweers et al., 2007; Сандовал и др., 2008). Этот белок активируется во время эритропоэза и вызывает деполяризацию митохондриальной мембраны и конъюгированный с мембраной рекрутинг LC3 в митохондрии (Aerbajinai et al., 2003; Novak et al., 2010). Действие Nix не опосредуется его доменом Bh4, а скорее, по-видимому, обусловлено цитоплазматическим коротким линейным мотивом, действующим как клеточный сигнал для рекрутирования др. Белков (Zhang et al., 2012). Однако до сих пор неизвестно, активирует ли индуцированная Nix деполяризация митохондрий паркин-зависимый путь (Yuan et al., 2017).
Недавно было обнаружено, что другие митохондриальные рецепторы участвуют в митофагии, такие как FUNDC1, индуцированная MARCH5, убиквитинлигазой E3, действующей в условиях гипоксии (Chen et al., 2017), Bcl2-L-13 (Murakawa et al., 2015 ), оптинейрин (Wong, Holzbaur, 2014) и Prohibitin 2 (Wei et al., 2017). Остается неизвестным, играют ли они роль в созревании эритроидов.
Канонические белки Atg также участвуют в терминальном созревании. В эритропоэзе человека расщепление LC3 находится под контролем эндопептидазы Atg4 и необходимо для созревания аутофагосом (Betin et al., 2013). У мышей экспрессия Ulk1 (Atg1) коррелирует с терминальной дифференцировкой и участвует в элиминации митохондрий и рибосом (Chan et al., 2007; Kundu et al., 2008). Зависимый от убиквитинирования путь также играет роль в созревании ретикулоцитов, но не является существенным. В самом деле, в ретикулоцитах Atg7 — / — клиренс митохондрий затрагивается лишь частично (Zhang and Ney, 2009; Zhang et al., 2009). Однако активация Nix и Ulk1, по-видимому, важна (Mortensen et al., 2010; Honda et al., 2014), подтверждая сосуществование как Atg5 / Atg7-зависимых, так и независимых путей во время терминальной дифференцировки.
Некоторые исследования подтверждают, что Atg5 / 7-независимая деградация митохондрий вовлекает эндосомные регулирующие Rab белки. Аутофагосомы, сформированные Ulk1-зависимым путем, сливаются с происходящими из Гольджи везикулами и поздними эндосомами Rab9a-зависимым образом, прежде чем они нацелены на лизосомы (Wang et al., 2016). Интересно, что недавно было показано, что Rab-белки участвуют в удалении митохондрий по полному независимому от аутофагии пути.Деполяризованные митохондрии, по-видимому, поглощаются Rab5-положительными эндосомами, которые созревают в Rab7-положительные поздние эндосомы, а затем сливаются с лизосомами (Hammerling et al., 2017a, b). В отличие от канонической аутофагии, которая включает окружение украшенной убиквитином мишени двойной мембранной структурой, все митохондрии, по-видимому, поглощаются ранней инвагинацией эндосомной мембраны посредством аппарата ESCRT. Неизвестно, может ли это происходить и в созревающих эритробластах.
Митофагия, по-видимому, также регулируется транскрипцией.Действительно, гемин-зависимая дифференцировка линии эритроидных клеток демонстрирует особенности митофагии (Fader et al., 2016). Фактор транскрипции NF-E2, участвующий в экспрессии гена глобина, также регулирует митофагию посредством регуляции генов Nix и Ulk1 (Gothwal et al., 2016; Lupo et al., 2016). Другим ключевым регулятором является регуляторный каскад KRAB / KAP1-miRNA, который действует как непрямой репрессор генов митофагии у мышей, а также в клетках человека, вероятно, посредством понижающей и повышающей регуляции ряда miRNA, таких как miR-351, которая нацелен на Nix (Barde et al., 2013).
Параллельно аутофагическому пути, цитозольная деградация, по-видимому, происходит во время созревания ретикулоцитов. 15-липоксигеназа (15-LOX), фермент, катализирующий диоксигенацию полиненасыщенных жирных кислот, трансляционно ингибируется до стадии ретикулоцитов и действует, повышая проницаемость мембран органелл, обеспечивая доступ протеасом и их деградацию. Интересно, что затрагивается только элиминация митохондрий, в то время как клиренс рибосом остается эффективным при использовании ингибитора липоксигеназы (Grüllich et al., 2001). Этот механизм все еще остается спорным, поскольку 15-LOX может также действовать в пути аутофагии как разрушитель градиента pH OMM, который может вызывать митофагию (Vijayvergiya et al., 2004), и на окисление фосфолипидов, конъюгированных с LC3, во время образования аутофагосом; даже в этом случае эти особенности, как показано в таблице 1, еще не были продемонстрированы в эритроидных клетках (Morgan et al., 2015).
Рибосомы и другие органеллы
В целом, аутофагия играет важную роль в удалении других органелл, таких как лизосомы, пероксисомы и ER.Однако в литературе представлено очень мало исследований на эритроидных клетках (таблица 1).
В то время как Nix необходим для удаления митохондрий, Ulk1 участвует в деградации рибосом и митохондрий (Schweers et al., 2007; Kundu et al., 2008; Sandoval et al., 2008). Сходным образом, эффективный клиренс рибосом и ER и ингибирование митофагии наблюдали у Atg7 — / — мышей (Mortensen et al., 2010). Эти данные предполагают, что неаутофагические или независимые от Atg7 аутофагические пути могут существовать для элиминации др. Органелл (Figure 1A).
Было высказано предположение, что в неэритроидных клетках млекопитающих пероксисомы удаляются тремя разными путями: макроаутофагией (Iwata, 2006), опосредованной 15-LOX (Yokota et al., 2001) и пероксисомными протеазами Lon (Yokota et al. , 2008). Более того, аутофагическая деградация лизосом (лизофагия) была недавно идентифицирована в клетках HeLa, где она опосредуется убиквитинизацией и включает белок p62 (Hung et al., 2013). Сходство между пексофагией / лизофагией и митофагией в неэритроидных клетках предполагает, что пути аутофагии также могут быть вовлечены в терминальное созревание эритробластов.
После энуклеации ретикулоциты созревают в костном мозге (R1), а затем выходят в кровоток (R2) для завершения процесса. Хотя разложение органелл начинается во время энуклеации, элиминация мРНК происходит в кровотоке и опосредуется рибонуклеазами, генерируя нуклеотиды, которые расщепляются эритроидной пиримидиннуклеотидазой. Это устранение имеет решающее значение, поскольку дефицит этого фермента вызывает гемолитическую анемию (Valentine et al., 1974). мРНК в ретикулоцитах R2 в основном относятся к трем перекрывающимся категориям: транспортная, метаболическая и сигнальная трансдукция (Lee et al., 2014), и их присутствие необходимо для достижения зрелой стадии эритроцитов. Это подтверждает важность пути экзосом для окончательного созревания в эритроциты с активным удалением других субклеточных компонентов.
Экзоцитоз и ремоделирование мембран
Экзосомы — это небольшие пузырьки, которые секретируются во внеклеточную среду из различных типов клеток. Инвагинации PM образуют ранние эндосомы, которые захватывают различные мишени, формируя мультивезикулярные тела (MVB, поздние эндосомы), которые в конечном итоге сливаются с PM и высвобождают экзосомы.В ретикулоцитах этот путь, как полагают, участвует в изменении объема клетки и ремоделировании мембраны для уменьшения объема и удаления нежелательных мембранных белков. Это было впервые обнаружено в ретикулоцитах овец, где рецептор трансферрина (TfR) сначала интернализуется в маленькие пузырьки размером 100–200 нм, прежде чем попасть в MVBs (Pan et al., 1985; Johnstone et al., 1989). Этап интернализации зависит от клатрина, а деградация не зависит от лизосом и происходит путем экзоцитоза после слияния MVB с PM, как показано на рисунке 1B (Killisch et al., 1992). Этот процесс необходим для окончательного удаления других мембранных белков, которые необходимы для ретикулоцита, но отсутствуют в зрелой клетке. Такие белки, как аквапорин-1 (AQP1) (Blanc et al., 2009), интегрин α4β1 (Rieu et al., 2000), переносчик глюкозы и ацетилхолинэстараза (Johnstone et al., 1987) обнаружены в гликофорине-A (GPA). положительные эндосомы, тогда как белки цитоскелета, такие как актин или спектрин, никогда не были обнаружены в этих эндосомах (Liu et al., 2010).
Хотя множество доказательств отмечает роль аутофагии в удалении органелл во время конечного созревания, сама стадия деградации показывает несоответствия с каноническим протеолизом с участием лизосомальных белков из-за исчезновения лизосомального компартмента во время созревания и удаления LAMP2 посредством экзоцитоза (Barres et al. ., 2010). Недавно было обнаружено, что GPA-положительные эндосомы экспрессируют LC3 на мембране эндосом, что указывает на сотрудничество как аутофагии, так и экзоцитоза в удалении остаточных органелл в ретикулоцитах R2. Эти гибридные везикулы содержат митохондрии, Гольджи и лизосомы, которые могут быть образованы слиянием внешней мембраны аутофагосомы и эндосомы, происходящей из PM (Griffiths et al., 2012). Экзоцитозу этого пузырька может способствовать селезенка, так как пациенты после спленэктомии обнаруживают большие вакуоли внутри ретикулоцитов (Holroyde and Gardner, 1970).
Следует указать на важность липидных доменов, таких как холестерин и сфингомиелин-обогащенные домены, в ремоделировании PM, поскольку они обнаруживаются в обоих сайтах, специфичных для мембранных везикуляций (Leonard et al., 2017).
Заключение
Даже если все животные модели, использованные для идентификации молекулярных игроков, участвующих во время терминальной дифференцировки, демонстрируют дефекты созревания и анемию, связь между клиренсом органелл и гематологическими заболеваниями человека все еще остается в основном неизвестной.Эритроидные расстройства, такие как β-талассемия и миелодиспластический синдром (МДС), характеризуются неэффективным кроветворением, анемией, диссоциацией между пролиферацией и дифференцировкой клеток-предшественников и неэффективным удалением агрегированного белка (Arber et al., 2016; Taher et al. , 2017). Действительно, дефекты созревания ретикулоцитов и аутофагии выявляются у пациентов с HbE / β-талассемией (Lithanatudom et al., 2011; Khandros et al., 2012; Butthep et al., 2015), а дефекты энуклеации обнаруживаются у пациентов с МДС (Garderet и другие., 2010; Park et al., 2016). Нарушение аутофагии участвует в накоплении цитозольных токсичных Lyn и митохондрий, а также в задержке деградации лизосом при хорея-акантоцитозе (Lupo et al., 2016). Использование модуляторов аутофагии полезно в случае ВСС или β-талассемии (Franco et al., 2014; Jagadeeswaran et al., 2017). Более того, анемия при синдроме Пирсона недавно была связана с неполным клиренсом митохондрий из ретикулоцитов (Palis, 2014) и асинхронизацией нагрузки железом (Ahlqvist et al., 2015), в то время как у пациентов с серповидно-клеточными клетками наблюдалось накопление белков в их эритроцитах, что указывает на дефект экзосомального пути (De Franceschi, 2009; Carayon et al., 2011).
Раскрытие молекулярных механизмов и взаимодействий, определяющих терминальное созревание эритробластов, было бы бесценным в терапии гематологических заболеваний. Однако большая часть наших знаний об эритропоэзе человека основана на моделях животных и / или культивируемых ex vivo клеток-предшественников человека (Таблица 1). При интерпретации результатов следует проявлять большую осторожность, учитывая важные различия между эритропоэзом мыши и человека, а также средой in vivo, и in vitro, , как подчеркивается в обширном анализе транскриптома в исследовании терминальной дифференцировки эритроидов (An et al. ., 2014).
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Финансирование
Это исследование было поддержано грантами Лаборатории передового опыта GR-Ex, ссылка ANR-11-LABX-0051. Labex GR-Ex финансируется программой «Investissements d’avenir» Французского национального исследовательского агентства, ссылка ANR-11-IDEX-0005-02.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
MM финансируется программой исследований и инноваций Европейского Союза Horizon 2020 в рамках грантового соглашения Марии Склодовской-Кюри № 665850. Мы благодарим И. Марджинедаса-Фрейша и К. Хаттаб за полезные обсуждения.
Список литературы
Адольфссон, Дж., Монссон, Р., Буза-Видас, Н., Халтквист, А., Люба, К., Йенсен, К. Т. и др. (2005). Идентификация лимфомиелоидных стволовых клеток Flt3 +, лишенных эритромегакариоцитарного потенциала. Ячейка 121, 295–306.DOI: 10.1016 / j.cell.2005.02.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Aerbajinai, W., Giattina, M., Lee, T. Y., Raffield, M., and Miller, J. L. (2003). Проапоптотический фактор Nix коэкспрессируется с Bcl-xL во время терминальной дифференцировки эритроидов. Кровь 102, 712–717. DOI: 10.1182 / кровь-2002-11-3324
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Альквист, К. Дж., Леончини, С., Пекорелли, А., Вортманн, С.Б., Ахола, С., Форсстрём, С., и др. (2015). Мутагенез мтДНК нарушает удаление митохондрий во время созревания эритроидов, что приводит к усилению разрушения эритроцитов. Нат. Commun. 6: 6494. DOI: 10.1038 / ncomms7494
PubMed Аннотация | CrossRef Полный текст | Google Scholar
An, X., Schulz, V.P., Li, J., Wu, K., Liu, J., Xue, F., et al. (2014). Глобальный анализ транскриптома терминальной дифференцировки эритроидов человека и мыши. Кровь 123, 3466–3477.DOI: 10.1182 / кровь-2014-01-548305
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Арбер, Д. А., Орази, А., Хассерджян, Р., Тиле, Дж., Боровиц, М. Дж., Ле Бо, М. М. и др. (2016). Пересмотр 2016 г. классификации миелоидных новообразований и острого лейкоза Всемирной организации здравоохранения. Кровь 127, 2391–2405. DOI: 10.1182 / кровь-2016-03-643544
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Барде, И., Раувель, Б., Марин-Флорез, Р. М., Корсинотти, А., Лауренти, Э., Верп, С. и др. (2013). Каскад KRAB / KAP1-miRNA регулирует эритропоэз посредством стадийно-специфичного контроля митофагии. Наука 340, 350–353. DOI: 10.1126 / science.1232398
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Barres, C., Blanc, L., Bette-Bobillo, P., Andre, S., Mamoun, R., Gabius, H.-J., et al. (2010). Галектин-5 связывается с поверхностью экзосом ретикулоцитов крысы и модулирует захват везикул макрофагами. Кровь 115, 696–705. DOI: 10.1182 / кровь-2009-07-231449
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бетин, В. М. С., Синглтон, Б. К., Парсонс, С. Ф., Ансти, Д. Дж., И Лейн, Дж. Д. (2013). Аутофагия способствует очищению органелл во время дифференцировки эритробластов человека: доказательства роли паралогов ATG4 во время созревания аутофагосом. Аутофагия 9, 881–893. DOI: 10.4161 / auto.24172
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Блан, Л., Де Гассар, А., Жеминар, К., Бетти-Бобилло, П., и Видаль, М. (2005). Высвобождение экзосом ретикулоцитами — неотъемлемой частью системы дифференцировки красных кровяных телец. клеток крови. Мол. Дис. 35, 21–26. DOI: 10.1016 / j.bcmd.2005.04.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Блан, Л., Лю, Дж., Видаль, М., Часис, Дж. А., Ан, X. и Мохандас, Н. (2009). Водный канал аквапорин-1 разделяется на экзосомы во время созревания ретикулоцитов: значение для регуляции объема клеток. Кровь 114, 3928–3934. DOI: 10.1182 / кровь-2009-06-230086
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Буттеп П., Визедпаничкий Р., Джиндадамронгвех С. и Фухароен С. (2015). Повышенные уровни эритропоэтина и цитокинов связаны с нарушением созревания ретикулоцитов у пациентов с талассемией. клеток крови. Мол. Дис. 54, 170–176. DOI: 10.1016 / j.bcmd.2014.11.007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Карайон, К., Chaoui, K., Ronzier, E., Lazar, I., Bertrand-Michel, J., Roques, V., et al. (2011). Протеолипидный состав экзосом изменяется по мере созревания ретикулоцитов. J. Biol. Chem. 286, 34426–34439. DOI: 10.1074 / jbc.M111.257444
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чан, Е. Ю., Кир, С., и Туз, С. А. (2007). Скрининг кинома siRNA идентифицирует ULK1 как мультидоменный модулятор аутофагии. J. Biol. Chem. 282, 25464–25474.DOI: 10.1074 / jbc.M703663200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Да Коста, Л., Мохандас, Н., Соретте, М., Гранж, М.-Дж., Черния, Г., и Кинобер, Т. (2001). Временные различия в потере мембран приводят к различным особенностям ретикулоцитов при наследственном сфероцитозе и иммунной гемолитической анемии. Кровь 98, 2894–2899. DOI: 10.1182 / blood.V98.10.2894
PubMed Аннотация | CrossRef Полный текст | Google Scholar
де Бак, Д.З., Костова, Э. Б., ван Краай, М., ван ден Берг, Т. К., и ван Брюгген, Р. (2014). Макрофагов и красных кровяных телец; сложная история любви. Перед. Physiol. 5: 9. DOI: 10.3389 / fphys.2014.00009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Деллаги, К., Вайнченкер, В., Винчи, Г., Паулин, Д., и Бруэ, Дж. К. (1983). Изменение экспрессии промежуточных филаментов виментина во время дифференцировки кроветворных клеток человека. EMBO J. 2, 1509–1514.
PubMed Аннотация | Google Scholar
Фейдер, К. М., Саласса, Б. Н., Гроссо, Р. А., Вергара, А. Н., и Коломбо, М. И. (2016). Гемин индуцирует митофагию в клеточной линии лейкозных эритробластов: гемин индуцирует митофагию в клетках K562. Biol. Ячейка 108, 77–95. DOI: 10.1111 / boc.201500058
CrossRef Полный текст | Google Scholar
Franco, S. S., De Falco, L., Ghaffari, S., Brugnara, C., Sinclair, D. A., Matté, A., et al. (2014). Ресвератрол ускоряет созревание эритроидов за счет активации FoxO3 и уменьшает анемию у мышей с бета-талассемией. Haematologica 99, 267–275. DOI: 10.3324 / haematol.2013.0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гардерет Л., Кобари Л., Мазурье К., Де Витте К., Джарратана М.-К., Перо К. и др. (2010). Неповрежденная терминальная дифференцировка эритроидов и сохраненная способность к энуклеации в миелодиспластических клонах 5q (del): исследование на одной клетке. Haematologica 95, 398–405. DOI: 10.3324 / haematol.2009.012773
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гейслер, С., Holmström, K.M, Skujat, D., Fiesel, F.C., Rothfuss, O.C., Kahle, P.J., et al. (2010). PINK1 / Паркин-опосредованная митофагия зависит от VDAC1 и p62 / SQSTM1. Нат. Cell Biol. 12, 119–131. DOI: 10.1038 / ncb2012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гнанапрагасам, М. Н., МакГрат, К. Э., Катерман, С., Сюэ, Л., Палис, Дж., И Бикер, Дж. Дж. (2016). Выход из клеточного цикла, регулируемый EKLF / KLF1, необходим для энуклеации эритробластов. Кровь 128, 1631–1641.DOI: 10.1182 / кровь-2016-03-706671
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Готвал М., Верле Дж., Ауманн К., Циммерманн В., Грюндер А. и Пал Х. Л. (2016). Новая роль ядерного фактора эритроид 2 в созревании эритроидов путем модуляции митохондриальной аутофагии. Haematologica 101, 1054–1064. DOI: 10.3324 / haematol.2015.132589
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гриффитс, Р. Э., Купциг, С., Коган, Н., Манкелоу, Т. Дж., Бетин, В. М. С., Тракарнсанга, К. и др. (2012). Созревающие ретикулоциты усваивают плазматическую мембрану в пузырьках, содержащих гликофорин А, которые сливаются с аутофагосомами перед экзоцитозом. Кровь 119, 6296–6306. DOI: 10.1182 / кровь-2011-09-376475
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Grüllich, C., Duvoisin, R.M, Wiedmann, M., and Van Leyen, K. (2001). Ингибирование 15-липоксигеназы приводит к замедленной деградации органелл в ретикулоците. FEBS Lett. 489, 51–54. DOI: 10.1016 / S0014-5793 (01) 02080-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хамасаки М., Фурута Н., Мацуда А., Незу А., Ямамото А., Фудзита Н. и др. (2013). Аутофагосомы образуются в сайтах контакта ER-митохондрий. Nature 495, 389–393. DOI: 10.1038 / природа11910
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хаммерлинг, Б. К., Наджор, Р. Х., Кортез, М. К., Ширес, С.Э., Леон, Л. Дж., Гонсалес, Э. Р. и др. (2017a). Эндосомный путь Rab5 опосредует паркин-зависимый клиренс митохондрий. Нат. Commun. 8: 14050. DOI: 10.1038 / ncomms14050
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хаммерлинг, Б. К., Ширес, С. Е., Леон, Л. Дж., Кортез, М. К., и Густафссон, А. Б. (2017b). Выделение Rab5-положительных эндосом выявляет новый путь деградации митохондрий, используемый BNIP3 и Parkin. Малые GTPases 11, 1–8.DOI: 10.1080 / 21541248.2017.1342749
CrossRef Полный текст | Google Scholar
Холройд, К. П., и Гарднер, Ф. Х. (1970). Приобретение аутофагических вакуолей эритроцитами человека физиологическая роль селезенки. Кровь 36, 566–575.
PubMed Аннотация | Google Scholar
Хонда С., Аракава С., Нисида Ю., Ямагути Х., Исии Э. и Симидзу С. (2014). Ulk1-опосредованная Atg5-независимая макроаутофагия опосредует элиминацию митохондрий из эмбриональных ретикулоцитов. Нат. Commun. 5: 4004. DOI: 10.1038 / ncomms5004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Hung, Y.-H., Chen, L.M-W., Yang, J.-Y., and Yuan Yang, W. (2013). Пространственно-временная индукция опосредованного аутофагией оборота лизосом. Нат. Commun. 4: 2111. DOI: 10.1038 / ncomms3111
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джагадисваран, Р., Васкес, Б. А., Тируппати, М., Ганеш, Б. Б., Ибанез, В., Cui, S., et al. (2017). Фармакологическое ингибирование LSD1 и mTOR снижает задержку митохондрий и связанные с ними уровни АФК в красных кровяных тельцах при серповидно-клеточной анемии. Exp. Гематол. 50, 46–52. DOI: 10.1016 / j.exphem.2017.02.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джаяпал, С. Р., Ли, К. Л., Джи, П., Калдис, П., Лим, Б., и Лодиш, Х. Ф. (2010). Подавление Myc необходимо для терминального созревания эритроидов. J. Biol.Chem. 285, 40252–40265. DOI: 10.1074 / jbc.M110.181073
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джи П., Джаяпал С. Р. и Лодиш Х. Ф. (2008). Энуклеация культивируемых эмбриональных эритробластов мыши требует Rac GTPases и mDia2. Нат. Cell Biol. 10, 314–321. DOI: 10.1038 / ncb1693
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джи, П., Йе, В., Рамирес, Т., Мурата-Хори, М., и Лодиш, Х. Ф. (2010). Гистоновая деацетилаза 2 необходима для конденсации хроматина и последующей энуклеации культивируемых эмбриональных эритробластов мыши. Haematologica 95, 2013–2021. DOI: 10.3324 / haematol.2010.029827
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Цзи, Ю. К., Чжан, Ю. К., Ли, М. К., Ду, М. Р., Вэй, В. У. и Ли, Д. Дж. (2011). ЭПО улучшает пролиферацию и ингибирует апоптоз трофобластов и децидуальных стромальных клеток за счет активации STAT-5 и инактивации сигнала p38 на ранних сроках беременности человека. Внутр. J. Clin. Exp. Патол. 4, 765–774.
PubMed Аннотация | Google Scholar
Джонстон, Р.М., Адам, М., Хаммонд, Дж. Р., Орр, Л., и Турбид, К. (1987). Формирование пузырьков при созревании ретикулоцитов. Ассоциация активности плазматической мембраны с высвобожденными везикулами (экзосомами). J. Biol. Chem. 262, 9412–9420.
PubMed Аннотация | Google Scholar
Джонстон Р. М., Бьянкини А. и Тенг К. (1989). Созревание ретикулоцитов и высвобождение экзосом: экзосомы, содержащие рецептор трансферрина, обладают множественными функциями плазматической мембраны. Кровь 19, 1844–1851.
Google Scholar
Кеэртхивасан, Г., Лю, Х., Гамп, Дж. М., Дауди, С. Ф., Викрема, А., и Криспино, Дж. Д. (2012). Новая роль сурвивина в энуклеации эритробластов. Haematologica 97, 1471–1479. DOI: 10.3324 / haematol.2011.061093
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кеэртивасан, Г., Смолл, С., Лю, Х., Викрема, А., и Криспино, Дж. Д. (2010). Транспортировка везикул играет новую роль в энуклеации эритробластов. Кровь 116, 3331–3340. DOI: 10.1182 / кровь-2010-03-277426
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хандрос, Э., Том, К. С., Д’Суза, Дж., И Вайс, М. Дж. (2012). Интегрированные пути контроля качества белка регулируют свободный α-глобин при β-талассемии у мышей. Кровь 119, 5265–5275. DOI: 10.1182 / кровь-2011-12-397729
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Киллиш И., Штейнлайн П., Ромиш К., Hollinshead, R., Beug, H., and Griffiths, G. (1992). Характеристика ранних и поздних эндоцитарных компартментов трансферринового цикла. Антитело к рецептору трансферрина блокирует дифференцировку эритроидов, улавливая рецептор в ранней эндосоме. J. Cell Sci. 103, 211–232.
PubMed Аннотация | Google Scholar
Ким Ю., Пак Дж., Ким С., Сонг С., Квон С.-К., Ли С.-Х. и др. (2008). PINK1 контролирует митохондриальную локализацию паркина посредством прямого фосфорилирования. Biochem. Биофиз. Res. Commun. 377, 975–980. DOI: 10.1016 / j.bbrc.2008.10.104
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кобаяси И., Убукава К., Сугавара К., Асанума К., Го Ю.-М., Ямасита Дж. И др. (2016). Энуклеация эритробластов — динеин-зависимый процесс. Exp. Гематол . 44, 247–256.e12. DOI: 10.1016 / j.exphem.2015.12.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кури, С.Т., Кури, М. Дж., И Бондюран, М. К. (1989). Распределение и функция цитоскелета во время созревания и энуклеации 13 эритробластов млекопитающих. J. Cell Biol. 109, 3005–3013.
Google Scholar
Кури, М. Дж., И Бондюран, М. К. (1990). Контроль производства эритроцитов: роль запрограммированной гибели клеток (апоптоз) и эритропоэтина. Переливание 30, 673–674. DOI: 10.1046 / j.1537-2995.1990.308321.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Краусс, С.W. (2005). Реорганизация ядерной субструктуры во время поздней стадии эритропоэза является избирательной и не включает расщепление каспазой основных ядерных субструктурных белков. Кровь 106, 2200–2205. DOI: 10.1182 / кровь-2005-04-1357
CrossRef Полный текст | Google Scholar
Кюн, Х., Белкнер, Дж., И Визнер, Р. (1990). Субклеточное распределение продуктов липоксигеназы в мембранах ретикулоцитов кролика. FEBS J . 191, 221–227. DOI: 10.1111 / j.1432-1033.1990.tb19113.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Kundu, M., Lindsten, T., Yang, C.-Y., Wu, J., Zhao, F., Zhang, J., et al. (2008). Ulk1 играет критическую роль в аутофагическом очищении митохондрий и рибосом во время созревания ретикулоцитов. Кровь 112, 1493–1502. DOI: 10.1182 / кровь-2008-02-137398
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, Э., Чой, Х. С., Хван, Дж. Х., Хо, Дж. К., Чо, Ю.-H., И Бэк, Э. Дж. (2014). РНК в ретикулоцитах — это не просто мусор: она необходима на заключительных стадиях образования эритроцитов. клеток крови. Мол. Дис. 53, 1–10. DOI: 10.1016 / j.bcmd.2014.02.009
CrossRef Полный текст | Google Scholar
Ли, Дж. К.-М., Гимм, Дж. А., Ло, А. Дж., Кури, М. Дж., Краусс, С. В., Мохандас, Н. и др. (2004). Механизм сортировки белков при энуклеации эритробластов: роль цитоскелетной связности. Кровь 103, 1912–1919.DOI: 10.1182 / кровь-2003-03-0928
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Леонард К., Конрард Л., Гутманн М., Поллет Х., Каркин М., Вермилен К. и др. (2017). Вклад липидных доменов плазматической мембраны в (ре) формирование красных кровяных телец. Sci. Отчет 7: 4264. DOI: 10.1038 / s41598-017-04388-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Lithanatudom, P., Wannatung, T., Leecharoenkiat, A., Svasti, S., Fucharoen, S.и Смит Д. Р. (2011). Повышенная активация аутофагии в эритробластах β-талассемии / Hb E во время эритропоэза. Ann. Гематол. 90, 747–758. DOI: 10.1007 / s00277-010-1152-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю Дж., Го X., Мохандас Н., Часис Дж. А. и Ань X. (2010). Ремоделирование мембран при созревании ретикулоцитов. Кровь 115, 2021–2027. DOI: 10.1182 / кровь-2009-08-241182
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лупо, Ф., Тибальди, Э., Матте, А., Шарма, А. К., Брунати, А. М., Альпер, С. Л. и др. (2016). Новая молекулярная связь между дефектной аутофагией и эритроидными аномалиями при хорея-акантоцитозе. Кровь 128, 2976–2987. DOI: 10.1182 / кровь-2016-07-727321
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Магор Г. В., Таллак М. Р., Гиллиндер К. Р., Белл К. К., МакКаллум Н., Уильямс Б. и др. (2015). У новорожденных с нулевым KLF1 обнаруживается водянка плода и нарушенный транскриптом эритроида. Кровь 125, 2405–2417. DOI: 10.1182 / кровь-2014-08-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Морган, А. Х., Хаммонд, В. Дж., Сако-Накатогава, М., Осуми, Ю., Томас, К. П., Бланше, Ф. и др. (2015). Новая роль 12/15-липоксигеназы в регуляции аутофагии. Редокс Биол. 4, 40–47. DOI: 10.1016 / j.redox.2014.11.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мортенсен, М., Фергюсон, Д.Дж. П., Эдельманн, М., Кесслер, Б., Мортен, К. Дж., Комацу, М., и др. (2010). Потеря аутофагии в эритроидных клетках приводит к дефектному удалению митохондрий и тяжелой анемии in vivo . Proc. Natl. Акад. Sci.U.S.A. 107, 832–837. DOI: 10.1073 / pnas.0913170107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Муракава Т., Ямагути О., Хашимото А., Хикосо С., Такеда Т., Ока Т. и др. (2015). Bcl-2-подобный белок 13 является гомологом Atg32 млекопитающих, который опосредует митофагию и фрагментацию митохондрий. Нат. Commun. 6: 7527. DOI: 10.1038 / ncomms8527
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нарендра Д. П., Джин С. М., Танака А., Суен Д.-Ф., Готье К. А., Шен Дж. И др. (2010). PINK1 избирательно стабилизируется на поврежденных митохондриях, чтобы активировать паркин. PLoS Biol. 8: e1000298. DOI: 10.1371 / journal.pbio.1000298
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нотта, Ф., Занди, С., Такаяма, Н., Добсон, С., Ган, О.И., Уилсон, Г. и др. (2016). Четкие пути развития клонов меняют иерархию крови человека в онтогенезе. Наука 351: aab2116. DOI: 10.1126 / science.aab2116
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Новак И., Киркин В., МакЭван Д. Г., Чжан Дж., Уайлд П., Розенкноп А. и др. (2010). Nix — это селективный рецептор аутофагии для очистки митохондрий. EMBO Rep. 11, 45–51. DOI: 10.1038 / embor.2009,256
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пан Б.-Т., Тэн К., Ву К., Адам М. и Джонстон Р. М. (1985). Электронно-микроскопические доказательства экстернализации рецептора трансферрина в везикулярной форме в ретикулоцитах овец. J. Cell Biol. 101, 942–948. DOI: 10.1083 / jcb.101.3.942
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Панкив, С., Клаузен, Т. Х., Ламарк, Т., Брех, А., Бруун, Ж.-А., Оутцен, Х., и другие. (2007). p62 / SQSTM1 связывается непосредственно с Atg8 / LC3, облегчая деградацию убиквитинированных белковых агрегатов за счет аутофагии. J. Biol. Chem . 282, 24131–24145. DOI: 10.1074 / jbc.M702824200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Парк, С. М., Оу, Дж., Чемберлен, Л., Симоне, Т. М., Янг, Х., Вирбазиус, К.-М., и др. (2016). U2AF35 (S34F) способствует трансформации, управляя аберрантным образованием 3′-конца пре-мРНК aTG7. Мол. Ячейка 62, 479–490.DOI: 10.1016 / j.molcel.2016.04.011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Паркинс А. С., Шарп А. Х. и Оркин С. Х. (1995). Летальная β-талассемия у мышей, лишенных эритроидного фактора транскрипции CACCC EKLF. Природа 375, 318–322. DOI: 10.1038 / 375318a0
CrossRef Полный текст | Google Scholar
Попова Е.Ю., Краусс С.В., Шорт С.А., Ли Г., Виллалобос Дж., Этцелл Дж. И др. (2009). Конденсация хроматина в терминально дифференцирующихся эритробластах мышей не связана с особыми архитектурными белками, но зависит от деацетилирования гистонов. Chromosome Res. 17, 47–64. DOI: 10.1007 / s10577-008-9005-y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рье, С., Жеминар, К., Рабесандратана, Х., Сент-Мари, Дж., И Видаль, М. (2000). Экзосомы, высвобождающиеся во время созревания ретикулоцитов, связываются с фибронектином через интегрин α4β1. Eur. J. Biochem. 267, 583–590. DOI: 10.1046 / j.1432-1327.2000.01036.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сандовал, Х., Thiagarajan, P., Dasgupta, S. K., Schumacher, A., Prchal, J. T., Chen, M., et al. (2008). Существенная роль Nix в аутофагическом созревании эритроидных клеток. Nature 454, 232–235. DOI: 10.1038 / nature07006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Schweers, R. L., Zhang, J., Randall, M. S., Loyd, M. R., Li, W., Dorsey, F. C., et al. (2007). NIX необходим для запрограммированного клиренса митохондрий во время созревания ретикулоцитов. Proc. Natl.Акад. Sci. США 104, 19500–19505. DOI: 10.1073 / pnas.0708818104
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сони, С., Бала, С., Гвинн, Б., Сахр, К. Э., Петерс, Л. Л., и Ханспал, М. (2006). Отсутствие белка макрофагов эритробластов (Emp) приводит к нарушению экструзии ядер эритробластов. J. Biol. Chem. 281, 20181–20189. DOI: 10.1074 / jbc.M603226200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шварц, К.Л., Вуд, С. Н., Мурти, Т., Рамирес, О., Цинь, Г., Пиллаи, М. М. и др. (2017). E2F-2 способствует ядерной конденсации и энуклеации терминально дифференцированных эритробластов. Мол. Клетка. Биол. 37: e00274 – e00216. DOI: 10.1128 / MCB.00274-16
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тахер, А. Т., Уизералл, Д. Дж., И Каппеллини, М. Д. (2017). Талассемия. Ланцет. DOI: 10.1016 / S0140-6736 (17) 31822-6. [Epub перед печатью].
CrossRef Полный текст | Google Scholar
Валентин, В.Н., Финк, К., Палья, Д. Э., Харрис, С. Р., и Адамс, В. С. (1974). Наследственная гемолитическая анемия с недостаточностью пиримидин-5′-нуклеотидазы в эритроцитах человека. J. Clin. Вкладывать деньги. 54, 866–879. DOI: 10.1172 / JCI107826
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Виджайвергия, К., Де Анжелис, Д., Вальтер, М., Кюн, Х., Дувуазен, Р. М., Смит, Д. Х. и др. (2004). Высокий уровень экспрессии кроличьей 15-липоксигеназы вызывает коллапс митохондриального градиента pH в культуре клеток. Биохимия 43, 15296–15302. DOI: 10.1021 / bi048745v
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wang, J., Fang, Y., Yan, L., Yuan, N., Zhang, S., Xu, L., et al. (2016). Клетки эритролейкемии приобретают альтернативную способность к митофагии. Sci. Реп. 6: 24641. DOI: 10.1038 / srep24641
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Дж., Рамирес, Т., Джи, П., Джаяпал, С. Р., Лодиш, Х. Ф., и Мурата-Хори, М.(2012). Энуклеация эритробластов млекопитающих требует PI3K-зависимой поляризации клеток. J. Cell Sci. 125, 340–349. DOI: 10.1242 / jcs.088286
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Во, Р. Э., МакКенни, Дж. Б., Баузерман, Р. Г., Брукс, Д. М., Валери, К. Р., и Снайдер, Л. М. (1997). Площадь и объем поверхности изменяются при созревании ретикулоцитов в кровообращении павиана. J. Lab. Clin. Med. 129, 527–535. DOI: 10.1016 / S0022-2143 (97) -X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вэй, Ю., Чанг, В.-К., Самптер, Р., Мишра, П., и Левин, Б. (2017). Prohibitin 2 — рецептор митофагии внутренней митохондриальной мембраны. Ячейка 168, 224–238.e10. DOI: 10.1016 / j.cell.2016.11.042
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вейл М., Рафф М. К. и Брага В. М. (1999). Активация каспаз в терминальной дифференцировке эпидермальных кератиноцитов человека. Curr. Биол . 9, 361–365. DOI: 10.1016 / S0960-9822 (99) 80162-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вонг, Ю.К., и Хольцбаур, Э. Л. (2014). Оптинейрин — это рецептор аутофагии для поврежденных митохондрий при паркин-опосредованной митофагии, которая нарушается мутацией, связанной с БАС. Proc. Natl. Акад. Sci. США 111, E4439 – E4448. DOI: 10.1073 / pnas.1405752111
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йокота, С., Харагути, К. М., и Ода, Т. (2008). Индукция пероксисомальной лон-протеазы в печени крыс после обработки ди- (2-этилгексил) фталатом. Histochem.Cell Biol. 129, 73–83. DOI: 10.1007 / s00418-007-0328-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йокота, С., Ода, Т., и Фахими, Х. Д. (2001). Роль 15-липоксигеназы в разрушении пероксисомальной мембраны и в запрограммированной деградации пероксисом в нормальной печени крысы. J. Histochem. Cytochem. 49, 613–621. DOI: 10.1177 / 002215540104
8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йошида, Х., Каване, К., Койке, М., Мори, Ю., Учияма, Ю., и Нагата, С. (2005). Фосфатидилсерин-зависимое поглощение макрофагами ядер из клеток-предшественников эритроидов. Nature 437, 754–758. DOI: 10.1038 / nature03964
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Yuan, Y., Zheng, Y., Zhang, X., Chen, Y., Wu, X., Wu, J., et al. (2017). BNIP3L / NIX-опосредованная митофагия защищает от ишемического повреждения мозга независимо от PARK2. Аутофагия 13, 1754–1766.DOI: 10.1080 / 15548627.2017.1357792
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжан Дж., Лойд М. Р., Рэндалл М. С., Уодделл М. Б., Кривацки Р. В. и Ней П. А. (2012). Короткий линейный мотив в BNIP3L (NIX) обеспечивает клиренс митохондрий в ретикулоцитах. Аутофагия 8, 1325–1332. DOI: 10.4161 / auto.20764
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжан Дж. И Ней П. (2009). Зависимые и независимые от аутофагии механизмы клиренса митохондрий во время созревания ретикулоцитов. Аутофагия 5, 1064–1065. DOI: 10.4161 / auto.5.7.9749
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Zhang, J., Randall, M. S., Loyd, M. R., Dorsey, F. C., Kundu, M., Cleveland, J. L., et al. (2009). Клиренс митохондрий регулируется Atg7-зависимыми и независимыми механизмами во время созревания ретикулоцитов. Кровь 114, 157–164. DOI: 10.1182 / кровь-2008-04-151639
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16.2A: Анатомия эритроцитов — Medicine LibreTexts
- Последнее обновление
- Сохранить как PDF
- Внешняя структура
- Внутренняя структура
- Ключевые моменты
- Ключевые термины
Цели обучения
- Схема анатомии эритроцита (эритроцита или эритроцита)
Человеческие эритроциты или красные кровяные тельца (эритроциты) являются основным клеточным компонентом крови.Они участвуют в транспортировке кислорода по телу и имеют особенности, которые отличают их от всех других типов клеток человека. Взрослые люди имеют примерно 20-30 триллионов эритроцитов в любой момент времени, что составляет примерно четверть от общего количества клеток человека.
Внешняя конструкция
Эритроциты : эритроциты человека (6–8 мкм)
RBC имеют форму диска с более плоским вогнутым центром. Эта двояковогнутая форма позволяет клеткам плавно проходить через самые узкие кровеносные сосуды.Газообмен с тканями происходит в капиллярах, крошечных кровеносных сосудах шириной всего в одну клетку. Многие эритроциты шире капилляров, но их форма обеспечивает необходимую гибкость для проталкивания.
Типичные эритроциты человека имеют диаметр диска 6–8 микрометров и толщину 2 микрометра, что намного меньше, чем у большинства других человеческих клеток. Эти клетки имеют средний объем около 90 фемтолитров (фл) с площадью поверхности около 136 квадратных микрометров. Они могут набухать до сферической формы, содержащей 150 мкл, не разрывая свою клеточную мембрану.Когда форма действительно меняется, это препятствует их способности переносить кислород или участвовать в газообмене. Это происходит у людей со сфероцитарной (сферической) анемией или серповидно-клеточной анемией.
Внутренняя структура
Хотя эритроциты считаются клетками, в них отсутствует ядро, ядерная ДНК и большинство органелл, включая эндоплазматический ретикулум и митохондрии. Следовательно, эритроциты не могут делиться или реплицироваться, как другие лабильные клетки организма. У них также отсутствуют компоненты для экспрессии генов и синтеза белков.В то время как у большинства клеток есть хемотаксические способы передвижения по телу, эритроциты переносятся по телу только за счет кровотока и давления.
Молекулы гемоглобина — самый важный компонент эритроцитов. Гемоглобин — это специализированный белок, который содержит сайт связывания для транспорта кислорода и других молекул. Характерный красный цвет эритроцитов обусловлен спектральными свойствами связывания гемических ионов железа в гемоглобине. Каждый эритроцит человека содержит приблизительно 270 миллионов этих биомолекул гемоглобина, каждая из которых несет четыре гемовые группы (отдельные белки).Гемоглобин составляет около трети от общего объема эритроцитов. Этот белок отвечает за транспортировку более 98% кислорода, а остальная часть перемещается в виде растворенных молекул через плазму.
Ключевые моменты
- Двояковогнутая форма позволяет эритроцитам изгибаться и плавно течь через капилляры тела. Это также облегчает транспортировку кислорода.
- Красные кровяные тельца считаются клетками, но у них нет ядра, ДНК и органелл, таких как эндоплазматический ретикулум или митохондрии.
- Красные кровяные тельца не могут делиться или воспроизводиться, как другие клетки тела. Они не могут самостоятельно синтезировать белки.
- Красный цвет крови обусловлен спектральными свойствами гемических ионов железа в гемоглобине.
- Каждый эритроцит человека содержит приблизительно 270 миллионов биомолекул гемоглобина, каждая из которых несет четыре гемовые группы, с которыми связывается кислород.
Ключевые термины
- железо : металлический химический элемент с атомным номером 26 и символом Fe.

