Физиология реобаза: 1. Реобаза, хронаксия и их значение в клинической практике. Хронаксиметрия.
1. Реобаза, хронаксия и их значение в клинической практике. Хронаксиметрия.
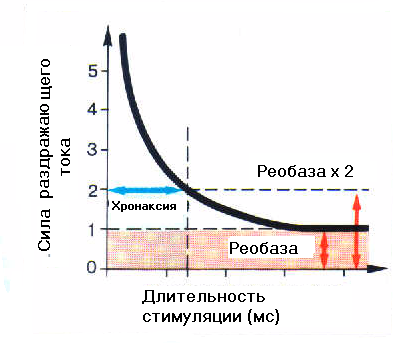
Реобаза – это минимальная сила раздражителя, вызывающая возбуждение при его действии в течение неограниченно долгого времени. На практике порог и реобаза имеют одинаковый смысл. Чем ниже порог раздражения или меньше реобаза, тем выше возбудимость ткани.
Хронаксия – это минимальное время действия раздражителя силой в две реобазы, необходимое для возникновения возбуждения. Этот параметр предложил рассчитывать Л.Лапик, для более точного определения показателя времени на кривой силы-длительности. Чем короче полезное время или хронаксия, тем выше возбудимость, и наоборот. В медицинской практике чаще всего определяется хронаксия мышц и двигательных нервов. Исследуется также хронаксия и чувствительной сферы. Хронаксия скелетных мышц человека колеблется от 0,1 до 0,7 мс. Хронаксия сгибателей у человека в 1,5-2 раза меньше хронаксии разгибателей.
Хронаксиметрия — метод, определяющий величину хронаксии, т. е. наименьшего времени, в течение которого раздражитель удвоенной пороговой силы вызовет процесс возбуждения.
Для измерения хронаксии пользуются специальным прибором — хронаксиметром, состоящим из источника постоянного тока, набора сопротивлений и приспособлений для дозировки времени действия тока, подающегося на объект. Хронаксиметрия применяется для определения дегенерации нерва при травмах различных нервных центров. Исследования хронаксии помогают установить сдвиги возбудимости при воздействии различных факторов: работы, тепла, холода, атмосферного давления и т. д.
2.Рецепторы: понятия, классификация, основные свойства и особенности возбуждения.

Существуют несколько классификаций рецепторов: По положению в организме: Экстерорецепторы — расположены на поверхности или вблизи поверхности тела и воспринимают внешние стимулы; Интерорецепторы — расположены во внутренних органах и воспринимают внутренние стимулы; Проприорецепторы — рецепторы опорно-двигательного аппарата, позволяющие определить, например, напряжение и степень растяжения мышц и сухожилий. Являются разновидностью интерорецепторов.
По способности воспринимать разные стимулы: Мономодальные — реагирующие только на один тип раздражителей; Полимодальные — реагирующие на несколько типов раздражителей
По адекватному раздражителю: Хеморецепторы — воспринимают воздействие растворенных или летучих химических веществ; Осморецепторы — воспринимают изменения осмотической концентрации жидкости ; Механорецепторы — воспринимают механические стимулы; Фоторецепторы — воспринимают видимый и ультрафиолетовый свет; Терморецепторы — воспринимают понижение (холодовые) или повышение (тепловые) температуры; Болевые рецепторы, стимуляция которых приводит к возникновению боли; Электрорецепторы — воспринимают изменения электрического поля; Магнитные рецепторы — воспринимают изменения магнитного поля.
Стимулами для разных рецепторов могут служить свет, механическая деформация, химические вещества, изменения температуры, а также изменения электрического и магнитного поля. В рецепторных клетках соответствующий сигнал изменяет конформацию чувствительных молекул-клеточных рецепторов, что приводит к изменению активности мембранных ионных рецепторов и изменению мембранного потенциала клетки.
ФИЗИОЛОГИЯ . РЕОБАЗА ХРОНОКСИЯ ПОЛЕЗНОЕ ВРЕМЯ. ФАКТОРЫ РАЗДРАЖИМОСТИ. ОСМОС
ФИЗИОЛОГ ИЯ ВОЗБУДИМ ЫХ ТКАНЕЙ М Б Ф К О З Л О В А А Л И Н А 3 . 2 . 1 1 Б ПОНЯТИЯ РАЗДРАЖИМОСТЬ И ВОЗБУДИМОСТЬ, ВОЗБУДИМЫЕ И НЕВОЗБУДИМЫЕ ТКАНИ. ЧЕМ ОТЛИЧАЕТСЯ РАЗДРАЖИМОСТЬ ОТ ВОЗБУДИМОСТИ. • Раздражимость –свойство живых организмов так или иначе реагировать на воздействия внешней среды ( т.е на стимулы / агенты / раздражители- любые факторы вызывающие ответную реакцию ) • Возбудимость – свойство клеточных мембран отвечать на действие адекватных раздражителей специфическими изменениями ионной проницаемости и мембранного потенциала. Другими словами это генерация потенциала действия. О видах раздражителей расскажу далее.. • В основе ответа лежит – возбуждение. А именно электрохимический процесс, идущий исключительно на мембране клетки , включающий изменение электрического состояния мембраны, в итоге запускающий специфическую для данной ткани ФУНКЦИЮ. • Таким образом, частным случаем раздражимости можно считать возбудимость. А ткани, клетки которых способны генерировать ПД называются – возбудимыми (нервная мышечная, секреторная ), а клетки не способные — невозбудимые (эпителиальная, соединительная) ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К РАЗДРАЖИТЕЛЯМ • ОСНОВНОЕ ТРЕБОВАНИЕ : значения параметров раздражителя должны быть достаточными для возникновения возбуждения , а именно следующие показатели • Сила раздражителя • Время, в течении которого раздражитель воздействует • Градиент нарастания силы во времени ЗАКОН СИЛЫ- ДЛИТЕЛЬНОСТИ. -ПАРАМЕТР РАЗДРАЖИТЕЛЯ-• Р – реобаза (минимальная величина раздражителя, вызывающая возбуждение) • Полезное время — (наименьшее время, в течение которого должен действовать раздражитель силой в одну реобазу, чтобы вызвать возбуждение) • Х – хронаксия (минимальное время действия раздражителя в 2 реобазы, необходимое для того, чтобы вызвать возбуждение) ЗАКОН ГРАДИЕНТА НАРАСТАНИЯ И Л И А К К О М О Д А Ц И И СИЛЫ РАЗДРАЖИТЕЛЯ — ЕЩЕ ОДИН ПАРАМЕТР РАЗДРАЖИТЕЛЯ- • Этот закон гласит, что действие раздражителя зависит не только от абсолютной величины его силы и времени действия, но и от скорости их нарастания ( крутизны) до порогового значения. Это значит, что при медленном нарастании силы тока, происходит явление аккомодации – возбудимость клетки будет снижаться .
• Раздражимость –свойство живых организмов так или иначе реагировать на воздействия внешней среды ( т.е на стимулы / агенты / раздражители- любые факторы вызывающие ответную реакцию ) • Возбудимость – свойство клеточных мембран отвечать на действие адекватных раздражителей специфическими изменениями ионной проницаемости и мембранного потенциала. Другими словами это генерация потенциала действия. О видах раздражителей расскажу далее.. • В основе ответа лежит – возбуждение. А именно электрохимический процесс, идущий исключительно на мембране клетки , включающий изменение электрического состояния мембраны, в итоге запускающий специфическую для данной ткани ФУНКЦИЮ. • Таким образом, частным случаем раздражимости можно считать возбудимость. А ткани, клетки которых способны генерировать ПД называются – возбудимыми (нервная мышечная, секреторная ), а клетки не способные — невозбудимые (эпителиальная, соединительная) ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К РАЗДРАЖИТЕЛЯМ • ОСНОВНОЕ ТРЕБОВАНИЕ : значения параметров раздражителя должны быть достаточными для возникновения возбуждения , а именно следующие показатели • Сила раздражителя • Время, в течении которого раздражитель воздействует • Градиент нарастания силы во времени ЗАКОН СИЛЫ- ДЛИТЕЛЬНОСТИ. -ПАРАМЕТР РАЗДРАЖИТЕЛЯ-• Р – реобаза (минимальная величина раздражителя, вызывающая возбуждение) • Полезное время — (наименьшее время, в течение которого должен действовать раздражитель силой в одну реобазу, чтобы вызвать возбуждение) • Х – хронаксия (минимальное время действия раздражителя в 2 реобазы, необходимое для того, чтобы вызвать возбуждение) ЗАКОН ГРАДИЕНТА НАРАСТАНИЯ И Л И А К К О М О Д А Ц И И СИЛЫ РАЗДРАЖИТЕЛЯ — ЕЩЕ ОДИН ПАРАМЕТР РАЗДРАЖИТЕЛЯ- • Этот закон гласит, что действие раздражителя зависит не только от абсолютной величины его силы и времени действия, но и от скорости их нарастания ( крутизны) до порогового значения. Это значит, что при медленном нарастании силы тока, происходит явление аккомодации – возбудимость клетки будет снижаться . Этот факт объясняется тем, что при действии медленно возрастающего раздражителя в мембране возбудимой ткани увеличивается уровень деполяризации.
Этот факт объясняется тем, что при действии медленно возрастающего раздражителя в мембране возбудимой ткани увеличивается уровень деполяризации.
Закон полярного действия электрического тока. Реобаза и хронаксия. Кривая «сила-длительность».
Все возбудимые клетки (ткани) обладают рядом общих физиологических свойств (законы раздражения), краткая характеристика которых приводится ниже. Универсальным раздражителем для возбудимых клеток является электрический ток.
Полярный закон
Деполяризация, повышение возбудимости и возникновение возбуждения происходят при действии на клетку выходящего тока. При действии входящего тока происходят противоположные изменения – гиперполяризация и снижение возбудимости, возбуждение не возникает. За направление тока принимают направление от области положительного заряда к области отрицательного заряда. При внеклеточном раздражении возбуждение возникает в области катода (–). При внутриклеточном раздражении для возникновения возбуждения необходимо, чтобы внутриклеточный электрод имел положительный знак
Реобаза и хронаксия
Методы изучения описанных явлений разнообразны. Так, о возбудимости можно судить по наименьшей силе раздражителя, необходимой для возникновения той или иной рефлекторной реакции или по пороговой силе тока или пороговому сдвигу потенциала, достаточным для возникновения ПД. Здесь необходимо ввести такие понятия, как реобаза и хронаксия. Реобаза (от греч. rheos — течение, поток и basis — ход, движение; основание), наименьшая сила постоянного электрического тока, вызывающая при достаточной длительности его действия возбуждение в живых тканях. Понятие реобазы и хронаксии ввёл в физиологию Л. Лапик в 1909, определяя зависимость между силой тока и длительностью его действия при изучении наименьшего (порогового) эффекта возбудимых тканей. Реобаза, как и хронаксия, даёт представление о возбудимости тканей и органов по порогу силы и длительности действия раздражения. Реобаза соответствует порогу раздражения и выражается в вольтах или миллиамперах.

Закон силы-длительности
Эффективность раздражителя зависит не только от силы, но и от времени его действия. Сила раздражителя, вызывающего процесс распространяющегося возбуждения, находится в обратной зависимости от длительности его действия. Графически эта закономерность выражается кривой Вейсса .
Минимальную силу раздражителя, вызывающую возбуждение, называют реобазой . Наименьшее время, в течение которого должен действовать раздражитель силой в одну реобазу, чтобы вызвать возбуждение, называют полезным временем . Для более точной характеристики возбудимости используют параметр хронаксия. Хронаксия – минимальное время действия раздражителя в 2 реобазы, необходимое для того, чтобы вызвать возбуждение.
Внимание!
Если вам нужна помощь в написании работы, то рекомендуем обратиться к профессионалам. Более 70 000 авторов готовы помочь вам прямо сейчас. Бесплатные корректировки и доработки. Узнайте стоимость своей работы.
Поможем написать любую работу на аналогичную тему
Получить выполненную работу или консультацию специалиста по вашему учебному проекту
Оценка нарушений электровозбудимости нейромышечного аппарата икроножной мышцы методом хронаксиметрической электродиагностики у пациентов с синдромом диабетической стопы
На правах рукописи
АРХИПОВ ЮРИЙ АЛЕКСАНДРОВИЧ
ОЦЕНКА НАРУШЕНИЙ ЭЛЕКТРОВОЗБУДИМОСТИ НЕЙРОМЫШЕЧНОГО АППАРАТА ИКРОНОЖНОЙ МЫШЦЫ МЕТОДОМ ХРОНАКСИМЕТРИЧЕСКОЙ ЭЛЕКТРОДИАГНОСТИКИ У ПАЦИЕНТОВ С СИНДРОМОМ ДИАБЕТИЧЕСКОЙ СТОПЫ
14. 00.16. — патологическая физиология
00.16. — патологическая физиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
НОВОСИБИРСК 2003
Работа выполнена в Научно-исследовательском институте клинической и экспериментальной лимфологии СО РАМН, г. Новосибирск.
Научный руководитель: член-корреспондент РАМН, доктор медицинских наук, профессор,
заслуженный врач Любарский Михаил Семенович
Научный консультант:
доктор медицинских наук Колпаков Михаил Аркадьевич
Официальные оппоненты:
доктор медицинских наук,
профессор Хаснулин Вячеслав Иванович
доктор медицинских наук,
профессор Ломиворотов Владимир Николаевич
Ведущая организация:
Сибирский Государственный Медицинский Университет, г. Томск
Защита диссертации состоится « » 2003 г. в
( О_часов на заседании диссертационного совета Д 001.048.dl в Научном
центре клинической и экспериментальной медицины Сибирского отделения Российской академии медицинских наук по адресу: ул. Академика Тимакова, 2, г. Новосибирск, 630117. Тел/факс 8 (3832) 33-64-56.
С диссертацией можно ознакомиться в библиотеке Научного центра клинической и экспериментальной медицины СО РАМН.
Автореферат разослан
»
2002 г.
Ученый секретарь диссертацио иного совета д.б.н.,
С.Н.Кутина
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
Денервационные нарушения, имеющие место у значительной части пациентов с сахарным диабетом, должны быть исследованы и оценены.
Это имеет огромное значение, т.к. основной причиной ранней инвалиди-зации больных сахарным диабетом, наряду с ангиопатиями, являются невропатические поражения. Одним из ключевых факторов, приводящих к поражению стоп при сахарном диабете, является периферическая невропатия (Строков И.А., с соавт, 1998). При развитии синдрома диабетической стопы возникает реальная угроза ампутации конечности, которая выполняется у больных диабетом в 15-40 раз чаще по сравнению с лицами, не страдающими этим недугом, и составляет 50-70% общего количества всех нетравматических ампутаций. Хронический характер течения сахарного диабета и высокая частота инвалидизации больных требует разработки новых подходов к их изучению, в особенности в плане лечения и профилактики (Консенсус…,1997). Ранняя диагностика невропатических осложнений и поиск новых доступных и информативных методов оценки состояния периферической иннервации при синдроме лиабетической стопы остается актуальной задачей. До сих пор единственным реально применяемым количественным методом оценки денервационных поражений остается электромиография. В то же время, по причине высокой стоимости оборудования и трудоемкости, метод не является широко используемым. К тому же большинство используемых методик травматичны и не всегда избирательны в оценке денервационных нарушений при невропатиях. По мнению многих авторов, для полноценной дифференциальной диагностики денервационных изменений в мышцах, желательна хронаксиметрическая электродиагностика. В настоящее время электродиагностика и хронаксиметрия являются одной из многих диагностических возможностей современной электромиографической аппаратуры, являясь в то же время самостоятельным методом на соответствующей аппаратной базе. Этот метод достаточно прост и относительно дешев. В то же время исследований, посвященных оценке диагностических возможностей электродиагностики при синдроме диабетической стопы явно недостаточно, а мнения авторов по поводу информативности метода иногда противоречивы. Традиционно метод называется хронаксиметрической электродиагностикой, хотя измерение хронаксии является лишь одной из возможностей этого метода. Основой данного вида исследования электровозбудимости является построение графика зависимости силы тока возбуждения от продолжительности импульса возбуждения (1Т-зави-симости). При этом обычно проводится 22 замера величины тока возбуждения при различной продолжительности импульса в диапазоне от 0,1 до 1000 мс. График имеет вид гиперболы, отражая характерные моменты элек-
Хронический характер течения сахарного диабета и высокая частота инвалидизации больных требует разработки новых подходов к их изучению, в особенности в плане лечения и профилактики (Консенсус…,1997). Ранняя диагностика невропатических осложнений и поиск новых доступных и информативных методов оценки состояния периферической иннервации при синдроме лиабетической стопы остается актуальной задачей. До сих пор единственным реально применяемым количественным методом оценки денервационных поражений остается электромиография. В то же время, по причине высокой стоимости оборудования и трудоемкости, метод не является широко используемым. К тому же большинство используемых методик травматичны и не всегда избирательны в оценке денервационных нарушений при невропатиях. По мнению многих авторов, для полноценной дифференциальной диагностики денервационных изменений в мышцах, желательна хронаксиметрическая электродиагностика. В настоящее время электродиагностика и хронаксиметрия являются одной из многих диагностических возможностей современной электромиографической аппаратуры, являясь в то же время самостоятельным методом на соответствующей аппаратной базе. Этот метод достаточно прост и относительно дешев. В то же время исследований, посвященных оценке диагностических возможностей электродиагностики при синдроме диабетической стопы явно недостаточно, а мнения авторов по поводу информативности метода иногда противоречивы. Традиционно метод называется хронаксиметрической электродиагностикой, хотя измерение хронаксии является лишь одной из возможностей этого метода. Основой данного вида исследования электровозбудимости является построение графика зависимости силы тока возбуждения от продолжительности импульса возбуждения (1Т-зави-симости). При этом обычно проводится 22 замера величины тока возбуждения при различной продолжительности импульса в диапазоне от 0,1 до 1000 мс. График имеет вид гиперболы, отражая характерные моменты элек-
тровозбудимости исследуемого нейромышечного аппарата. окив при синдроме диабетической стопы не корректна в случае превышения пороговой величины реобазы. Найдена величина этого порога.
окив при синдроме диабетической стопы не корректна в случае превышения пороговой величины реобазы. Найдена величина этого порога.
На примере использования параметров комплексной оценки 1Т- зависимости показаны дополнительные резервы электродиагностики в количественной оценке аксонопатических и миелинопатических изменений при синдроме диабетической стопы, что позволяет расширить сферу применения данного метода.
Возможно уточнение результатов хронаксиметрических исследований, выполненных авторами с превышением порога реобазы.
Возможно уточнение параметров электростимуляции, разработанных на основе хронаксиметрии с превышением порога реобазы.
Внедрение результатов исследования
Предложенный метод оценки денервационных нарушений внедрен в лечебную практику Фонда «Медсанчастть-168», клиники НИИ Клинической и Экспериментальной Лимфологии СО РАМН.
Апробация работы
Основные положения работы были доложены на межрегиональной научно-практической конференции с международным участием «Проблемы экспериментальной, клинической и профилактической лимфологии», Новосибирск, 2002; 4 съезде физиологов Сибири, Новосибирск, 2002, 12-й научно-практической конференции врачей, Новосибирск, 2002.
Публикации
По теме диссертации опубликовано 9 печатных работ.
Объем и структура диссертации
Диссертация изложена на 110 страницах, включающих обзор литературы, материалы и методы исследования, результаты собственных исследований, обсуждение полученных результатов и выводы. Список литературы включает 33 работы отечественных и 131 работу зарубежных авторов. Диссертация иллюстрирована 21 таблицами и 9 рисунками.
Данная работа является частью комплексного исследования, проводимого в Институте клинической и экспериментальной лимфологии СО РАМН по теме № 01.9.60 001180 «Разработка новых способов диагностики, профилактики и лечения хирургической, терапевтической и гинекологической патологии с позиции современной лимфологии» под руководством академика РАМН, доктора медицинских наук, профессора Ю. И. Бородина.
И. Бородина.
МАТЕРИАЛЫ И МЕТОДЫ
Клиническая характеристика больных
В группу исследования были включены 122 пациента, страдающих сахарным диабетом II типа, с синдромом диабетической стопы смешанной формы. Сахарный диабет средней степени тяжести был отмечен у 53 (43,4%) пациентов, у 69 (56,6%) пациентов наблюдалось тяжелое течение сахарного диабета.
Женщин — 84 (69 %), мужчин — 38 (31%), возраст от 19 до 80 лет, средний возраст — 61 год. Давность заболевания составила от 5-ти до 12-ти лет. Анализировались результаты 450 электродиагностических исследований, полученных при их обследовании до и после лечения.
Из них были сформированы две группы :
NU группа — результаты электродиагностики на конечностях без язвенных проявлений:
102 пациента — (404 случаев электродиагностики),
и группа — результаты электродиагностики на конечностях с язвенными проявлениями:
20 пациентов — (46″случаевэлектродиагностики).-‘————————— ——
Группа сравнения:
N группа — 64 электродиагностических исследования 32-х испытуемых (21 женщина и И мужчин) без клинических признаков сахарного диабета, сосудистой и неврологической симптоматики. Возраст от 19 до 67 лет, средний возраст 56 лет.
В пределах N11 и и групп были сформированы три подгруппы в соответствии с величиной реобазы. С целью решения задач данного исследования был использован следующий вариант группировки:
• 1-я подгруппа: случаи с реобазой до 9 мА,
• 2-я подгруппа: случаи с реобазой от 10 до 13мА
• 3-я подгруппа: случаи с реобазой, превышающей 13мА;
Методы лечения
Традиционную консервативную терапию по поводу смешанной формы синдрома диабетической стопы получали все пациенты, вошедшие в данное исследование. Все пациенты получали пероральные сахароснижающие препараты для достижения оптимального уровня гликемии. Для улучшения реологических свойств крови всем больным назначалось внутривенное капельное введение трентала.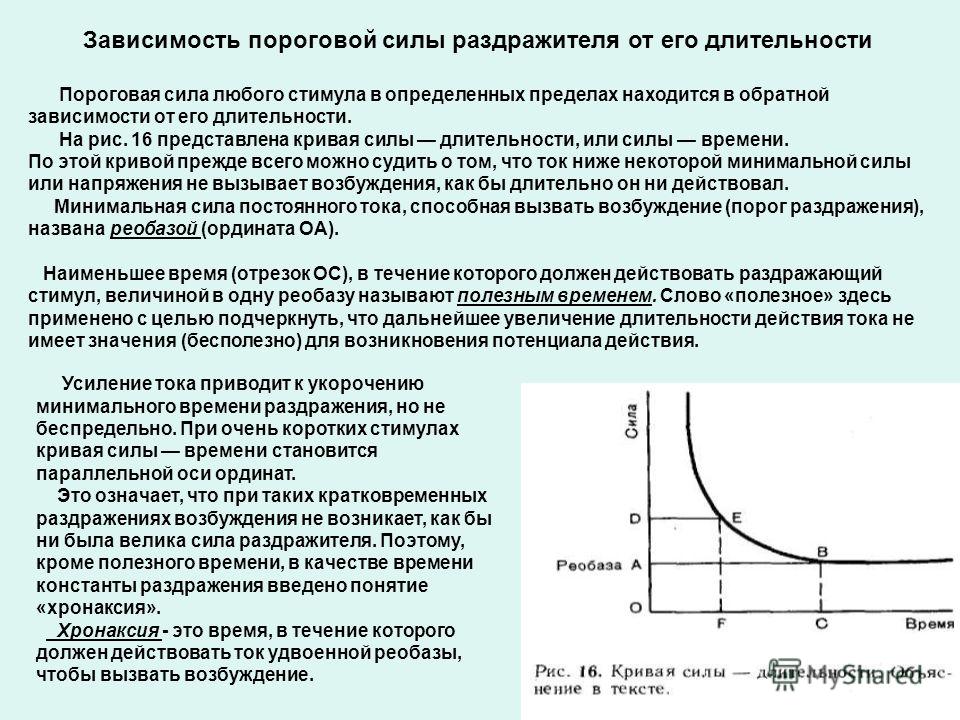 иБ. Диагностика электровозбудимости проводилась на обеих нижних конечностях, до и после проводимого курса лечения по стандартной методике (Гуляев В.Ю., и соавт. 2000, Ушаков А.А. 1996). Больной находился в положении лежа на животе, анод (резиновый электрод площадью 50 см. кв. с влажной вискозной прокладкой) располагался на коже задней поверхности коленного сгиба, катод (металлический точечный электрод площадью 1,5см. кв. с вискозной прокладкой) располагался на задней поверхности средней трети голени, в двигательной точке ш.5о1еи5. На аппарате РЬузютей-ехреП исследование сократительной способности мышц проводится с помощью последовательных одиночных импульсов электрического тока прямоугольной формы длительностью 1000700-500-300-200-150-100-70-50-30-20-10-7-5-3-2-1 -0,7-0,5-0,3-0,2-0,1 мс. На графике по оси абсцисс откладывают длительность импульсов, а по оси ор-
иБ. Диагностика электровозбудимости проводилась на обеих нижних конечностях, до и после проводимого курса лечения по стандартной методике (Гуляев В.Ю., и соавт. 2000, Ушаков А.А. 1996). Больной находился в положении лежа на животе, анод (резиновый электрод площадью 50 см. кв. с влажной вискозной прокладкой) располагался на коже задней поверхности коленного сгиба, катод (металлический точечный электрод площадью 1,5см. кв. с вискозной прокладкой) располагался на задней поверхности средней трети голени, в двигательной точке ш.5о1еи5. На аппарате РЬузютей-ехреП исследование сократительной способности мышц проводится с помощью последовательных одиночных импульсов электрического тока прямоугольной формы длительностью 1000700-500-300-200-150-100-70-50-30-20-10-7-5-3-2-1 -0,7-0,5-0,3-0,2-0,1 мс. На графике по оси абсцисс откладывают длительность импульсов, а по оси ор-
динат — значения пороговой силы тока. Полученная кривая имеет вид гиперболической регрессии и отражает обратную зависимость между пороговой силой тока, необходимой для получения мышечного сокращения, и длительностью импульса.
Основным моментом хронаксиметрической электродиагностики является определение величины реобазы (пороговой силы тока, при которой наступает мышечное сокращение) и хронаксии.
Хронаксия (время возбуждения) — это минимальная длительность импульса тока прямоугольной формы, необходимая для получения минимального сокращения исследуемой мышцы при силе тока, равной двум реобазам.
Исследование происходит в несколько этапов:
J- определение реобазы,
2- построение кривой «сила — длительность»,
3- нахождение величины хронаксии, являющейся решающим звеном в установлении степени денервационных изменений нейромы-шечного аппарата.
По данным И.С.Беритова (1959) и G.Bourguignon (1926) хронаксия крупных скелетных мышц составляет 0.2 — 1мс, с увеличением степени поражения нейромышечного аппарата величина хронаксии возрастает, достигая 1-5мс при количественных поражениях нейромышечного аппарата, 5-Юме -при реакции перерождения (РП) типа А, 10-50мс — при РП типа Б, и более 50мс — при полной РП. Средняя величина реобазы для скелетных мышц человека по данным A.A. Ушакова (1996) составляет 4 мА, по данным Б.М.Гехт(1990) — 4 — 8 мА.
Средняя величина реобазы для скелетных мышц человека по данным A.A. Ушакова (1996) составляет 4 мА, по данным Б.М.Гехт(1990) — 4 — 8 мА.
Статистическая обработка полученных данных
Полученные результаты подвергались статистической обработке с вычислением средней арифметической (М) и стандартной ошибки средней арифметической (ш). Достоверность различий сравниваемых параметров рассчитывалась с использованием критерия Стьюдента и величины нормированного отклонения Z (Лакин Г.Ф., 1980, Иванов Ю.И., Погорелюк О.Н., 1990). Различия считались значимыми при р < 0,05 и малозначимыми при р < 0,1. Оценка значимости различий долей выборок производилась по методу углового преобразования Фишера (Гублер В.Е. ¡978). Информативность исследуемых признаков оценивалась с использованием информационной меры Кульбака (Гублер В.Е. 1978) по формуле:
где J(xij) — информативность всего признака, представляющая сумму _____информативностей всех его диапазонов,
1 л 1 „PiXij / Al) — диагностический коэффициент диапазона признака, hP(X,j/Ai)
P(Xij/А\) — вероятность (частость) диапазона признака в выборке А\,
P(Xij! Al) — вероятность (частость) диапазона признака в выборке Al.
Расчеты производились на персональном компьютере с использованием пакета статистических программ «Microsoft Excel’2000».
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Хронаксией называют минимальное время, в течение которого должен действовать раздражитель удвоенной реобазы, чтобы вызвать возбуждение. Считается, что использование этого критерия позволяет точно измерить временные характеристики возбудимых структур, поскольку измерение происходит на крутом изгибе графика зависимости силы тока возбуждения от продолжительности импульса возбуждения (Покровский В.М., Коротько Г.Ф., и др. 1997).
Сам график имеет вид гиперболы и называется IT-кривой или графиком IT-зависимости (рис.1). Хронаксия является количественным показателем функциональной лабильности ткани. Установлено, что форма кривой, характеризующей возбудимость ткани в зависимости от силы и длительное ги действия раздражителя, однотипна для самых разнообразных тканей, а отличаются возбудимые ткани друг от друга только временной константой раздражения. Известно, что различные причины внутреннего и внешнего характера могут приводить к изменению свойств возбудимых тканей и отражаться изменением характера IT- зависимости. В частности сегментарная демиелинизация и аксональная дегенерация, характерные для диабетических невропатий, по разному отражаются на графике IT-зависимости (Гехт Б.М. 1990). Процесс демиелинизации нерва без поражения осевого цилиндра характеризуется высокими значениями реобазы с общим подъемом графика вверх без сдвига вершины гиперболы вправо. Аксональная дегенерация проявляется, прежде всего, сдвигом графика вправо, приводя к высоким значениям хронаксии. Сочетание этих патологических процессов приводит к подъему графика вверх со сдвигом вершины гиперболы вправо. В связи с тем, что угасание ахиллова рефлекса наблюдается первым при стопе диабетика, в качестве объекта исследования была выбрана икроножная мышца.
Установлено, что форма кривой, характеризующей возбудимость ткани в зависимости от силы и длительное ги действия раздражителя, однотипна для самых разнообразных тканей, а отличаются возбудимые ткани друг от друга только временной константой раздражения. Известно, что различные причины внутреннего и внешнего характера могут приводить к изменению свойств возбудимых тканей и отражаться изменением характера IT- зависимости. В частности сегментарная демиелинизация и аксональная дегенерация, характерные для диабетических невропатий, по разному отражаются на графике IT-зависимости (Гехт Б.М. 1990). Процесс демиелинизации нерва без поражения осевого цилиндра характеризуется высокими значениями реобазы с общим подъемом графика вверх без сдвига вершины гиперболы вправо. Аксональная дегенерация проявляется, прежде всего, сдвигом графика вправо, приводя к высоким значениям хронаксии. Сочетание этих патологических процессов приводит к подъему графика вверх со сдвигом вершины гиперболы вправо. В связи с тем, что угасание ахиллова рефлекса наблюдается первым при стопе диабетика, в качестве объекта исследования была выбрана икроножная мышца.
Ниже даны определения классических параметров электродиагностики. Как известно, ими считаются реобаза и хронаксия. Классическим, но практически не применяемым после введения хроноксии параметром, является МПВД.
Рисунок 1 График 1Т зависимости « длительиост
Реобаза (КЬ) — минимальная величина электрического тока, вызывающая возбуждение при неограниченной продолжительности импульса.
МПВД — минимальная продолжительность импульса, вызывающего возбуждение при токе реобазы.
Хронаксия (СЬг) — наименьшее время действия на ткань постоянного электрического тока удвоенной реобазы.
Далее даны определения вновь предложенных и примененных в данном исследовании параметров.
ГГпип — сила тока, вызывающая возбуждение НМА при минимальной продолжительности импульса (0,1 тс).
СЛР6 — продолжительность импульса возбуждения при силе тока, превышающей реобазу на б мА.
Необходимость введения новых параметров была продиктована некото-_____
рыми практическими обстоятельствами. Было установлено, что случаи значительного снижения электровозбудимости с высокой реобазой и выраженными клиническими проявлениями невропатии, довольно часто, сопровождаются нормальными значениями хронаксии. Также было обращено внимание на парадоксальную динамику параметров электровозбудимости, когда снижение реобазы, демонстрируя положительную динамику, сопровождалось отрицательной динамикой хронаксии. Было замечено, что определяемая хронаксня соответствовала совершенно разным участкам 1Т-гиперболы в случае низких и высоких значений реобазы. Соответствующая хронаксии точка пересечения горизонтали удвоенной реобазы с графиком 1Т-зависимости, почти всегда, находилась значительно левее при высоких значениях реобазы, соответствуя нормальным величинам данного параметра. В дальнейшем было замечено, что координата довольно сложно вычисляемой вершины 1Т-гиперболы, наиболее часто, соответствовала точке пересечения графика с горизонталью, превышающей реобазу на 4 — 8мА. Наиболее близкое соответствие координат хронаксии и вершины гиперболы наблюдалось при реобазе 6мА. В связи с этим было решено применить, параллельно с хронаксиметрией, новый параметр — СЯР6, соответствующий продолжительности импульса возбуждения при силе тока, превышающей реобазу на 6мА. Данный параметр не требует громоздких вычислений, в практическом использовании так же удобен, как хронаксия. Учитывая, что способ вычисления данного параметра следует из основного требования к хронаксии отражать характерный участок в месте крутого изгиба 1Т-гиперболы, новый параметр был применен в качестве денервационного критерия с патологическим диапазоном хронаксии.
Диагностика электровозбудимости проводилась на обеих нижних конечностях, до и после проводимого курса лечения. В соответствии с требованиями обязательного медицинского страхования проводилась стандартная терапия в рамках федеральной программы «Стопа диабетика».
Во время диагностической процедуры пациент находился в положении лежа на животе, анод (резиновый электрод площадью 50см. кв. с влажной вискозной прокладкой) располагался на коже задней поверхности коленного сгиба, катод (металлический точечный электрод площадью !.5см. кв. с вискозной прокладкой) располагался на задней поверхности средней трети голени, в двигательной точке т.5о1еиз.
При электродиагностике на аппарате РЬуБютеё-ехреи исследование сократительной способности мышц проводится с помощью последовательных одиночных импульсов электрического тока прямоугольной формы длительностью от 1 ООО до 0,1 мс (всего — 22 замера).
На графике по оси абсцисс отмечалась длительность импульсов, а по оси ординат — значения пороговой силы тока. Было оценено 450 протоколов исследований икроножной мышцы при синдроме диабетической стопы..
Были сформированы три группы протоколов:
NU-группа — 404 исследования без язвенных проявлений,
U-группа — 46 исследований с язвенными осложнениями синдрома диабетической стопы.
N — группа контроля — 64 исследования у лиц без проявлений невропатии.
Ключевым моментом проведенного исследования была проверка предположения о том, что проблемы хронаксиметрии связаны с влиянием на результат величины реобазы. В целом реобаза сама по себе является важным параметром, отражая электровозбудимость мышц и нервов при неограниченной величине импульса тока и широко используется в физиологических исследованиях для оценки электровозбудимости мышц, нервов и мозговых структур. Метаболические, микроциркуляторные и невропатические изменения при сахарном диабете неизбежно приводят к изменениям электровозбудимости тканей. Известно, что в неблагоприятных условиях кровоснабжения возбудимость скелетных мышц снижается (Рыжов А.Я., Кононов A.B. 1973). Доказано, что диабетический нерв является гипоксиче-ским, а гипергликемия вызывает сдвиги в скорости проведения ионов калия (Schneider U, et al. «значений реобазы, превышение которых приводит к резкому изменению частости патологического диапазона хронаксии. Это порог 6мА, подтвердивший правильность исходных предпосылок для введения нового параметра — СЯР6, пороги 9мА и 13мА, взятые в качестве границ при разделении групп на подгруппы.
«значений реобазы, превышение которых приводит к резкому изменению частости патологического диапазона хронаксии. Это порог 6мА, подтвердивший правильность исходных предпосылок для введения нового параметра — СЯР6, пороги 9мА и 13мА, взятые в качестве границ при разделении групп на подгруппы.
В таблице 1 анализируются частоты и частости выбранных диапазонов реобазы в трех основных группах. Видно, что подгруппа с реобазой выше 13мА не встречается в группе здоровых, и в то же время в наибольшей степени представлена в группе язвенных осложнений стопы диабетика. Данный факт демонстрирует большую выраженность патофизиологических нарушений, приводящих к снижению электровозбудимости, в группе язвенных осложнений. Если принять сегментарную демиелинизацию за основную причину повышения реобазы ш.вокиз в группах стопы диабетика, можно сделать вывод о том, что данные нарушения в 1,8 раза чаще наблюдаются в группе язвенных осложнений.
Таблица I
Частоты и частости трех диапазонов реобазы в 14, N11 и II группах.
Подгруппы ЯЬ < 9 мА 9мА<Шэ< 13м А Шэ> 1 ЗмА
Группы Случаи Частота Частость Частота Частость Частота Частость
(N1 (Ю % (Ы) % %
N 64 34 53* 30 47 0 0
ии . , 404 118 30 . 185 45 101 25
и 46 11 24 15 33** 20 43***
* — достоверность различий между группами, р = 0,007 ** — достоверность различий между группами, р = 0,004 *** — достоверность различий между группами, р = 0,004
В таблице 2 представлены результаты расчета встречаемости патологического диапазона хронаксии при различной величине реобазы в группах исследования. Видна достоверная разница между всеми подгруппами, парадоксальное снижение встречаемости при высоких значениях реобазы. В группе язвенных осложнений наблюдается полное отсутствие случаев патологической хронаксии при превышении реобазой порога 13мА. Данные результаты подтверждают зависимость результатов вычисления хронаксии от величины реобазы и необходимость применения адекватных способов оценки ГГ-зависимости. ______
______
80% 70% 60% 50% 40% 30% 20% 10% 0%
СДС без язв (N10
URb до 9мА (118) . □ Rb:10• 13MA (185) MRb> 13mA{101)
-. .. — I
ТИ j
—T ■ I— I
Хрона ксия(СЬг)>1 мс
СЯРб >1мс
МПВДМОмс
ITmin>43mA
‘ сRb до 9мА (11) ——СДС с язвами (U)____
: QRb: 10 — 13мА (15>f__— — ‘
™ЯЬ>13мА(20)
Хронаксия(СЬг)>1мс СЯРб > 1мс МПВД > Юме 1Ттш>43шА
различия между подгруппами достоверны в сравнен»!! с N11 группой, р< 0.05
Рисунок 2. Встречаемость патологических диапазонов всех параметров в подгруппах с различной величиной реабазы
На встречаемость патологических диапазонов СЯР6 и МПВД величина реобазы не оказывает существенного влияния. Оба параметра значительно чаще (более чем в 2 раза) встречаются в группе язвенньГгГосложнений диа-~ бетической стопы, отражая большую выраженность метаболических, мик-роциркуляторных и невропатических нарушений в данной группе.
Интересно, что в 90 — 100% случаев наблюдается совпадение патологических значений МПВД и СЯРб. Подобный процент совпадений МПВД с хронаксией наблюдается только при величине реобазы допорогового уровня (Ш> < 9мА) Выявленная некорректность хронаксиметрии при превышении порога реобазы и столь же высокая вероятность совпадений патологического диапазона МПВД и С11Р6 подтверждает возможность применения СИР6, в качестве критерия денервации у данных групп пациентов, независимо от величины реобазы.
В этом случае выявляемость денервационных нарушений оказывается аналогичной литературным данным для данной категории пациентов, превышая в то же время хронаксиметрическую выявляемость в 2,7 раза.
С11Р6, отражая положение значимого участка крутого изгиба гиперболы, является в данном случае критерием аксональной дегенерации нейромы-шечного аппарата т.8о1еи5 при стопе диабетика. Он демонстрирует наличие аксональных поражений в безъязвенной группе в 27%, а в группе язвенных осложнений в 72% случаев (рис. 3). Превышение реобазой порога 13мА наблюдается с аналогичной частотой (25%) в безъязвенной и значительно реже (43%) в группе язвенных осложнений. Это свидетельствует о преобладании процессов аксональной дегенерации над сегментарной демиелиниза-цией при язвенных осложнениях стопы диабетика.
3). Превышение реобазой порога 13мА наблюдается с аналогичной частотой (25%) в безъязвенной и значительно реже (43%) в группе язвенных осложнений. Это свидетельствует о преобладании процессов аксональной дегенерации над сегментарной демиелиниза-цией при язвенных осложнениях стопы диабетика.
80% 70% 60% 50% 40% 30% 20% 10% 0%
СИР6>1мс
РЬ>13тА
!П 1Ми !еэ и !
тШ
СИР6>1тс при КЬ>13тА
* — различия между группами достоверны, р < 0,05 !
Рисунок 3. Встречаемость патологических диапазонов СЯР6 и ЯЬ при синдроме диабетической стопы
Вероятно, именно потеря трофического контроля, наступающая при поражении осевого цилиндра аксона, является причиной развития язвенных осложнений в данной группе пациентов. Сочетание высокой реобазы и патологических значений С11Р6, наблюдается в 7% случаев в безъязвенной и в 28% случаев в группе язвенных осложнений. Совпадение электродиагностических признаков сегментарной демиелинизации и аксональной дегенерации является проявлением более тяжелой стадии невропатии. Нарушения аксонального транспорта и потеря трофического контроля в случае преобладания процессов аксональной дегенерации, вероятно, имеет более тяжелый прогноз в развитии язвенных осложнений при синдроме диабетической стопы.
Результаты расчета информационной меры Кульбака для всех параметров представлены в таблице 3.
Таблица 3
Сравнение ииформативностей хронаксии и СЯРб при язвенных осложнениях синдрома диабетической стопы (и-группа)
Инф. мера Кульбака СЬг С11Р6 МПВД ГТпип
J{Xij) 3.554 7.765 5.980 7.848
Видно, что информативность СЯР6 и 1Ттт более чем в 2 раза превышает информативность хронаксии. Информативность МПВД несколько ниже, но также значительно превосходит хронаксию. По изменению средних величин электродиагностических параметров была проведена оценка динамики электровозбудимости т.зокиэ в результате проведенного лечения. Данные представлены в таблице 4.
Данные представлены в таблице 4.
Таблица 4
Динамика средних величин электродиагностических параметров в оценке результатов терапии диабетической стопы в N11 группе
До лечения Мер ±ошибка После лечения Мер ±ошибка Достоверность различий (р)
ЯЬ (мА) 12,1 ±0,3 11,5 ±0,2 0,003
СЬгопаху (мс) 0,6 ±0,1 0,6 ±0,1 0,841
СИР6 (мс) 2,2 ±0,3 1,6 ±0,2 0,003
МПВД (мс) 15,8 ±1,4 12,9 ± 1,1 0,003
ГГггйп (мА) 41,0 ±1,0 37,6 ±0,8 0,003
Для группы диабетической стопы без язвенных осложнений наблюдается достовернаядинамика всех параметров кроме хронаксии. Динамика параметров в и-группе представлена в таблице 5.
Таблица 5
Динамика срелних величин электродиагностических параметров в оценке результатов терапии диабетической стопы в и группе
До лечения После лечения Ъ — критерий
КЬ (мА) 14,1 + 1,4 13,4 ±1,4 0,37
СЬгопаху (мс) 2,4 ±0,4 2,2 ±0,4 0,55
СЯР6 (мс) 6,3 ±1,4 5,1 ± 1,4 0,13
МПВД (мс) 30,9 ±7,2 23,6 ±3,3 0,003
ГГгтп (мА) 54,8 ±2,9 51,5 ±3,0 0,003
Для группы язвенных осложнений стопы диабетика достоверная положительная динамика наблюдается только для параметров МПВД и 1Тгтп, отражая, вероятно, значительную представленность необратимых денерва-ционных нарушений в данной группе. В то же время положительная направленность изменений средних величин наблюдается для всех параметров. Наибольшая достоверная положительная динамика зарегистрирована для ГГтт, подтверждая высокую оценку информативности данного параметра. Результаты проведенных исследований позволяют надеяться на использование новых подходов в оценке прогноза течения невропатии и выявления ранних изменений электровозбудимости при синдроме диабетической стопы, дифференцированному назначению нейропротективных препаратов и оценке эффективности лечебных мероприятий.
выводы
1. Превышение пороговой величины реобазы (9 мА), наблюдающееся в 71 — 76% случаев электродиагностики т. зо1еиз при синдроме диабетической стопы, создает условия для некорректного применения хронаксимет-рии в качестве критерия количественной оценки денервационных нарушений при синдроме диабетической стопы.
зо1еиз при синдроме диабетической стопы, создает условия для некорректного применения хронаксимет-рии в качестве критерия количественной оценки денервационных нарушений при синдроме диабетической стопы.
2. Комплексная оценка 1Т-зависимости позволяет выявлять нарушения электровозбудимости т.5о1еи5 в 28-31% случаев диабетической стопы без язв и в 72-80% язвенных осложнений данного синдрома, что значительно превышает диагностическую эффективность хронаксиметрии (7% для группы без язв и 28% для группы язвенных осложнений).
3. Информативность предложенных к применению параметров комплексной оценки 1Т-зависимости в 1,7 — 2,2 раза превышает информативность хронаксии при синдроме диабетической стопы.
4. Патологический диапазон реобазы (ЯЬ>13мА), может быть использован в качестве критерия сегментарной демиелинизации т.Боксю при синдроме диабетической стопы. Электродиагностические признаки сегментарной демиелинизации встречаются в 43% случаев в группе язвенных осложнений, что в 1,7 раза превышает аналогичные показатели в группе диабетической стопы без язвенных осложнений (25%).
5. Патологический диапазон СИРб может быть использован в качестве критерия аксональной дегенерации т.Бокиз при синдроме диабетической стопы. Электродиагностические признаки аксональной дегенерации в группе язвенных осложнений встречаются в 72% случаев, что в 2,7 раза превышает аналогичные показатели в группе диабетической стопы без язвенных осложнений (27%).
6. Электродиагностические признаки сочетания сегментарной демиелинизации и аксональной дегенерации т.5о1еш в 4 раза чаще наблюдаются при язвенных осложнениях стопы диабетика (28%), чем при их отсутствии (7%).
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Необходимо использовать аппарат для провёдешм хронаксиметриче————
ской электродиагностики: «РЬузщтес1-ехрегЬ> или аналогичный.
2. Положение пациента и расположение электродов зависят от выбора объекта исследования. В случае электродиагностики икроножной мышцы, пациент находится в положении лежа на животе. Анод (резиновый или металлический электрод площадью 50 -100 см. кв. с влажной вискозной прокладкой) располагается на проекции нервного ствола (на задней поверхности коленного сустава), катод (металлический точечный электрод площадью 1.5см. кв. с вискозной прокладкой) располагается на задней поверхности средней трети голени, в двигательной точке т.$о1еи5.
В случае электродиагностики икроножной мышцы, пациент находится в положении лежа на животе. Анод (резиновый или металлический электрод площадью 50 -100 см. кв. с влажной вискозной прокладкой) располагается на проекции нервного ствола (на задней поверхности коленного сустава), катод (металлический точечный электрод площадью 1.5см. кв. с вискозной прокладкой) располагается на задней поверхности средней трети голени, в двигательной точке т.$о1еи5.
3. Денервационные изменения нейромышечного аппарата рекомендуется оценивать с использованием методики расчета нового электродиагностического параметра — СЯРб: Значение СЯРб равно минимальной величине продолжительности импульса при токе возбуждения, превышающего реобазу на 6 мА. Расчет параметра проводится при анализе 1Т-зависимости, выраженной в виде графика. Для этого требуется 1Т кривая, стандартно построенная по результатам электродиагностики на прямоугольных импульсах. Прибавив к величине реобазы 6 мА и проведя горизонталь, соответствующую этой величине тока, мы получим точку пересечения с графиком Независимости, координата которой на оси абсцисс соответствует величине параметра СЯРб.
4. Возможен сокращенный вариант вычисления СЯРб, который включает в себя два этапа:
• нахождение реобазы,
• определение минимальной продолжительности импульса возбуждения при токе, превышающем реобазу на 6мА.
5. Рекомендуется использование С11Р6 в качестве нового электродиагностического критерия количественной оценки денервационных изменений при стопе диабетика.
6. Использование традиционных и вновь предложенных параметров для комплексной оценки ГГ-зависимости позволяет получить высокочувствительный метод диагностики невропатических изменений, который может быть рекомендован при клинической апробации новых хирургических и терапевтических подходов при синдроме диабетической стопы.
7. Значение 1Ттт определяется путем нахождения необходимой величины тока, требующейся для возбуждения нейромышечного аппарата объекта исследования, при минимальной величине импульса (обычно при Т = 0,1 мс). Патологическим диапазоном данного параметра рекомендуется считать превышение порога 43мА при импульсе 0,1 мс. Значение МПВД определяется путем нахождения минимальной продолжительности импульса при токе реобазы (¿оответствует абсциссе крайней левой точки на горизон-
Патологическим диапазоном данного параметра рекомендуется считать превышение порога 43мА при импульсе 0,1 мс. Значение МПВД определяется путем нахождения минимальной продолжительности импульса при токе реобазы (¿оответствует абсциссе крайней левой точки на горизон-
тальной линии реобазы на графике Независимости). Патологическим диапазоном данного параметра рекомендуется считать превышение порога 10 мс.
8. Результаты настоящего исследования позволяют предположить высокую эффективность комплексной оценки Независимости не только у пациентов с диабетической стопой, но и при других заболеваниях, сопровождающихся нарушением возбудимости мышц и нервов. Рекомендуется использование данных подходов при исследовании электровозбудимости мышц и нервов в различных областях физиологии и медицины.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Ю.А.Архипов, М.А.Колпаков, Ю.В.Башкирова, P.C. Хапаев. Хронакси-метрическая электродиагностика при синдроме диабетической стопы: Актуальные вопросы современной медицины. //Тезисы докладов двенадцатой научно-практической конференции врачей 23-25 апреля 2002, СОРАМН, Новосибирская государственная медицинская академия. -С.274.
2. Морозов В.В., Архипов Ю.А., Авдонина О.Г., Хабаров Д.В., Колпаков М.А. Хронаксиметрическая электродиагностика как критерий эффективности регионарной лимфотропной терапии в лечении больных с синдромом диабетической стопы //Бюлл. СО РАМН №2. — Новосибирск, 2002 -С. 16-18.
3. Архипов Ю.А., Колпаков М.А., Любарский М.С. Длительность нагрева кожи до заданной температуры, как новый критерий оценки резервов капиллярного кровотока при синдроме диабетической стопы.// «Применение лазерной допплеровской флоуметрии в медицинской практике». Материалы IV Всероссийского симпозиума, Пущино, Моск. обл., 2002 -С. 172.
4. Архипов Ю.А., Колпаков М.А., Любарский М.С. Опыт оценки резервов капиллярного кровотока при синдроме диабетической стопы. 4 съезд физиологов Сибири. //Тез. докл. Новосибирск.- 2002- С. 17.
//Тез. докл. Новосибирск.- 2002- С. 17.
5. Архипов Ю.А., Колпаков М.А., Хапаев P.C. Хронаксиметрическая электродиагностика в оценке нарушений электровозбудимости m.soleus у пациентов с синдромом диабетической стопы. // Проблемы экспериментальной, клинической и профилактической лимфологии. Труды НИИ-КиЭЛ СОРАМН. Под ред. Ю.И. Бородина — Новосибирск, 2002 — Т.9. -С.23.
6. Архипов Ю.А., Колпаков М.А., Любарский М.С. Опыт применения хро-наксиметрической электродиагностики в оценке электровозбудимости m.soleus у пациентов с синдромом диабетической стопы // Проблемы
экспериментальной, клинической и профилактической лимфологии. Труды НИИКиЭЛ СОРАМН. Под ред._Ю.И. Бородина — Новосибирск, 2002 — Т.9. — С.24.
7. Архипов Ю.А., Колпаков М.А., Хапаев P.C. Новые подходы в оценке результатов тепловой пробы при ЛДФ исследованиях пациентов с синдромом диабетической стопы.// Проблемы экспериментальной, клинической и профилактической лимфологии. Труды НИИКиЭЛ СОРАМН. Под ред. Ю.И. Бородина — Новосибирск, 2002 — Т.9. — С.26.
8. Архипов Ю.А., Колпаков М.А., Хапаев P.C. Новые параметры хронак-смметрической электродиагностики при диабетической ангиопатии нижних конечностей.// Проблемы экспериментальной, клинической и профилактической лимфологии. Труды НИИКиЭЛ СОРАМН. Под ред. Ю.И. Бородина. Новосибирск, 2002 — Т.9. — С.28.
9. Хапаев P.C., Колпаков М.А., Архипов Ю.А., Авдонина О.Г. Динамика показателей крово- и лимфотока на фоне традиционной терапии по поводу диабетической ангиопатии.// Проблемы экспериментальной, клинической и профилактической лимфологии. Труды НИИКиЭЛ СОРАМН. Под ред. Ю.И. Бородина. Новосибирск, 2002 — Т.9. — С.373.
В чем разница между реобазой и порогом?
Отличный вопрос! Разница заключается в том, что реобаза является примером пороговой меры. Порог , как вы правильно предполагаете, представляет собой минимальную энергию (обычно уровень тока, а не напряжение, как вы предлагаете) для возбуждения нервной ткани. Порог применяется только при определенных настройках экспериментальных параметров. Эти параметры включают тип электрического стимула (например, двухфазный импульс тока), конфигурацию электрода (например, биполярное возбуждение) и длительность стимула (например, 200 микросекунд).
Порог применяется только при определенных настройках экспериментальных параметров. Эти параметры включают тип электрического стимула (например, двухфазный импульс тока), конфигурацию электрода (например, биполярное возбуждение) и длительность стимула (например, 200 микросекунд).
Реобаза — это минимальный уровень тока, необходимый для возбуждения ткани при применении бесконечно долгого стимула . Реобаза обычно определяется путем построения порогового уровня (как определено выше) как функции длительности стимула. Причиной разработки этой меры является тот факт, что возбудимые мембраны интегрируют введенный ток, поэтому в ткани накапливается заряд. Другими словами, увеличение длительности импульса уменьшает необходимый пороговый уровень тока. Следовательно, реобаза является удобной пороговой мерой, потому что она включает в себя параметр длительности стимула. Это все еще будет зависеть от таких вещей, как конфигурация электрода и форма стимула.
Функция отношения прочности к продолжительности может быть снабжена экспоненциальной убывающей величиной:
I = I th / (1-е (-t / Tsd) )
где I = пороговый уровень тока; I rh = реобаза t = длительность стимула Tsd = Tau = экспоненциальная
Вот изображение теоретической кривой силы-продолжительности, скопированной со страницы вики на rheobase. [NB: я считаю страницу вики излишне сложной].
Реобаза — это горизонтальная асимптота. Часто используемым параметром для характеристики функции является хронакси, то есть длительность импульса, эквивалентная удвоенной реобазе.
Объяснение, данное здесь, было взято из книги «Кохлеарные имплантаты», глава 5 «Биофизика и физиология» Аббаса и Миллера, двух ветеранов по электрофизиологии кохлеарных имплантатов. К сожалению, я не могу дать вам ссылку на PDF, поскольку у меня есть работа в печатном виде.
Законы раздражения возбудимых тканей. Реобаза, хронаксия и их значение в клинической практике
Подборка по базе: Физиология возбудимых тканей.
 docx, Биоэлектрические явления в возбудимых тканях.docx, 5fan_ru_ОБЩИЕ СВОЙСТВА ВОЗБУДИМЫХ ТКАНЕЙ.doc, Возбудимость. Параметры возбудимости. Биоэлектрические явления. , Реферат Законы сохранения в механике .docx, Закрытые повреждения мягких тканей.docx, Физиология возбудимых тканей 1.pdf, Лекция. Законы идеальных газов (2).pptx, ОСНОВНЫЕ ЗАКОНЫ МАССОПЕРЕДАЧИ.docx, Режиссура ФЭТ- Основные законы инсценирования.docx
docx, Биоэлектрические явления в возбудимых тканях.docx, 5fan_ru_ОБЩИЕ СВОЙСТВА ВОЗБУДИМЫХ ТКАНЕЙ.doc, Возбудимость. Параметры возбудимости. Биоэлектрические явления. , Реферат Законы сохранения в механике .docx, Закрытые повреждения мягких тканей.docx, Физиология возбудимых тканей 1.pdf, Лекция. Законы идеальных газов (2).pptx, ОСНОВНЫЕ ЗАКОНЫ МАССОПЕРЕДАЧИ.docx, Режиссура ФЭТ- Основные законы инсценирования.docxПеречень вопросов по кредиту 1
Возбудимые ткани, физиологические свойства возбудимых тканей. Лабильность, рефрактерность. Биоэлектрические явления в живых тканях (1 и 2 опыты Гальвани).
Законы раздражения возбудимых тканей. Реобаза, хронаксия и их значение в клинической практике.
Физиологические свойства скелетных мышц. Физиологические свойства гладких мышц, их функции, регуляция деятельности. Основные отличия в функционировании скелетных и гладких мышц.
Мембранный потенциал, его регистрация, механизм возникновения. Натрий-калиевый насос, его физиологическая роль.
Локальный ответ. Особенности местного и распространяющегося возбуждения.
Критический уровень деполяризации. Потенциал действия и его фазы, происхождение, регистрация.
Соотношение фаз возбудимости с фазами потенциала действия.
Распространение возбуждения по безмиелиновым и миелиновым нервным волокнам. Характеристика их возбудимости и лабильности. Закономерности проведения возбуждения по нервам.
Парабиоз, его фазы (Н.Е. Введенский), значение этого учения для теории и практики медицины.
Строение, классификация и функциональные свойства синапсов. Механизм и особенности передачи возбуждения в синапсах. Механизмы возбуждения, ионные механизмы ВПСП.
Тормозящие синапсы и их медиаторы. Ионные механизмы ТПСП.
Понятие о двигательной единице. Электромиография.
Виды и режимы сокращения скелетных мышц.
 Одиночное мышечное сокращение, его фазы.
Одиночное мышечное сокращение, его фазы. Суммация одиночных мышечных сокращений. Тетанус, его виды. Оптимум и пессимум силы и частоты раздражения.
Механизм мышечного сокращения и расслабления. Химические и тепловые процессы в мышце при сокращении.
Физические свойства мышц. Сила и работа мышц. Утомление мышц, теории утомления изолированной мышцы. Методы изучения.
Перечень вопросов по кредиту 2
Торможение в ЦНС (И.М Сеченов), механизмы центрального торможения. Основные виды торможения в ЦНС (постсинаптическое, пресинаптическое, реципрокное, латеральное торможение, поступательное, возвратное, торможение после возбуждения, пессимальное), их роль.
Основные свойства и особенности распространения возбуждения в ЦНС (суммация, виды суммации, конвергенция, дивергенция возбуждений, одностороннее проведение возбуждения, трансформация).
Общие принципы координационной деятельности ЦНС. Тонус нервных центров. Принцип взаимодействия нейронов ЦНС (иррадиация, мультипликация, пролонгирование возбуждения, принципы облегчения, окклюзии.).
Явление доминанты и её свойства (А.А. Ухтомский).
Проблема утомления целостного организма. Теории утомления, факторы, способствующие развитию утомления.
Гипоталамо-гипофизарная система, её роль в адаптации организма к изменениям внешней среды. Нейросекреторная функция гипоталамуса: либерины и статины. Функциональные связи гипоталамуса с гипофизом.
Общая характеристика эндокринных желез. Общие свойства и функции гормонов.
Механизмы действия гормонов. Виды взаимодействия гормонов между собой.
Основной обмен и факторы его определяющие. «Закон поверхности» Рубнера. Значение определения основного обмена для клиники.
Обмен белков, азотистый баланс. Коэффициент изнашивания Рубнера.
Биологическая ценность белков. Регуляция белкового обмена.

Обмен жиров в организме.
Обмен углеводов в организме. Регуляция уровня глюкозы в крови. Специфическое динамическое действие пищи. Правила изодинамии Рубнера.
Методы изучения энергетического обмена. Прямая калориметрия.
Непрямая колориметрия. Дыхательный коэффициент.
Центр терморегуляции. Механизмы теплообразования. Механизмы теплоотдачи. Механизмам регуляции теплопродукции и теплоотдачи.
Перечень вопросов по кредиту 3
Значение анализаторов в познании окружающей среды и организма, функциональная характеристика периферического, проводникового, коркового отделов анализаторов.
Рецепторный отдел анализаторов. Свойства и особенности рецепторов.
Классификация рецепторов. Механизм возникновения возбуждения. Функциональная мобильность.
Учение П.К. Анохина о функциональных системах, саморегуляции функций. Общие периферические и центральные узловые механизмы.
Явление торможения в ВНД. Виды торможения. Механизмы внешнего и внутреннего торможения ВНД.
Память, её виды Механизмы кратковременной памяти.
Механизмы долговременной памяти.
Мотивации. Биологические и социальные мотивации. Теории мотиваций. Роль биологических мотиваций.
Врождённые формы поведения (безусловные рефлексы и инстинкты), их значение для приспособительной деятельности организма.
Условный рефлекс как форма приспособления животных и человека к изменяющимся условиям существования. Классификация условных рефлексов. Закономерности образования и проявления условных рефлексов.
Физиологические механизмы образования условных рефлексов, их структурно-функциональная основа. Развитие представлений И.П. Павлова о механизмах формирования временных связей.
Динамический стереотип, его физиологическая сущность, значение для обучения и приобретения трудовых навыков.

Сон. Виды и фазы. Активный и пассивный сон. Физиологические механизмы сна.
Типы высшей нервной деятельности животных и человека (И.П. Павлов), их классификация, характеристика.
Особенности ВНД человека и отличие от ВНД животных. Учение И.П. Павлова о I и II сигнальных системах.
Речь. Функции речи. Функциональная асимметрия коры больших полушарий, связанная с развитием речи у человека.
1. 1. Возбудимые ткани, физиологические свойства возбудимых тканей. Лабильность, рефрактерность. Биоэлектрические явления в живых тканях (1 и 2 опыты Гальвани).
Основным свойством живых клеток является раздражимость, т.е. их
способность реагировать изменением обмена веществ в ответ на дейст¬
вие раздражителей. Возбудимость — свойство клеток отвечать на раздра¬
жение возбуждением. К возбудимым относят нервные, мышечные и не¬
которые секреторные клетки. Возбуждение — ответ ткани на ее раздраже¬
ние, проявляющийся в специфической для нее деятельности (проведе¬
ние возбуждения нервной тканью, сокращение мышцы, секреция желе¬
зы) и неспецифических реакциях (генерация потенциала действия, мета¬
болические изменения).
Одним из важных свойств живых клеток является их электрическая воз¬
будимость, т.е. способность возбуждаться в ответ на действие электриче¬
ского тока. Высокая чувствительность возбудимых тканей к действию сла¬
бого электрического тока впервые была продемонстрирована Л. Гальвани
в опытах на нервно-мышечном препарате задних лапок лягушки. Если к
нервно-мышечному препарату лягушки приложить две соединенные меж¬
ду собой пластинки из различных металлов, например медь—цинк, таким
образом, чтобы одна пластинка касалась мышцы, а другая — нерва, то
мышца сокращается (первый опыт Гальвани).
Детальный анализ результатов опытов Гальвани, проведенный Вольта,
позволил сделать другое заключение: электрический ток возникает не в жи¬
вых клетках, а в месте контакта разнородных металлов с электролитом, по¬
скольку тканевые жидкости представляют собой раствор солей.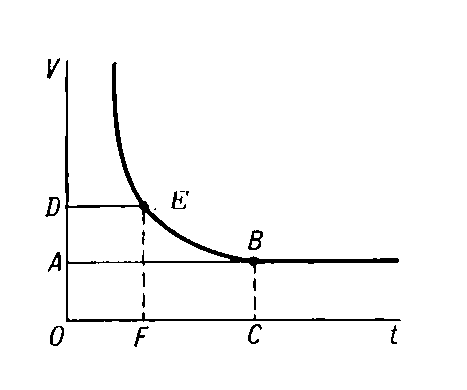 В результа¬
В результа¬
те своих исследований Вольта создал устройство, получившее название
«вольтов столб» — набор последовательно чередующихся цинковых и сереб¬
ряных пластинок, разделенных бумагой, смоченной солевым раствором. В
доказательство справедливости своей точки зрения Гальвани провел другой
опыт: набрасывал на мышцу дистальный отрезок нерва, который иннерви-
рует эту мышцу, при этом мышца также сокращалась {второй опыт Гальва¬
ни, или опыт без металла). Отсутствие металлических проводников при
проведении опыта позволило Гальвани подтвердить свою точку зрения и
развить представления о «животном электричестве», т.е. электрических яв¬
лениях, возникающих в живых тканях. Окончательное доказательство су¬
ществования электрических явлений в живых тканях было получено в опы¬
те «вторичного тетануса» Маттеуччи, в котором один нервно-мышечный
препарат возбуждался током, а биотоки сокращающейся мышцы раздража¬
ли нерв второго нервно-мышечного препарата.
Возбудимость — способность ткани отвечать на действие раздражителей переходом в активное состояние. Возбудимость характерна для нервной, мышечной и железистой тканей. Возбудимость обратно пропорциональна силе действующего раздражителя: В = 1/S. Чем больше сила действующего раздражителя, тем меньше возбудимость, и наоборот. Возбудимость зависит от состояния обменных процессов и заряда клеточной мембраны. Невозбудимость = рефрактерность. Наибольшей возбудимостью обладает нервная ткань, затем поперечно-полосатая скелетная и сердечная мышечная ткань, железистая ткань.
Проводимость — способность ткани проводить возбуждение в двух или одном направлении. Показателем проводимости является скорость проведения возбуждения (от 0,5 до 120 м/с в зависимости от ткани и строения волокна). Быстрее всего возбуждение передается по миелинизированному нервному волокну, затем по немиелинезированному волокну, и самой низкой проводимостью обладает синапс.
Для мышечной ткани характерна также сократимость. Сократимость – способность мышцы отвечать сокращением на раздражение.
Лабильность, или функциональная подвижность (Н.Е.Введенский), — это скорость протекания одного цикла возбуждения, т.е. ПД. Как видно из определения, лабильность ткани зависит от длительности ПД. Это означает, что лабильность, как и ПД, определяется скоростью перемещения ионов в клетку и из клетки, которая в свою очередь зависит от скорости изменения проницаемости клеточной мембраны. При этом особое значение имеет длительность рефрактерной фазы: чем больше рефрактерная фаза, тем ниже лабильность ткани.
Мерой лабильности является максимальное число ПД, которое ткань может воспроизвести в 1 с. В эксперименте лабильность исследуют с помощью регистрации максимального
числа ПД, которое может воспроизвести клетка при увеличении частоты ритмического раздражения.
Лабильность различных тканей существенно различается. Так, лабильность нерва равна 500—1000, мышцы — около 200, нервно-мышечного синапса — порядка 100 импульсов в секунду. Лабильность ткани понижается при длительном бездействии органа и при утомлении, а также в случае нарушения иннервации.
Следует отметить, что при постепенном увеличении частоты ритмического раздражения лабильность ткани повышается, т.е. ткань отвечает более высокой частотой возбуждения по сравнению с исходной частотой. Это явление открыто А.А.Ухтомским и называется усвоением ритма раздражения.
Абсолютная рефрактерная фаза — это полная невозбудимость клетки (возбудимость равна нулю), она соответствует пику ПД и продолжается 1—2 мс; если ПД более продолжителен, то более продолжительна и абсолютная рефрактерная фаза. Клетка в этот период времени на раздражения любой силы не отвечает. Невозбудимость клетки в фазах деполяризации и восходящей части инверсии объясняется тем, что потенциалзависимые т-ворота Na-каналов уже открыты и Na+ быстро поступает в клетку по всем открытым каналам. Те ворота Na-каналов, которые еще не успели открыться, открываются под влиянием деполяризации — уменьшения мембранного потенциала. Поэтому дополнительное раздражение клетки относительно движения Na+ в клетку ничего изменить не может. Именно поэтому ПД либо совсем не возникает при раздражении, если оно мало, либо является максимальным, если действует раздражение достаточной силы (пороговой или сверхпороговой). В период нисходящей части фазы инверсии клетка невозбудима потому, что закрываются инактивационные h-ворота Na-каналов, в результате чего клеточная мембрана непроницаема для Na+ даже при сильном раздражении. Кроме того, в этот период открываются (уже в большом количестве) К-каналы, К+ быстро выходит из клетки, обеспечивая нисходящую часть фазы инверсии и реполяризацию. Абсолютная рефрактерная фаза продолжается и в период реполяризации клетки до достижения уровня мембранного потенциала Екр ±10 мВ. Абсолютный рефрактерный период ограничивает максимальную частоту генерации ПД. Если абсолютный рефрактерный период завершается через 2 мс после начала ПД, клетка может возбуждаться с частотой максимум 500 имп/с. Существуют клетки с еще более коротким рефрактерным периодом, в которых возбуждение может в крайних случаях повторяться с частотой 1000 имп/с. С такой частотой могут возбуждаться нейроны ретикулярной формации ЦНС, толстые миелино-вые нервные волокна.
Относительная рефрактерная фаза — это период восстановления возбудимости
клетки, когда сильное раздражение может вызвать новое возбуждение (см. рис. 4.6, Б-3). Относительная рефрактерная фаза соответствует конечной части фазы реполяризации (начиная от Екр ± 10 мВ) и следовой гиперполяризации клеточной мембраны, если она имеется. Пониженная возбудимость является следствием все еще повышенной проницаемости для К+ и избыточного выхода его из клетки. Поэтому, чтобы вызвать возбуждение в этот период, необходимо приложить более сильное раздражение, так как выход К+ из клетки препятствует ее деполяризации. Кроме того, в период следовой гиперполяризации мембранный потенциал больше и, естественно, дальше отстоит от критического уровня деполяризации. Если реполяризация в конце пика ПД замедляется (см. рис. 4.4, А), то относительная рефрактерная фаза включает и период замедления реполяризации, и период гиперполяризации, т.е. продолжается до возвращения мембранного потенциала к исходному уровню после гиперполяризации. Продолжительность относительной рефрактерной фазы вариабельна, у нервных волокон она невелика и составляет несколько мс.
2. Законы раздражения возбудимых тканей. Реобаза, хронаксия и их значение в клинической практике.
Реобаза — это наименьшая сила тока, способная вызвать импульсное возбуждение. Если возбудимость ткани высока, пороговая сила раздражителя мала. Чем выше возбудимость, тем ниже пороговая сила. Большая пороговая сила свидетельствует о низкой возбудимости ткани. При внутриклеточном раздражении пороговая сила электрического тока для различных клеток равна 10-7 -10 -9 А». При медленно нарастающей силе раздражителя возбуждение может не возникнуть даже при достижении большой его силы, значительно превосходящей пороговую, вследствие развития аккомодации (снижения возбудимости и ПД вплоть до полного его отсутствия при медленно нарастающем стимуле, так как развивается инактивация №-каналов).
Важным условием, обеспечивающим возникновение возбуждения при действии раздражителя, является его длительность.
Как указывалось выше, существует определенное соотношение между
временем действия раздражителя и его амплитудой. Эта зависимость в гра¬
фическом выражении получила название кривой «сила—длительность»
(рис. 2.10). Иногда по имени авторов ее называют кривой Гоорвега—Вей-
са—Лапика. На этой кривой видно, что уменьшение значения тока ниже
определенной критической величины не приводит к возбуждению ткани
независимо от продолжительности времени, в течение которого действует
этот раздражитель, а минимальная величина тока, вызывающая возбужде¬
ние, получила название порога раздражения, или реобазы. Величина реоба¬
зы определяется разностью между критическим потенциалом и мембран¬
ным потенциалом покоя.
Хронаксия — время, в течение которого должен действо¬
вать раздражитель удвоенной реобазы, чтобы вызвать возбуждение. Ис¬
пользование этого критерия позволяет точно измерить временные харак¬
теристики возбудимых структур, поскольку измерение происходит на кру¬
том изгибе гиперболы (отрезок AD на рис. 2.10). Хронаксиметрия исполь¬
зуется при оценке функционального состояния нервно-мышечной систе¬
мы у человека. При ее органических поражениях величина хронаксии и
реобазы нервов и мышц значительно возрастает. Для измерения хронаксии пользуются специальным прибором — хронаксиметром, состоящим из источника постоянного тока, набора сопротивлений и приспособлений для дозировки времени действия тока, подающегося на объект. Хронаксиметрия применяется для определения дегенерации нерва при травмах различных нервных центров. Исследования хронаксии помогают установить сдвиги возбудимости при воздействии различных факторов: работы, тепла, холода, атмосферного давления и т. д.
Законы раздражения возбудимых тканей отражают определенную зависимость между действием раздражителя и ответной реакцией возбудимой ткани. Эта зависимость выражается законами раздражения возбудимых тканей. К законам относятся: закон силы, закон Франка-Старлинга («все или ничего»), закон Дюбуа-Раймона (закон аккомодации), закон силы-времени (силы-длительности), закон полярного действия постоянного тока, закон физиологического электротона.
Закон силы: чем больше сила раздражителя, тем больше величина ответной реакции. В соответствии с этим законом функционируют сложные структуры, например скелетная мышца. Амплитуда ее сокращений от минимальных (пороговых) величин постепенно увеличивается с увеличением силы раздражителя до субмаксимальных и максимальных значений. Это обусловлено тем, что скелетная мышца состоит из множества мышечных волокон, имеющих различную возбудимость. Поэтому на пороговые раздражители отвечают только те мышечные волокна, которые имеют самую высокую возбудимость, амплитуда мышечного сокращения при этом минимальна. С увеличением силы раздражителя в реакцию вовлекается все большее число мышечных волокон, и амплитуда сокращения мышцы все время увеличивается. Когда в реакцию вовлечены все мышечные волокна, составляющие данную мышцу, дальнейшее увеличение силы раздражителя не приводит к увеличению амплитуды сокращения.
Закон Франка-Старлинга «все или ничего»: подпороговые раздражители не вызывают ответной реакции («ничего»), на пороговые раздражители возникает максимальная ответная реакция («все»). По этому закону сокращаются сердечная мышца и одиночное мышечное волокно. Закон «все или ничего» не абсолютен. Во-первых, на раздражители подпороговой силы не возникает видимой ответной реакции, но в ткани происходят изменения мембранного потенциала покоя в виде возникновения местного возбуждения (локального ответа). Во-вторых, сердечная мышца, растянутая кровью, при наполнении ею камер сердца, реагирует по закону «все или ничего», но амплитуда ее сокращения будет больше по сравнению с сокращением сердечной мышцы нерастянутой кровью.
Закон раздражения Дюбуа-Раймона, или закон аккомодации: раздражающее действие постоянного тока зависит не только от абсолютной величины силы тока или его плотности, но и от скорости нарастания тока во времени. При действии медленно нарастающего раздражителя возбуждение не возникает, так как происходит приспосабливание возбудимой ткани к действию этого раздражителя, что получило название аккомодации. Последняя обусловлена тем, что при действии медленно нарастающего раздражителя в мембране возбудимой ткани происходит повышение критического уровня деполяризации. При снижении скорости нарастания силы раздражителя до некоторого минимального значения ПД вообще не возникает. Причина заключается в том, что деполяризация мембраны является пусковым стимулом к началу двух процессов:
быстрого, ведущего к повышению натриевой проницаемости и
обусловливающего возникновение ПД;
медленного, приводящего к инактивации натриевой проницаемости и окончанию ПД.
При быстром нарастании стимула повышение натриевой проницаемости успевает достичь значительной величины прежде, чем наступит инактивация натриевой проницаемости. При медленном нарастании тока на первый план выступают процессы инактивации, приводящие к повышению порога или к ликвидации возможности генерировать ПД вообще. Способность к аккомодации различных структур неодинакова. Наиболее высокая аккомодация — у двигательных нервных волокон, а наиболее низкая — у сердечной мышцы и гладких мышц кишечника, желудка.
Закон силы-длительности: раздражающее действие постоянного тока зависит не только от его величины, но и от времени, в течение которого он действует. Чем больше ток, тем меньше времени он должен действовать для возникновения возбуждения. Исследования зависимости силы-длительности показали, что последняя имеет гиперболический характер.
Хронаксия — это минимальное время, в течение которого нужно действовать на возбудимую ткань током в 2R, чтобы возникло возбуждение. Из этого следует, что ток ниже некоторой минимальной величины не вызывает возбуждения, как бы длительно ни действовал, и чем короче импульсы тока, тем меньшую раздражающую способность они имеют. Причиной такой зависимости является мембранная емкость. Очень «короткие» токи просто не успевают разрядить эту емкость до критического уровня деполяризации. Минимальная величина, способная вызвать возбуждение при неограниченной длительности его действий, называют реобазой. Время, в течение которого действует ток, равный 1/?, вызывающий возбуждение, называется полезным временем. В связи с тем, что определение этого времени затруднено, было введено понятие «хронаксия».
Закон полярного действия постоянного тока: при замыкании тока возбуждение возникает под катодом, а при размыкании — под анодом. Прохождение постоянного электрического тока через нервное или мышечное волокно вызывает изменение мембранного потенциала или ПП. В частности, в области приложения катода к возбудимой ткани, когда положительный потенциал на наружной стороне мембраны уменьшается, возникает деполяризация, которая быстро достигает критического уровня и вызывает возбуждение. В области приложения анода положительный потенциал на наружной стороне мембраны возрастает, происходит гиперполяризация мембраны, и возбуждение не возникает. Но при этом под анодом критический уровень деполяризации смещается к уровню ПП. Поэтому при размыкании цепи тока гиперполяризация на мембране исчезает и ПП, возвращаясь к исходной величине, достигает смещенного критического уровня — возникает возбуждение.
Закон физиологического электротона: действие постоянного тока на ткань сопровождается изменением ее возбудимости. При прохождении постоянного тока через нерв или мышцу порог раздражения под катодом и на соседних с ним участках понижается вследствие деполяризации мембраны — возбудимость повышается. В области приложения анода происходит повышение порога раздражения, т.е. снижение возбудимости вследствие гиперполяризации мембраны. Эти изменения возбудимости под катодом и анодом получили название электротона (электротоническое изменение возбудимости). Повышение возбудимости под катодом называется катэлектротоном, а снижение возбудимости под анодом — анэлектротоном.
При дальнейшем действии постоянного тока первоначальное повышение возбудимости под катодом сменяется ее понижением, развивается так называемая католическая депрессия. Первоначальное снижение возбудимости под анодом сменяется ее повышением — анодная экзальтация. При этом в области приложения катода происходит инактивация натриевых каналов, а в области действия анода происходит снижение калиевой проницаемости и ослабление исходной инактивации натриевой проницаемости.
Закон силы
Чтобы возникло возбуждение, раздражитель должен быть достаточно сильным — пороговой или сверхпороговой силы. Потенциал действия возникает только при достижении критического уровня деполяризации клеточной мембраны. Критический уровень деполяризации — минимальная деполяризация клеточной мембраны, при которой возникает потенциал действия. Дальнейшее раздражение клетки не изменяет процесс возникновния ПД, так как деполяризация клетки, достигнув критической величины, способствует открытию потенциалозависимых ворот Na+-каналов, в результате чего ионы натрия устремляются в клетку, ускоряя деполяризацию независимо от действия раздражителя. Критический уровень деполяризации клеточной мембраны нейрона составляет около -50 мВ. В соответствии с этим законом функционируют поперечнополосатые мышцы. Например, амплитуда сокращений скелетной мышцы постепенно увеличивается с нарастанием силы раздражителя до максимальных значений. Это связано с тем, что скелетные мышцы состоят из множества мышечных волокон, имеющих неодинаковую возбудимость. Поэтому сначала на пороговый раздражитель отвечают те мышечные волокна, которые имеют более высокую возбудимость. С увеличением силы раздражителя в реакцию вовлекается все большее число мышечных волокон, поскольку для менее возбудимых из них эта сила будет пороговой. В результате амплитуда сокращения мышцы увеличивается. После возбуждения всех волокон данной мышцы дальнейшее увеличение силы раздражителя уже не приводит к увеличению амплитуды сокращения.
Закон градиента, или аккомодации
Этот закон гласит, что действие раздражителя зависит не только от абсолютной величины его силы, но и от скорости ее нарастания до порогового значения. Например, действие очень медленно нарастающего раздражения не вызывает возбуждения, так как раздражаемая ткань адаптируется к его влиянию. Этот факт объясняется тем, что при действии медленно возрастающего раздражителя в мембране возбудимой ткани увеличивается уровень деполяризации.
При снижении скорости нарастания силы раздражителя до некоторого минимального значения ответная реакция не возникает при любой силе раздражителя. Это явление получило название аккомодации. Причиной аккомодации является инактивация Na+-каналов, возникающая при медленной деполяризации клеточной мембраны, которая длится в течение 1 с и более.
Способность к аккомодации у различных структур неодинакова. Она высокая у нервных волокон и низкая у сердечной мышцы, гладких мышц кишечника и желудка.
Закон «все или ничего»
Сущность этого закона состоит в том, что если на ткань или орган воздействует раздражитель допороговой силы, то при этом не наблюдается ответной реакции («ничего»), а когда используется раздражитель пороговой силы, то наблюдается максимальная ответная реакция («все»). Данный закон проявляется при воздействии на сердечную мышцу или одиночное нервное и мышечное волокно. Однако даже если на раздражители подпороговой силы не возникает ответной реакции, в ткани могут происходить изменения мембранного потенциала покоя.
Закон длительности силы
Согласно этому закону для проявления реакции на раздражитель необходимо не только применять раздражитель пороговой силы, но и обеспечить его действие в течение определенного времени. Чем больше сила раздражителя, тем менее продолжительно он должен действовать для того, чтобы возникло возбуждение.
Зависимость между силой постоянного электрического тока и длительностью его воздействия для появления ответной реакции имеет гиперболический характер. Поэтому воздействие тока ниже минимальной величины не вызовет возбуждение в ткани, как бы длительно он ни действовал. Кроме того, чем короче импульс тока, тем меньше его раздражающая способность. Причиной этой зависимости является неспособность раздражителя осуществить определенный сдвиг мембранного потенциала вследствие кратковременности действия или недостаточной силы раздражителя.
Минимальная величина тока, способная вызвать возбуждение, называется реобазой. Если возбудимость ткани высока, то пороговая сила раздражителя может быть низкой.
Важным условием для возникновения возбуждения при действии раздражителя является его длительность. Поэтому для оценки свойств возбудимой ткани вводится понятие «пороговое время». Пороговое время — минимальное время, в течение которого раздражитель пороговой силы должен действовать на ткань, чтобы вызвать ее возбуждение.
Пороговое время называют также полезным временем. В связи с тем что определить это время достаточно сложно, было введено понятие хронаксии. Хронаксия — минимальное время, в течение которого должен действовать ток в две реобазы, чтобы вызвать возбуждение. Хронаксия измеряется в миллисекундах. Чем меньше полезное время и хронаксия, тем выше возбудимость ткани.
Закон полярного действия постоянного тока
Этот закон проявляется в том, что при действии постоянного тока средней силы на ткань возбуждение возникает только в момент замыкания и в момент размыкания цепи.
Во время замыкания тока возбуждение происходит в участке, расположенном под катодом, а при размыкании — под анодом. Обусловлено это тем, что прохождение постоянного электрического тока через возбудимую ткань вызывает изменение мембранного потенциала покоя ее клеток. В области катода положительный потенциал на наружной поверхности клеточной мембраны уменьшается, и происходит деполяризация мембраны, которая быстро достигает критического уровня и вызывает возбуждение. В области анода положительный потенциал на наружной поверхности мембраны клеток ткани возрастает и развивается гиперполяризация мембраны. При размыкании электрической цепи на аноде мембранный потенциал быстро возвращается к исходному уровню и достигает критической величины, в результате чего открываются ворота Na+ -каналов и возникает размыкательное возбуждение.
4. Мембранный потенциал, его регистрация, механизм возникновения. Натрий-калиевый насос, его физиологическая роль.
Суммарная проводимость для того или иного иона определяется числом одновременно открытых соответствующих каналов. В состоянии покоя открыты только калиевые каналы, обеспечивающие поддержание определенного мембранного потенциала и закрыты натриевые. Поэтому мембрана избирательно проницаема для калия и очень мало для ионов натрия и кальция, за счет имеющихся неспецифических каналов. Соотношение проницаемости мембраны для калия и натрия в состоянии покоя составляет 1:0,04. Ионы калия поступают в цитоплазму и накапливаются в ней. Когда их количество достигает определенного предела, они по градиенту концентрации начинают выходить через открытые калиевые каналы из клетки. Однако уйти от наружной поверхности клеточной мембраны они не могут. Там их удерживает электрическое поле отрицательно заряженных анионов, находящихся на внутренней поверхности. Это сульфат, фосфат и нитрат анионы, анионные группы аминокислот, для которых мембрана не проницаема. Поэтому на наружной поверхности мембраны скапливаются положительно заряженные катионы калия, а на внутренней отрицательно заряженные анионы. Возникает трансмембранная разность потенциалов. Рис.
Выход ионов калия из клетки происходит до тех пор, пока возникший потенциал с положительным знаком снаружи не уравновесит концентрационный градиент калия, направленный из клетки. Т.е. накопившиеся на наружной стороне мембраны ионы калия не будут отталкивать внутрь такие же ионы. Возникает определенный потенциал мембраны, уровень которого определяется проводимостью мембраны для ионов калия и натрия в состоянии покоя. В среднем, величина потенциала покоя близка к калиевому равновесному потенциалу Нернста. Например, МП нервных клеток составляет 55-70 мВ, поперечно-полосатых — 90-100 мВ, гладких мышц — 40-60 мВ, железистых клеток — 20-45 мВ. Меньшая реальная величина МП клеток, объясняется тем, что его величину уменьшают ионы натрия, для которых мембрана незначительно проницаема и они могут входить в цитоплазму. С другой стороны, отрицательные ионы хлора, поступающие в клетку, несколько увеличивают МП.
Так как мембрана в состоянии покоя незначительно проницаема для ионов натрия, необходим механизм выведения этих ионов из клетки. Это связано с тем, что постепенное накопление натрия в клетке привело бы к нейтрализации мембранного потенциала и исчезновению возбудимости. Этот механизм называется натрий-калиевым насосом. Он обеспечивает поддержание разности концентраций калия и натрия по обе стороны мембраны. Натрий-калиевый насос — это фермент натрий-калиевая АТФ-аза. Его белковые молекулы встроены в мембрану. Он расщепляет АТФ и использует высвобождающуюся энергию для противоградиентного выведения натрия из клетки и закачивания калия в неё. За один цикл каждая молекула натрий-калиевой АТФ-азы выводит 3 иона натрия и вносит 2 иона калия. Так как в клетку поступает меньше положительно заряженных ионов, чем выводится из неё, натрий-калиевая АТФ-аза на 5-10 мВ увеличивает мембранный потенциал.
В мембране имеются следующие механизмы трансмембранного транспорта ионов и других веществ:
1.Активный транспорт. Он осуществляется с помощью энергии АТФ. К этой группе транспортных систем относятся натрий-калиевый насос, кальциевый насос, хлорный насос.
2.Пассивный транспорт. Передвижение ионов осуществляется по градиенту концентрации без затрат энергии. Например, вход калия в клетку и выход из неё по калиевым каналам.
3.Сопряженный транспорт. Противоградиентный перенос ионов без затрат энергии. Например таким образом происходит натрий-натриевый, натрий-кальциевый, калий -калиевый обмен ионов. Он происходит за счет разности концентрации других ионов.
Мембранный потенциал регистрируется с помощью микроэлектродного метода. Для этого через мембрану, в цитоплазму клетки вводится тонкий, диаметром менее 1 мкМ стеклянный микроэлектрод. Он заполняется солевым раствором. Второй электрод помещается в жидкость, омывающую клетки. От электродов сигнал поступает на усилитель биопотенциалов, а от него на осциллограф и самописец (рис).
Примером первичного активного транспорта является механизм, под¬
держивающий низкую внутриклеточную концентрацию Na+ и высокую
концентрацию К+ (натрий-калиевый насос) (рис. 2.5). Известно, что в клеточной мембране имеется система переносчиков, каждый из которых
связывается с тремя находящимися внутри клетки Na+ и выводит их нару¬
жу. С наружной стороны переносчик связывается с двумя находящимися
вне клетки К+ , которые переносятся в цитоплазму. Энергообеспечение ра¬
боты систем переносчиков обеспечивается АТФ. Функционирование насо¬
са по такой схеме приводит к следующим результатам.
* Поддерживается высокая концентрация К+ внутри клетки, что обеспе¬
чивает постоянство величины потенциала покоя. Вследствие того что за
один цикл обмена ионов из клетки выводится на один положительный
ион больше, чем вводится, активный транспорт играет роль в создании
потенциала покоя (электрогенный насос). Однако величина вклада элек¬
трогенного насоса в общее значение потенциала покоя обычно невелика
и составляет несколько мВ.
* Поддерживается низкая концентрация Na+ внутри клетки, что обеспе¬
чивает работу механизма генерации потенциала действия и сохранение
нормальных осмолярности и объема клетки.
Примером вторичного активного транспорта может служить механизм
поддержания низкой внутриклеточной концентрации кальция за счет вы¬
сокого натриевого концентрационного градиента. Экспериментально было
показано, что выведение Са2 + уменьшается при удалении Na+ из окружа¬
ющей среды. Доказано, что существует специальный обменный механизм
(переносчик-обменник), источником энергии которого служит высокий
градиент Na+.
Поддерживая стабильный концентрационный градиент Na+ , натрий-
калиевый насос способствует сопряженному транспорту аминокислот и
Сахаров через клеточную мембрану.
Таким образом, возникновение трансмембранной разности потенциа¬
лов (потенциал покоя) обусловлено высокой проводимостью клеточной
мембраны в состоянии покоя для К+ (для мышечных клеток и С1-), ион¬
ной асимметрией концентраций для К+ (для мышечных клеток и для С1-),
работой систем активного транспорта, которые создают и поддерживают
ионную асимметрию.
При выведении кончика микроэлектрода из клетки возвратным движением или прокалывание ее насквозь разность потенциалов между электродами скачкообразно исчезает. Разность зарядов между внутренней и наружной сторонами мембраны клетки называют мембранным потенциалом (МП). В покое эта величина варьирует от -9 до -100 мВ в зависимости от вида ткани и называется мембранным потенциалом покоя (МПП). Следовательно, в состоянии покоя клеточная мембрана поляризована. Уменьшение величины МПП называют деполяризацией, увеличение – гиперполяризацией, восстановление исходного значения – реполяризацией мембраны.
5. Локальный ответ. Особенности местного и распространяющегося возбуждения.
Комплексный потенциал действия | Кривая «сила-продолжительность» | ||||||||||||||||||||||
Цель этой части лаборатории — изучить взаимозависимость между силой стимула и продолжительностью стимула в активации нерва, и построить кривую «сила-продолжительность». | |||||||||||||||||||||||
| |||||||||||||||||||||||
| Мы видели, как форма, амплитуда и продолжительность изменения ВП по мере увеличения силы стимула, потому что постепенно более сильная стимуляция активирует все больше и больше отдельных нервных волокон, индивидуальные потенциалы действия суммируются, чтобы получить ВП.Таким образом, когда стимул сильнее, большее количество волокон достигает порога. | |||||||||||||||||||||||
| Однако порог активации волокна зависит от не только от силы стимула, но и от продолжительность раздражителя. | |||||||||||||||||||||||
| Деполяризация возбудимой мембраны требует прохождения электрического заряда через мембрану.Из-за преобладающая электрическая емкость мембраны, соответствующий параметр для эффективной деполяризации мембраны — общее количество заряда переносится через мембрану. | |||||||||||||||||||||||
| Для кратковременного стимула, вызывающего установившийся трансмембранный ток, переносимый заряд ( Q ) равен пропорционально произведению тока I и времени T : | |||||||||||||||||||||||
Q = I x Т | |||||||||||||||||||||||
Следовательно, если сумма заряда, необходимая для активировать волокно Q t , а длительность стимула D , текущий I t для активации потребуется: | |||||||||||||||||||||||
I т = Q т / D | |||||||||||||||||||||||
| Это говорит о том, что график порога сила стимула по сравнению с продолжительностью стимула должна снизиться до почти ноль при увеличении длительности стимула.Другими словами, стимул сила, необходимая для достижения порога, должна уменьшаться в течение более длительная стимуляция. Обратите внимание, что мы можем использовать напряжение (В) и ток (I) взаимозаменяемо как мера силы стимула. | |||||||||||||||||||||||
| Кривая «сила-продолжительность» для типичного нервная мембрана похожа, но отличается тем, что кривая четко выражена сглаживается с большой продолжительностью стимула, достигая асимптоты, называемой РЕБАЗА.Когда сила стимула ниже реобазы, стимуляция неэффективна даже при очень большой продолжительности стимула. | |||||||||||||||||||||||
Несоответствие наблюдаемой формы кривая «сила-продолжительность», предсказываемая приведенным выше уравнением, обусловлена тем, что что предсказанные отношения верны для идеальный конденсатор , без сопротивление утечке.При длительной стимуляции (большие значения t) уравнение не может предсказать передачу заряда через нервную мембрану, потому что под ними условиях фактический перенос заряда меньше прогнозируемого из-за утечки из-за заметное электрическое сопротивление мембраны . Из-за взаимодействия между резистивными и емкостными эффектами в мембране, перенос заряда (и мембрана потенциал) фактически возрастает экспоненциально до плато во время длительной стимуляции, вместо этого возрастает линейно со временем.Таким образом, если раздражитель слишком мал, мембрана потенциал никогда не достигает порога. | |||||||||||||||||||||||
| При исследовании силы-продолжительности связь в нервном стволе, содержащем тысячи нервных волокон, одно нужно быть осторожным, чтобы определить, какое из этих многих волокон является порогом в вопрос относится к. Пороговое напряжение стимула для CAP как целое на самом деле является порогом для самых быстрых и самых возбудимых волокон в нерве.Поскольку точно определить этот порог сложно, процедура, описанная ниже, использует в качестве опорного сигнала с CAP чей пик амплитуда составляет примерно одну пятую от максимальной. Таким образом, этот порог явно порог для другой менее возбудимой группы волокон. | |||||||||||||||||||||||
| Для начала устанавливается длительность стимула 1.0 мс с помощью ручки на стимуляторе. | |||||||||||||||||||||||
ШАГ A: напряжение стимула медленно увеличивается, пока не появится CAP. В в этом примере мы отрегулировали напряжение пока амплитуда CAP не заполнит два интервала горизонтальной сетки на экране. Эта амплитуда CAP будет использоваться в качестве справочного материала для остальной части эксперимента. (Другой справочная линия также может быть выбрана при условии, что она сохраняется на протяжении всего упражнение) | |||||||||||||||||||||||
Считываем напряжение стимула со стимулятора, а соответствующую длительность стимула (в данном случае 1 мс) и введите эту пару значений в стол.Таким образом, длительность этого стимула и напряжение довели до порогового значения небольшой группа возбудимых волокон в нерве, хотя они не самые возбудимые. | |||||||||||||||||||||||
| ШАГ B: Теперь потихоньку убываем длительность стимула до исчезновения ВП. (Останавливаемся, когда на дисплее отображается плоский линия, где раньше была CAP). | |||||||||||||||||||||||
| Затем повторяем ШАГ A; то есть, увеличивайте стимулирующее напряжение до тех пор, пока CAP не достигнет эталонной амплитуды, указанной выше.(В этом случае заполнение двух интервалов сетки). Читаем новое напряжение стимула и длительность стимула от стимулятора и введите пару значений в таблицу. | |||||||||||||||||||||||
| Эта процедура повторяется до тех пор, пока у нас не будет 10 разные пары значений. По нашим данным построена кривая «сила-продолжительность»: | |||||||||||||||||||||||
| |||||||||||||||||||||||
| Помимо Реобазы, сила-продолжительность
Curve также предоставляет другую информацию — Chronaxie.Chronaxie — это
измерение длительности, соответствующее удвоенному значению Rheobase. Из приведенного выше графика, Rheobase составляет примерно 0,64 вольт, а Хронакси составляет около 0,16 мс. | |||||||||||||||||||||||
| Вопрос: Что такое
значение Реобазы? A: Обычно около отметки 1 мс на кривая сила-продолжительность, кривая сглаживается в реобазе, точке, где прогрессивное увеличение длительности импульса больше не связано с прогрессирующим снижение напряжения.Другими словами, для более длительных стимулов минимальная напряжение, необходимое для доведения нерва до порога, будет реобазой. | |||||||||||||||||||||||
| Q: Каково значение
Хронакси? A: Учитывая, что у двух нервов одинаковые Реобаза, хронакси (длительность стимула, соответствующая удвоенной реобазе) может дают представление об их относительной возбудимости.На кривой «сила-продолжительность» справа нерв В более возбудимый. | |||||||||||||||||||||||
| Q: Как бы
Кривая сила-продолжительность для набора медленных волокон (не очень возбудимых) по сравнению с
Кривая сила-продолжительность для набора быстрых волокон (очень возбудимая)? A: Кривая для более медленных волокна будет смещен вправо, указывая на то, что для данной силы стимула более длительный Длительность стимула потребуется, чтобы довести более медленные волокна до порогового значения. | |||||||||||||||||||||||
Нажмите здесь, чтобы продолжить тему Скорость проводимости (разностный и абсолютный методы) | |||||||||||||||||||||||
Rheobase Медицинское определение | Медицинский словарь Merriam-Webster
рео · база | \ ˈRē-ō-bās \Медицинское определение
реобазы : минимальный электрический ток, необходимый для возбуждения ткани (например, нерва или мышцы) в течение неопределенно длительного времени, в течение которого прикладывается ток — ср. Хронакси.% PDF-1.vH ݾ: q% 3N ؏ # vCn 凸 @ + 5Gz | 8> n8y3P4K2fZ۵t ܣ e9 $ 3H ޞ (l * = kŇ> m #) Ǟ | * p ۼ & 8 j = I {GK.y Np; ‘ow6 = o’mwg8: w {; p7 ~ H ڦ $ s: dT | 9) ‘ON.IGlOOS: [\ > | L = bH ~ = 蝑 g {tGIj:% IA? NSDwNcC * ~ ҕy Jyx {lxCS v] 8 \ [- kp gꪚtb \ pi = n: & s (> Aop | = sIz5wr, -ữ1> E 5K | 63wRvtksjrEy {152ZFI5S ‘{> Yv2A |? .2Sf 41’5srtzn- ޓ1 U e / 5 \: $ 2KSG & W ׳ kgTO \ {: ̓ Z> M ~ | c4 Ӥ҇v | VX = s6kZWSw0F> dS. گ [`@ $ 褝 uJj | (緽 G 2! ҎŠ3, VO | = $ O | 6yt.I =: v | 4 靼 i ‘~ .Nm4} gVҵs> U!% D [)! 9Mfdzb3eYcv
> ylZ1 @ AOp ՝ JdS? = Xi ۭ 1 p2NiCAch «OKmo } \ U} (a $ X | aGlgt] {«$)% F4w / ‘VNF> rc] l҈8 + ؑ» ǢF | IFN6yI} S = _ i7E’ ‘[W:% L = U «ɳJx + = Fy {]) s1 ~ Ih # syR3N69hlifDuFZ.KQ ٱ Ky2 +? U7pumҠx ~ o% Z / -o.oˏϫ) hbl7HC̫e7_z4χf ?? w + (mO \ W՜ * TdH 冯 RwCB (@L Տ Jɪ; Uoun ~ ɑUQ.ZS_ = R [X $ = 4Clya
Chronax Различные ткани | Мышцы | Люди
Возбудимость различных тканей сильно различается. Некоторые ткани очень возбудимы, тогда как другие тупые.
При рассмотрении возбудимости ткани необходимо учитывать два фактора:
(a) Сила используемого тока, и
(b) Продолжительность тока, протекающего через ткань.
Эти два фактора имеют обратную зависимость. Чем сильнее ток, тем меньше потребуется продолжительность. Но есть предел. Установлены два стандарта для измерения возбудимости различных тканей. [Используемые инструменты — жидкостный потенциометр Лапика или пружинный реотом Кейта Лукаса] Эталон прочности (порог интенсивности) называется реобазой. Эталон продолжительности (временная характеристика) Лапик назвал Хронакси.
Реобаза определяется как минимальный гальванический ток, который, если ему позволить бесконечно протекать, будет возбуждать ткань.Хронакси определяется как кратчайшая продолжительность стимула, необходимого для возбуждения ткани силой тока, равной удвоенному напряжению реобазы. Хронаксия ткани — это определенная мера ее возбудимости.
Менее возбудимая ткань имеет более длинную хронаксию, тогда как более возбудимая ткань имеет более короткую. Скорость активности ткани и ее хронаксия имеют прямое отношение. Ткань, имеющая более короткую хронаксию, имеет более короткий период действия, более короткий рефрактерный период и более быструю скорость распространения.
Вялые ткани, такие как некоторая форма гладких мышц, имеют более длительную хронаксию. Из-за этого они не могут быть возбуждены фарадеевской стимуляцией (индукционным шоком), потому что продолжительность тока здесь очень мала.
Хронаксии различных тканей следующие:
и. Хронаксия тканей новорожденного ребенка в десять раз длиннее, чем у взрослых. Это объясняет более медленные движения младенцев.
ii. Ткани хладнокровных животных обычно имеют более длительную хронаксию (т. Е. Они более вялые), чем ткани теплокровных.
iii. Мышцы:
а. Хронаксия скелетных мышц короче, чем у простых и сердечных. Хронаксия мышц-сгибателей короче, чем у мышц-разгибателей. Бледные мышечные волокна (более активные) имеют более короткую хронаксию, чем красные мышцы (вялые).
Усталость удлиняет, а адреналин сокращает хронаксию скелетных мышц.Точно так же холод удлиняет, а тепло укорачивает. Дегенерирующая мышца имеет более длинный хронаксиальный пояс; поэтому его не удается возбудить фарадеевской стимуляцией на ранней стадии реакции дегенерации.
г. Хронаксия простой мышцы длиннее, чем у скелетной мышцы. Стимуляция блуждающего нерва укорачивает, а симпатическая стимуляция удлиняет хронаксию гладких мышц живота. Растяжка уменьшает их хронаксию и увеличивает возбудимость.
г. Сердечная мышца — Хронаксия желудочковых и предсердных мышц такая же, но соединительных тканей в три раза длиннее. Стимуляция блуждающего нерва, растяжения, простуды и ингибирующие препараты, такие как ацетилхолин, укорачивают хронаксию. Тепло, симпатическая стимуляция и препараты-ускорители, такие как атропин, адреналин и т. Д., Удлиняют хронаксию.
iv. Нервы:
Хронаксия вегетативных нервов больше, чем хронаксия соматических нервов. Нервные волокна большего диаметра (которые проводят быстрее) имеют более короткие хронаксии, чем более тонкие (имеющие меньшую проводимость).Хронаксия соответствующих сенсорных и двигательных нервов примерно одинакова.
В дегенерирующем нерве хронаксия удлиняется. [Хронаксия некоторых тканей лягушки следующая: скелетные мышцы — 0,3-0,9 миллисекунды, желудочки — 3,5 миллисекунды, желудок — 30-100 миллисекунд, пигментные клетки кожи — 11000-15000 миллисекунд.]
|
нейрофизиология — В чем разница между реобазой и порогом?
Отличный вопрос! Разница в том, что реобаза является примером меры порога .Порог , порог , как вы правильно предполагаете, — это минимальная энергия (обычно уровень тока, а не напряжение, как вы предлагаете) для возбуждения нервной ткани. Пороговое значение применяется только при определенных используемых настройках экспериментальных параметров. К этим параметрам относятся тип электрического стимула (например, двухфазный импульс тока), конфигурация электродов (например, биполярная стимуляция) и продолжительность стимула (например, 200 микросекунд).
Реобаза — это минимальный уровень тока, необходимый для возбуждения ткани при применении бесконечно длинного стимула .Реобаза обычно находится путем построения графика порогового уровня (как определено выше) как функции длительности стимула. Причина разработки этой меры заключается в том, что возбудимые мембраны интегрируют введенный ток, поэтому в ткани накапливается заряд. Другими словами, увеличение длительности импульса снижает необходимый уровень порогового тока. Следовательно, реобаза является удобной пороговой мерой, поскольку она включает параметр длительности стимула. Это все равно будет зависеть от таких вещей, как конфигурация электродов и форма стимула.
Функцию зависимости силы от продолжительности можно описать убывающей экспоненциальной:
I = I th / (1-e (-t / Tsd) )
где I = пороговый уровень тока; I rh = реобаза t = продолжительность стимула Tsd = Tau = экспонента
Вот изображение теоретической кривой «сила-продолжительность», скопированное с вики-страницы на rheobase. [NB: я считаю вики-страницу излишне сложной].
Реобаза — горизонтальная асимптота.Часто используемый параметр для характеристики функции — хронаксия, которая представляет собой длительность импульса, эквивалентную удвоенной реобазе.
Приведенное здесь объяснение было адаптировано из книги «Кохлеарные имплантаты», глава 5 «Биофизика и физиология» Аббаса и Миллера, двух ветеранов электрофизиологии кохлеарных имплантатов. К сожалению, я не могу дать вам ссылку на pdf, так как у меня есть работа в бумажном виде.
Воздействие злоупотребленного ингалянтом Толуол изменяет физиологию медиальной префронтальной коры
Проекции префронтальной коры в NAcc и NAcs
Крысам вводили флуоресцентные ретробусины в NAcc ( n = 44) или NAcs ( n = 36) на 29–30 сутки после рождения (рис. 2а и б).На рисунке 2c показаны репрезентативные примеры инъекций, демонстрирующие, что ретробусины были ограничены либо NAcc, либо NAc. Период восстановления 10–14 дней для подростков и 65–69 дней для взрослых дал надежную маркировку пирамидных нейронов, выступающих за ядро или оболочку в префронтальной коре (рис. 2c). Пирамидные нейроны, проецирующиеся в NAcc, были расположены по всей ПРЛ и IL mPFC, тогда как пирамидные нейроны, проецирующие NAcs, были в основном локализованы в IL mPFC. Мечение нейронов, проецирующих NAcs, в вентральных частях ПРЛ также наблюдалось, в частности, в слоях 5/6 ПРЛ.
Рисунок 2Экспериментальная временная шкала и локализация ретроградного индикатора в NAc и mPFC. На временной шкале показаны процедуры и возраст крыс для экспериментов с участием подростков (а) и взрослых (б) животных. (c) Типичные изображения и рисунки атласа, показывающие расположение и экспрессию ретробусин. Диаграммы атласа кортикальных срезов головного мозга крысы (перерисованные из Paxinos and Watson, 2005) показывают репрезентативные местоположения инъекций ретробусин в NAc и меченных гранулами нейронах mPFC, используемых для записи.На изображениях показан пирамидный нейрон PRL L5, экспрессирующий флуоресцентные ретробусины (вверху; масштабная линейка 25 мкм), и примеры инъекций ретробусин в ядро (в центре) и оболочку (внизу) NAc.
Слайд PowerPoint
Воздействие толуола вызывает проекционные и субрегиональные изменения внутренней возбудимости пирамидных нейронов mPFC у крыс-подростков
Примерно через 2 недели после введения ретроградных индикаторов крысы-подростки (P41–44) приучали к паровой камере на следующий день подверглись воздействию толуола или воздуха.После воздействия крыс возвращали в их домашнюю клетку и готовили срезы для записи на следующий день. Вызванная активация была значительно снижена в нейронах PRL5 / 6-NAcc от крыс, подвергшихся воздействию толуола, по сравнению с нейронами от контрольных крыс, подвергшихся воздействию воздуха (эффект препарата: F (1,21) = 27,94, p <0,0001 Рисунок 3а). На активацию нейронов PRL2 / 3-NAcc не повлияло воздействие толуола (эффект препарата: F (1,12) = 0,36, p = 0,56; рисунок 3c).В отличие от нейронов PRL5 / 6-NAcc, вызванная активация нейронов IL5 / 6-NAcc была значительно усилена у крыс, подвергшихся воздействию толуола (эффект препарата: F (1,15) = 16,46, p <0,001; фиг. 3д). Подобное увеличение возбуждения также наблюдалось в нейронах IL2 / 3-NAcc (лекарственный эффект: F (1,11) = 7,62, p <0,05; фиг. 3g). Чтобы определить, зависели ли дифференциальные эффекты толуола на возбуждение mPFC от мишени проекции, была определена собственная возбудимость нейронов, проецируемых в NAcs.Лечение толуолом значительно снизило вызванное возбуждение выступающих нейронов IL5 / 6-NAcs (эффект препарата: F (1,17) = 9,70, p <0,01; рис. 3f), но не повлияло на внутреннюю возбудимость PRL5 / 6. -NAcs (эффект лекарственного средства: F (1,14) = 0,34, p = 0,57; рисунок 3b), PRL2 / 3-NAcs (эффект лекарственного средства: F (1,12) = 3,03 , p = 0,11; рис. 3d), или IL2 / 3-NAcs (лекарственный эффект: F (1,13) = 0,57, p = 0.46; Рисунок 3h) нейроны. Эти данные свидетельствуют о том, что определенные связи в цепи вознаграждения mPFC-NAc однозначно нарушаются после кратковременного воздействия толуола.
Рисунок 3Воздействие толуола вызывает селективные изменения субрегиона и проекционной мишени в вызванном током возбуждении нейронов мПФК подросткового возраста. На рисунках показано влияние толуола на активацию прелимбических и инфралимбических нейронов mPFC, проецируемых в ядро (a — воздух: n = 11, толуол: n = 12; c — воздух: n = 7, толуол: n = 7; e — воздух: n = 8, толуол: n = 9; g — воздух: n = 6, толуол: n = 7) или оболочка (b — воздух: n = 8, толуол: n = 8, d — воздух: n = 7, толуол: n = 7; f — воздух: n = 9, толуол: n = 10; h —Воздух: n = 7, толуол: n = 8) NAc.Кривые на каждом рисунке показывают примеры стрельбы (вызванной током с шагом 250 пА) от крыс, подвергшихся воздействию воздуха (левая кривая) или толуола (правая кривая), измеренные через 24 часа после воздействия 10 500 ч / мин. пары толуола. Данные представлены как среднее значение и стандартная ошибка среднего. Символ (*) указывает на основной эффект обработки толуолом на обжиг (двухфакторный дисперсионный анализ с повторными измерениями; p <0,05).
Слайд PowerPoint
Толуол-индуцированная дисфункция мПФК Внутренняя возбудимость пирамидных нейронов временная.
Чтобы определить, сохраняются ли вызванные толуолом изменения в возбуждении более 24 часов, у крыс-подростков через 7 дней после воздействия воздуха или толуола оценивали вызванное толуолом возбуждение.В отличие от изменений, наблюдаемых через 1 день после воздействия толуола, пирамидные нейроны, выступающие из NAcc, не показали изменений в возбуждении через 7 дней после воздействия (PRL5 / 6-NAcc: лекарственный эффект: F (1,10) = 0,16 , p = 0,70; Рисунок 4a, PRL2 / 3-NAcc: лекарственный эффект: F (1,10) = 1,11, p = 0,32; Рисунок 4c, IL5 / 6-NAcc: лекарственный эффект: F (1,10) = 4,58, p = 0,06; Рисунок 4e, IL2 / 3-NAcc: лекарственный эффект: F (1,10) = 0.29, p = 0,60; Рисунок 4g). Точно так же не было различий в возбуждении пирамидных нейронов, проектирующих NAcs, после 7-дневного восстановления после воздействия толуола (PRL5 / 6-NAcs: лекарственный эффект: F (1,10) = 0,14, p = 0,71; Рисунок 4b, PRL2 / 3-NAcs: лекарственный эффект: F (1,10) = 1,43, p = 0,26; Рисунок 4d, IL5 / 6-NAcs: лекарственный эффект: F ( 1,10) = 2,70, p = 0,13; Рисунок 4f, IL2 / 3-NAcs: лекарственный эффект: F (1,10) = 1.55, p = 0,24; Рисунок 4h). Эти данные показывают, что однократное переедание толуолом вызывает временные изменения возбудимости нейронов mPFC, которые варьируются в зависимости как от слоя, так и от мишени проекции NAc.
Рисунок 4Индуцированные толуолом изменения внутренней возбудимости нейронов mPFC-NAc у крыс-подростков являются временными. На рисунках показано влияние толуола на активацию прелимбических и инфралимбических нейронов mPFC, проецируемых в ядро (a — воздух: n = 6, толуол: n = 6; c — воздух: n = 6, толуол: n = 6; e — воздух: n = 6, толуол: n = 6; g — воздух: n = 6, толуол: n = 6) или оболочка (b — воздух: n = 6, толуол: n = 6; d — воздух: n = 6, толуол: n = 6; f — воздух: n = 6, толуол: n = 6; h —Воздух: n = 6, толуол: n = 6) NAc.Кривые на каждом рисунке показывают примеры возбуждения (вызванного током с шагом 250 пА) от крыс, подвергшихся воздействию воздуха (левая кривая) или толуола (правая кривая) через 7 дней после воздействия 10 500 ч / мин. пары толуола. Данные представлены как среднее значение и стандартная ошибка среднего.
Слайд PowerPoint
Взрослые крысы демонстрируют пониженную чувствительность к индуцированным толуолом изменениям внутренней возбудимости пирамидных нейронов mPFC
Чтобы расширить результаты, полученные на подростковых крысах, мы оценили последствия кратковременного воздействия толуола на пирамидные mPFC, выступающие в ядре или оболочке. нейроны взрослых крыс.На момент экспонирования и регистрации возраст этих животных составлял 98–101 день. В отличие от животных-подростков, воздействие толуола в зрелом возрасте не изменяло внутренней возбудимости пирамидных нейронов, проектирующих NAcc, в различных тестируемых субрегионах mPFC (PRL5 / 6-NAcc: лекарственный эффект: F (1,14) = 1,14 , p = 0,30; Фигура 5a, PRL2 / 3-NAcc: лекарственный эффект: F (1,10) = 1,47, p = 0,25; Рисунок 5c, IL5 / 6-NAcc: лекарственный эффект: Факс (1,12) = 2.24, p = 0,16; Фигура 5e, IL2 / 3-NAcc: лекарственное действие: F (1,11) = 0,14, p = 0,72; Рисунок 5g). Точно так же вызванное возбуждение пирамидных нейронов, проектирующих NAcs, у взрослых крыс, получавших толуол, было аналогично воздушному контролю во всех субрегионах (PRL5 / 6-NAcs: лекарственный эффект: F (1,11) = 0,02, p = 0,87; Фигура 5b, PRL2 / 3-NAcs: лекарственный эффект: F (1,10) = 1,23, p = 0,29; Рисунок 5d, IL5 / 6-NAcs: лекарственный эффект: F. (1,14) = 2.07, p = 0,17; Фигура 5f, IL2 / 3-NAcs: лекарственный эффект: F (1,101 = 0,07, p = 0,79; фигура 5h).
Рис. 5Воздействие толуола в зрелом возрасте не влияет на внутреннюю возбудимость нейронов мПФК, проецирующих NAc. На рисунках показано влияние толуола на активацию предлимбических и инфралимбических нейронов mPFC, проецируемых в ядро (a — воздух: n = 8, толуол: n = 8; c — воздух: n = 6, толуол: n = 6; e — воздух: n = 7, толуол: n = 7; g — воздух: n = 7, толуол: n = 6) или оболочка (b — воздух: ). n = 7, толуол: n = 6; d — воздух: n = 6, толуол: n = 6; f — воздух: n = 9, толуол: n = 7; h —Воздух: n = 7, толуол: n = 6) NAc.Кривые на каждом рисунке показывают примеры вызванного током возбуждения (вызванного током с шагом 250 пА) от воздуха (левая кривая) или толуола (правая кривая), подвергнутого воздействию взрослых крыс через 24 часа после воздействия 10 500 ч / мин. пары толуола. Данные представлены как среднее значение и стандартная ошибка среднего.
Слайд PowerPoint
В ходе этих исследований мы отметили, что крысы-подростки выходили из камеры в основном под действием седативных средств и демонстрировали почти полную потерю двигательной функции, которая сохранялась в течение нескольких минут.Напротив, в то время как взрослые крысы демонстрировали явные признаки интоксикации (двигательная несогласованность, атаксия) после воздействия толуола, они не получали полного седативного эффекта. Чтобы определить, будет ли увеличение седативного действия взрослых крыс выявить изменения в возбуждении, группа взрослых крыс получила однократное 20-минутное воздействие толуола, которое вызвало уровень седативного действия и потерю двигательной функции, сопоставимый с таковым у крыс-подростков. Однако, несмотря на этот протокол усиленного воздействия, не наблюдалось изменений внутренней возбудимости пирамидных нейронов mPFC, проектирующих NAcc, у этих животных (PRL5 / 6-NAcc: лекарственный эффект: F (1,12) = 0.04, p = 0,83; Дополнительный рисунок 1a, IL5 / 6-NAcc: лекарственный эффект: F (1,12) = 1,42, p = 0,26; Дополнительный рисунок 1b). Эти данные свидетельствуют о том, что мозг подростка особенно чувствителен к толуолу.
Влияние толуола на электрофизиологические свойства нейронов в mPFC
Для выявления потенциальных механизмов, лежащих в основе влияния толуола на возбудимость mPFC нейронов, мы оценили электрофизиологические характеристики пирамидных нейронов подростков и взрослых крыс, подвергшихся воздействию воздуха или толуола (дополнительная информация , Дополнительная таблица 1).По сравнению с нейронами из контроля воздуха, нейроны PRL5 / 6-NAcc от крыс, подвергшихся воздействию толуола, имели увеличение реобазы ( t (21) = 4,63, p <0,05) и продолжительности спайка (t (21) = 2,20, p <0,05) с уменьшением сопротивления мембраны ( t (21) = 2,33, p <0,05) и I h амплитуда (t (21) = 4.05, p <0,05). Нейроны IL5 / 6-NAcc крыс, подвергшихся воздействию толуола, имели пониженную реобазу ( t (15) = 2.88, p <0,05) и снижение AHP ( t (15) = 2,35, p <0,05) по сравнению с контрольными животными, подвергнутыми воздействию воздуха. Хотя в нейронах PRL2 / 3-NAcc от животных, получавших толуол, значительного изменения вызванной активности не наблюдалось, эти нейроны имели снижение амплитуды AHP ( t (12) = 2,88, p <0,05) по сравнению с нейроны крыс, подвергшихся воздействию воздуха. Не было значительных изменений в мембранных свойствах нейронов IL2 / 3-NAcc у крыс, подвергшихся воздействию воздуха и толуола.Нейроны IL5 / 6-NAcs от крыс, подвергшихся воздействию толуола, имели повышенную реобазу ( t (17) = 2,64, p <0,05), увеличенную продолжительность спайка ( t (17) = 2,17, p <0,05) и уменьшила амплитуду I h ( t (17) = 3,25, p <0,05) по сравнению с контрольными животными, подвергнутыми воздействию воздуха. Не было значительных изменений мембранных свойств нейронов PRL5 / 6-NAc, PRL2 / 3-NAc или IL2 / 3-NAc у крыс, подвергшихся воздействию воздуха и толуола.Кроме того, не было значительных различий в мембранных свойствах нейронов, проецирующих NAcc или NAcs, в любой префронтальной субрегионе крыс-подростков через 7 дней после воздействия толуола (дополнительная информация, дополнительная таблица 2). Однако сопротивление мембраны было увеличено в PRL2 / 3-NAcs ( t (10) = 3,47, p <0,05; дополнительная информация, дополнительная таблица 2), IL5 / 6-NAcs ( t (10 ) = 4,43, p <0,05; дополнительная информация, дополнительная таблица 2) и IL2 / 3-NAcs ( t (10) = 2.79, p <0,05; Дополнительная таблица 2) нейроны. Свойства мембран нейронов, проецирующих NAcc или NAcs, у взрослых крыс, получавших толуол, не отличались от контрольных (дополнительная информация, дополнительная таблица 1).
Затем был проведен анализ методом частичных наименьших квадратов (PLS), чтобы определить, какие данные о свойствах мембраны больше всего связаны с изменениями в пике (Beckley et al, 2015). Тремя переменными с наивысшими показателями переменной в проекции (VIP) были реобаза, продолжительность потенциала действия и анализ I ч .Из этих I h можно напрямую манипулировать, и, таким образом, вызванное током возбуждение было измерено в отсутствие и в присутствии блокатора каналов I h ZD7288. Эти исследования были выполнены с нейронами PRL5 / 6-NAcc, поскольку они показали значительное снижение амплитуды тока I ч ч после воздействия толуола (дополнительная информация, дополнительная таблица 1). Пикинг сначала измеряли в базовых условиях, а затем наносили ZD7288 (20 мкМ) на 10 мин.Поскольку блокада I ч обычно гиперполяризует RMP (Maccaferri and McBain, 1996; Albertson et al, 2011), что само по себе влияет на возбуждение, все нейроны были повторно зажаты до -70 мВ после воздействия ZD7288. В нейронах PRL5 / 6-NAcc от животных, подвергшихся воздействию воздуха, ZD7288 значительно снижал амплитуду I h ( t (5) = 3,37, p <0,05; дополнительная информация, дополнительная таблица 3; рисунок 6a ) и сдвинули влево соотношение пиковых значений тока (эффект ZD: F (1,10) = 5.31, p <0,05; Рисунок 6c). В присутствии ZD7288 возбуждение усиливалось при умеренных токах деполяризации (от +25 до +250 пА), но уменьшалось при более высоких шагах тока. В нейронах PRL5 / 6-NAcc от животных, подвергшихся воздействию толуола, возбуждение в отсутствие ZD7288 было уменьшено по сравнению с контрольным воздухом (рис. 6b), а продолжительность спайка была увеличена ( t (10) = 2,45, p <0,05; дополнительная информация, дополнительная таблица 3), что согласуется с предыдущими выводами. I ч амплитуда также была уменьшена в этих нейронах по сравнению с контрольными элементами в воздухе ( t (10) = 2.30, p <0,05; Дополнительная информация, дополнительная таблица 3). После воздействия ZD7288 произошло умеренное, но статистически незначимое снижение I ч ( t (5) = 2,82, p = 0,17; дополнительная информация, дополнительная таблица 3; рисунок 6b) или возбуждение (эффект ZD: F (1,10) = 1,49, p = 0,25; фиг. 6d) в нейронах PRL5 / 6 от животных, обработанных толуолом. В совокупности эти результаты предполагают, что изменения в функции каналов HCN не являются основным фактором, лежащим в основе изменений в возбуждении нейронов mPFC после воздействия толуола.
Рисунок 6Влияние блокаторов каналов I ч и синаптическая передача на активацию нейронов PRL5 / 6-NAcc mPFC от крыс-подростков, подвергшихся воздействию воздуха или паров толуола. (a и b) Кривые показывают репрезентативные ответы нейронов от воздуха (a; n = 6) или обработанных толуолом (b; n = 6) крыс на шаги гиперполяризации тока в отсутствие (черный) и присутствие (зеленый ) 20 мкМ ZD7288. Сводные графики показывают амплитуду I ч в отсутствие и в присутствии ZD7288.(c и d) Влияние ZD7288 на вызванное током возбуждение нейронов от крыс, подвергшихся воздействию воздуха (c) или толуола (d) в отсутствие (черный) и присутствие (зеленый) ZD7288. (e – h) Влияние блокаторов синаптической передачи на вызванное током возбуждение PRL5 / 6- и IL5 / 6-NAcc mPFC нейронов крыс-подростков через 24 часа после воздействия воздуха (e; n = 6, g; n = 6) или 10 500 частей на миллион пары толуола (f; n = 6, h; n = 6). Кривые на (e – h) показывают примеры возбуждения, вызванного током (вызванного шагом тока 250 пА) в нейронах от животных, обработанных воздухом (слева) или толуолом (справа).Данные представлены как среднее значение и стандартная ошибка среднего. Символ (*) значение значимо ( p <0,05) отличается от контроля (a и b; непарный t -тест; c – h; двухфакторный дисперсионный анализ с повторными измерениями).
Слайд PowerPoint
В последнем наборе исследований записи проводились в присутствии синаптических блокаторов, чтобы определить, могли ли изменения синаптической активности способствовать изменениям собственной возбудимости, наблюдаемым у животных, получавших толуол.После базовых измерений возбуждения aCSF, содержащего коктейль блокаторов (пикротоксин, CGP55845, стрихнин и киневриновую кислоту), перфузировали, и снова измеряли вызванное током возбуждение. Не наблюдалось значительного влияния блокаторов на врожденную возбудимость PRL5 / 6-NAcc (эффект SB: F (1,5) = 0,08, p = 0,79; Рисунок 6e) или IL5 / 6-NAcc ( Эффект SB: F (1,5) = 0,32, p = 0,59; фиг.6g) нейроны крыс, обработанных воздухом.Как уже наблюдалось ранее (Фигуры 3a, e и 6c, d), воздействие толуола при переедании уменьшало возбуждение нейронов PRL5 / 6-NAcc и увеличивало возбуждение нейронов IL5 / 6-NAcc по сравнению с соответствующими контрольными воздухом. Хотя синаптические блокаторы не влияли на возбуждение нейронов PRL5 / 6 у животных, получавших толуол (эффект SB: F (1,5) = 0,64, p = 0,46; рисунок 6f), наблюдалось очень небольшое но статистически значимое снижение возбуждения нейронов IL5 / 6-NAcc от крыс, обработанных толуолом (эффект SB: F (1,5) = 7.28, p <0,05; Рисунок 6h). Анализ свойств мембран выявил незначительное, но значительное увеличение AHP нейронов IL5 / 6-NAcc после перфузии коктейлем синаптических блокаторов (дополнительная таблица 3).
